Отличие транквилизаторов от нейролептиков: ПСИХОТРОПНЫЕ СРЕДСТВА: АНТИДЕПРЕССАНТЫ, ТРАНКВИЛИЗАТОРЫ, НЕЙРОЛЕПТИКИ — В ЧЕМ ОТЛИЧИЕ? или Как не испугаться психиатра. | Врач-психотерапевт Игорь Юров
Психотропные средства: (нейролептики, транквилизаторы).
Нейролептики — это большая группа препаратов, применяемых в лечении психических расстройств. Наибольшей ценностью этих лекарств является способность бороться с психозом, отсюда и второе название — антипсихотики.
Все нейролептики принято классифицировать на две группы:
Типичные нейролептики. Классические антипсихотические препараты. На фоне высоких лечебных возможностей имеют достаточно высокую вероятность развития побочных эффектов. Представители: Аминазин, Галоперидол и др.
Атипичные нейролептики. Современные препараты, отличительной способностью которых является значительно сниженная вероятность развития и выраженность побочных эффектов, в первую очередь — неврологических. К ним относят: Клозапин, Рисполепт, Кветиапин, Оланзапин.
Нейролептики призваны бороться со следующими симптомами:
• психомоторное возбуждение;
• агрессивное и опасное поведение;
• бред и галлюцинации;
• выраженное чувство страха;
• напряжение в теле;
• перепады настроения;
• апатия и вялость при депрессии;
• плохой сон;
• рвота.
Хлорпромазин (Chlorpromazine)(«Аминазин») – первый препарат нейролептического действия, он дает общий антипсихотический эффект, способен купировать галлюцинаторно-параноидный (бредовой) синдром, а также маниакальное возбуждение
Галоперидол (Haloperidol) – наиболее мощный нейролептик, который имеет широкий спектр действия. Купирует все виды возбуждения (кататоническое, маниакальное, бредовое) быстрее, чем трифтазин, и эффективнее устраняет галлюцинаторные и псевдогаллюцинаторные проявления.
Аминазин – ампулы
Rp: Sol. Aminazini 2,5 % — 1 ml
D. t. d. N 6 in ampull.
S. В/м, предварительно развести в 5 мл 0,5 % растворе новокаина.
Галоперидол — таблетки
Rp: Tab. Haloperidoli 0,0015
D. t. d. N 50
S. По 1 таблетке 3 раза в день.
Транквилизаторы — успокаивающие средства, способные устранять страх, тревогу, эмоциональное напряжение.
Они обладают центральным миорелаксантным и противосудорожным эффектами. В отличие от нейролептиков не имеют антипсихотической активности, практически не влияют на вегетативную нервную систему, не дают экстрапирамидных расстройств.
Применяются они при невротических состояниях, для снятия эмоционального напряжения, тревоги, для устранения невротических реакций при гипертонической болезни, ИБС, язвенной болезни желудка, кожных заболеваниях: препараты часто используют в анестезиологии для медикаментозной подготовки больных к различного рода болезненным манипуляциям, в том числе и у врача-стоматолога.
Транквилизаторы по химическому строению делят на:
1) производные бензодиазепина: хлордиазепоксид (элениум) , диазепам (сибазон, седуксен, реланиум
2) препараты разных химических групп: мепротан, бенактизин (амизил), фенибут, мебикар,.
Механизм действия транквилизаторов связан с угнетением структур мозга (лимбической системы, гипоталамуса, ретикулярной формации ствола мозга, таламических ядер), ответственных за регуляцию эмоциональных реакций. В настоящее время хорошо изучен механизм действия производных бензодиазепина.
Седативный (успокаивающий) эффект связан с действием препаратов на другой тип бензодиазепиновых рецепторов, локализованных в ретикулярной формации ствола мозга, неспецифических ядрах таламуса.
Способ применение: В/м, в/в, таблетки.
Сибазон (Диазепам) — ампулы
Rp: Sol. Sibazoni 0,5 % — 2 ml
D. t. d. N 10 in ampull.
S. По 2 мл в/м 1-2 раза в сутки.
Психотропные средства: (антидепрессанты, психостимуляторы, ноотропы).
Психотропные лекарственные средства
Группа Антидепрессанты
Группа Ноотропные препараты
Группа Средства, стимулирующие ЦНС
Подгруппа а) Психомоторные стимуляторы
(пр.пурина и имидазола, арилалкиламины)
в) Стимуляторы функций спинного мозга
г) Средства «тонизирующие» ЦНС
(растительные)
Типовые механизмы действия психоаналептиков
1. Стимуляция адренергических, дофаминовых и серотонинергических структур (непосредственная или опосредованная через депонирование, выброс, захват, обмен) — Психостимуляторы (неизбирательная стимуляция коры и подкорки), Антидепрессанты (избирательная стимуляция лимбической системы)
2. Стимуляция обменных процессов в ЦНС(активация передачи возбуждения в коре головного мозга — Ноотропы
3.
4. Блокада тормозных рецепторов — Стрихнин
5. Блокада аденозиновых рецепторов— Кофеин
АНТИДЕПРЕССАНТЫ — лекарственные средства, устраняющие депрессии (эмоциональной подавленности, тоски, угнетенности)
депрессия— это длящееся не менее двух недель сниженное большую часть дня патологически подавленное настроение
2 варианта депрессии (в зависимости от типа наиболее выраженного аффекта)
- Апатическая депрессия (тоскливая депрессия)
- Тревожная депрессия
КЛАССИФИКАЦИЯ
I. ИНГИБИТОРЫ МАО— в основном предназначена для лечения апатического и тоскливого вариантов депрессии
II. ИНГИБИТОРЫ НЕЙРОНАЛЬНОГО ЗАХВАТА(в основном предназначены для лечения тревожного варианта депрессии)
- Неизбирательные (трициклические — Амитриптилин, тимолептики – с седативным эффектом)
- Избирательные ингибиторы обратного захвата— безопаснее
а) Серотонина: Флуоксетин — стимулятор, Сертралин – нейтральный
АМИТРИПТИЛИН(Amitriptylinum)антидепрессивный + седативный эффекты
(устраняет тревогу и страх).
Форма выпуска. Драже или таблетки по 25 мг, р-р для инъекций.
Препараты 2 поколения, избирательно ингибирующие обратный захват серотонина — флюоксетин, флювоксамин, сертралин, циталопрам, пароксетим.
По эффективности селективные ингибиторы обратного захвата серотонина приблизительно равны классическим антидепрессантам, но зато они значительно более безопасны.
ПСИХОСТИМУЛЯТОРЫ
Это лекарственные средства повышающие психомоторную активность (восприятие, память, настроение, физическую и умственную работоспособность), снижающие потребность во сне и чувство усталости .
Известно огромное количество психостимуляторов, почти все они относятся к допинговым средствам.
КЛАССИФИКАЦИЯ ПСИХОСТИМУЛЯТОРОВ
1. Производные фенилалкиламина(катехоламины)
Амфетамин (Фенамин), Первитин
2. Производные фенилалкилпиперидина
Меридил, Пиридрол, Метилфенидат, Пемолин
3. Производные фенилалкилсиднонимина
Мезокарб (Сиднокарб), Фепрозидин (Сиднофен), Сидноглутон
4. Производные пурина
Сaffeine (Кофеин, Кофеин-бензоат натрия)
5. Производные бензимидазола
Бемитил
ОБЩАЯ ХАРАКТЕРИСТИКА ПСИХОСТИМУЛЯТОРОВ:
Типовой механизм действия— центральный симпатомиметический эффект, обусловленный выбросом эндогенных катехоламинов из пресинаптических депо, угнетение обратного захвата медиатора и увеличением его концентрации в синоптический щели, прямым воздействием на постсинаптические адренорецепторы, торможением моноаминоксидазы
Основной фармакологический эффект
Сфера применения— повышенная утомляемость, сонливость, легкая депрессия, отравления веществами. угнетающими ЦНС.
Важнейший представитель — КОФЕИН* (Caffeine)
I. Центральное действие:
мягкий и непродолжительный «нисходящий» дозозависимый стимулирующий эффектна все отделы ЦНС; (по мере увеличения дозы — возбуждение коры головного мозга, затем продолговатого мозга, далее — спинного мозга).
Три вида центральной активности кофеина:
2. Аналептическая активность— в высоких дозах стимулирует центры продолговатого мозга — вагусный, сосудодвигательный и дыхательный.
3. Облегчение рефлекторной передачи возбуждения в спинном мозге.
НООТРОПЫ— лекарственные средства, оказывающие прямое активирующее влияние на обучение, улучшающие память и умственную деятельность, а также повышающие устойчивость организма к агрессивным воздействиям
КЛАССИФИКАЦИЯ НООТРОПОВ
Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
что такое, принцип действия, в чем разница между транквилизаторами и антидепрессантами?
Ежедневный стресс давно стал реальностью для большинства россиян, живущих в мегаполисах. Повышенный темп жизни, неприятности на работе, недостаток сна и отдыха приводят к появлению раздражительности, тревоги и беспокойства, эмоциональному напряжению. В результате снижается работоспособность, возникают проблемы со сном, а отдых не приносит полноценного расслабления. Уменьшить действие стрессовых факторов, снизить уровень тревожности и обрести эмоциональную стабильность помогают транквилизаторы… Но какой ценой?
Разбираемся в понятиях
Свое название транквилизаторы получили от латинского слова tranquillo — «успокаивать». Транквилизаторы относятся к психотропным препаратам, то есть оказывают влияние на центральную нервную систему. Они имеют успокаивающее действие, уменьшают тревожность, страхи и любое эмоциональное напряжение. Механизм их действия связан с угнетением структур мозга, отвечающих за регуляцию эмоциональных состояний. Наиболее полно изучено действие средств, являющихся производными бензодиазепина, — именно к ним относится большинство транквилизаторов, представленных сегодня на рынке (есть и препараты, не относящиеся к данной группе, о них мы поговорим далее).
Бензодиазепины — вещества, снижающие возбудимость нейронов за счет воздействия на рецепторы ГАМК (гамма-аминомасляной кислоты). Большинство соединений из группы бензодиазепинов являются транквилизаторами, некоторые используются как снотворные средства. При долговременном использовании могут вызывать привыкание и физическую зависимость.
Часто транквилизаторы путают с антидепрессантами, считая эти термины синонимами. В чем же разница между транквилизаторами и антидепрессантами? Антидепрессанты относятся к психотропным средствам, стимулирующим нервную систему, тогда как транквилизаторы — к угнетающим. То есть антидепрессанты повышают эмоциональную активность и улучшают настроение, а транквилизаторы — успокаивают.
Успокаивающие средства делятся на 3 основных группы (классификация транквилизаторов):
- Нейролептики, или «большие» транквилизаторы, — антипсихотические препараты, которые применяются в основном при шизофрении и других тяжелых психических заболеваниях, сопровождающихся чувством тревоги, страха и двигательным возбуждением.
- Анксиолитики (от латинского «anxietas» — тревожное состояние, страх, и древнегреческого «???????» — ослабляющий), или «малые» транквилизаторы, — сейчас именно они чаще всего понимаются под транквилизаторами, а нейролептики перестают считаться таковыми.
- Седативные средства — препараты, действие которых главным образом направлено на торможение нервной системы и улучшение качества сна.
В данной статье под термином «транквилизаторы» мы будем понимать только препараты из группы анксиолитиков, как и принято в современной медицине.
Основное действие транквилизаторов
Анксиолитики могут обладать различными эффектами, выраженность которых варьируется у разных препаратов. Некоторые анксиолитики, например, не обладают снотворным и седативным действием. В целом препараты данной группы оказывают следующие действия:
- Противотревожное — уменьшение тревоги, страха, беспокойства, устранение навязчивых мыслей и излишней мнительности.
- Седативное — уменьшение активности и возбудимости, сопровождается снижением концентрации, заторможенностью, сонливостью.
- Снотворное — увеличение глубины и длительности сна, ускорение его наступления, в первую очередь свойственно бензодиазепинам.
- Миорелаксантное — расслабление мускулатуры, которое проявляется слабостью и вялостью. Является положительным фактором при снятии стресса, однако может оказать отрицательное действие при работе, требующей физической активности, и даже при работе за компьютером.
- Противосудорожное — блокирование распространения эпилептогенной активности.
Кроме того, некоторые транквилизаторы оказывают психостимулирующее и антифобическое действие, могут нормализовать активность автономной нервной системы, однако это, скорее, исключение, чем правило.
Первый транквилизатор, синтезированный в 1952 году, — мепробамат. Широкое применение анксиолитики получили в 60-е годы XX века.
Преимущества и недостатки приема анксиолитиков
Общие показания к применению транквилизаторов следующие:
- Неврозы, сопровождающиеся тревожными состояниями, раздражительностью, страхами и эмоциональным напряжением, неврозоподобные состояния.
- Соматические заболевания.
- Посттравматическое стрессовое расстройство.
- Уменьшение влечения к курению, алкоголю и психоактивным веществам (синдром «отмены»).
- Предменструальный и климактерический синдромы.
- Расстройство сна.
- Кардиалгия, ишемическая болезнь сердца, реабилитация после инфаркта миокарда — в составе комплексного лечения.
- Улучшение переносимости нейролептиков и транквилизаторов (для устранение их побочных эффектов).
- Реактивная депрессия.
- Эпилепсия — в качестве вспомогательного средства.
- Спазмы, ригидность мышц, судороги, тики.
- Психотические и подобные состояния.
- Профилактика эмоционального напряжения.
- Вегетативные дисфункции.
- Функциональные расстройства ЖКТ.
- Мигрени.
- Панические состояния и др.
Нужно учитывать, что большинство анксиолитиков не назначаются (!) при повседневном стрессе, их прием имеет смысл только при острых стрессовых состояниях и в экстремальных ситуациях. Бензодиазепиновые транквилизаторы нельзя употреблять во время беременности и кормления грудью. Помните: лечение транквилизаторами может проводиться только под наблюдением врача.
Противопоказаниями к приему транквилизаторов бензодиазепинового ряда являются: печеночная и дыхательная недостаточность, атаксия, глаукома, миастения, суицидальные наклонности, алкогольная и наркотическая зависимость.
К минусам бензодиазепиновых транквилизаторов также относится формирование зависимости. Возможно возникновение синдрома отмены при прекращении приема. В связи с этим Согласительная комиссия ВОЗ не рекомендовала (!) применять транквилизаторы бензодиазепинового ряда непрерывно более 2–3 недель. При необходимости длительного лечения по истечении 2–3 недель следует прекратить прием на несколько дней, после чего возобновить его в той же дозировке. Синдром отмены можно уменьшить или избежать его полностью, если перед прекращением приема транквилизаторов постепенно снижать дозу и увеличивать интервал между приемами.
Транквилизаторы — достаточно эффективные препараты, имеющие тем не менее существенные противопоказания и недостатки. Именно поэтому они, как правило, отпускаются в аптеках строго по рецепту. В связи с этим современная медицина продолжает поиск успокаивающих средств с минимальными побочными действиями, более эффективных и безопасных, не вызывающих зависимости.
Безрецептурный препарат как альтернатива транквилизаторам
Безрецептурных транквилизаторов, включенных в международную систему классификации лекарственных средств, зарегистрированных на территории России, очень мало. Один из таких препаратов, принадлежащих к последнему поколению, — «Афобазол». Это уникальная альтернатива транквилизаторам при тревожных состояниях, различных соматических заболеваниях, при нарушениях сна, предменструальном синдроме, алкогольном абстинентном синдроме, при отказе от курения и возникновении синдрома отмены.
Афобазол — небензодиазепиновый анксиолитик и при его приеме не возникает привыкания. Он оказывает противотревожное и легкое стимулирующее действие, не вызывает сонливости и заторможенности, а значит, может применяться в рабочее время. Также «Афобазол» не вызывает мышечной слабости, не влияет на концентрацию внимания. После окончания приема не возникает синдрома отмены. Препарат имеет минимальные побочные действия, которые могут заключаться в аллергических реакциях и временной головной боли. Препарат имеет некоторые противопоказания, а потому перед его приемом следует проконсультироваться со специалистом.
P.S. «Отисифарм» — крупнейшая в России фармацевтическая компания, производитель безрецептурных препаратов, одним из которых является «Афобазол».
36) Нейролептические средства. Отличия от транквилизаторов. Показания к назначению.
36) Нейролептические средства. Отличия от транквилизаторов. Показания к назначению.Нейролептики по химическому строению делятся на следующие группы:
В нарушении психической деятельности большое значение имеет изменение основных медиаторных систем в соответствующих структурах мозга (ретикулярной формации, лимбической системе, гипоталамусе). Так, психические расстройства при шизофрении(мании, бред, галлюцинации) возникают при гиперфункции дофаминовых систем; Психоэмоциональное напряжение, тревога, страх, связаны с повышением роли адренергических, серотонинергических систем.Нейролептики, обладая способностью вмешиваться в обмен определенных медиаторных структур мозга , уравновешивают медиаторный фон. Проникая в головной мозг. они блокируют дофаминовые, адренергические, серотонинергические, холинергические рецепторы, либо тормозят выброс соответствующих медиаторов, а также могут инактивировать их в нервном окончании.
Фармакологические свойства.Нейролептики оказывают многогранное действие, вызывают многозвеньевую блокаду центральной и вегетативной нервной системы. Препараты имеют своеобразный успокаивающий эффект, снижают психомоторное возбуждение, двигательную активность, агрессивность; вызывают безразличие к окружающей среде, эмоциональную «тупость», тормозят условно- рефлекторную деятельность и даже подавляют рефлекс избегания опасности. Успокаивающее действие нейролептиков связано с угнетением адренергической и серотонинергической передачи в ретикулярной формации, ядрах среднего мозга. За счет выраженного успокаивающего эффекта нейролептики потенцируют и пролонгируют действие средств, угнетающих центральную нервную систему (общих анестетиков, снотворных, болеутоляющих и др.). Все эти препараты, в отличие от других успокаивающих, обладают антипсихотическимдействием (снимают бред, галлюцинации). Этот эффект объясняется блокадой дофаминовых рецепторов в головном мозге. При шизофрении в определенных его структурах увеличивается плотность дофаминовых рецепторов. Нейролептики ее снижают. Они уменьшают также количество синаптического дофамина. Со снижением дофаминовой активности связано не только антипсихотическое действие, но и основной побочный эффект этих препаратов — экстрапирамидные расстройства (лекарственный паркинсонизм): нейролептики блокируют дофаминовую передачу в черной субстанции, что приводит к растормаживанию стриопаллидарной системы. Экстрапирамидные расстройства менее характерны для нейролептиков, обладающих центральной холинолитической активностью и избирательно блокирующих дофаминовые рецепторы лимбической системы и коры мозга. Нейролептики угнетают вегетативную нервную систему, многие из них обладают a-адреноблокирующим действием (аминазин, дроперидол и др.), расширяя сосуды, снижают артериальное давление. Кроме того, некоторые нейролептики проявляют М-холиноблокирующие свойства (вызывают тахикардию, снижают секрецию слюнных, бронхиальных и пищеварительных желез). Резерпин является симпатолитиком, уменьшает количество норадреналина в окончаниях симпатических нервов и снижает артериальное давление. Нейролептикам свойственна антигистаминная и антисеротониновая активность. Ряд нейролептиков (галоперидол, дроперидол, этаперазин, аминазин) подавляют рвоту и икоту. Они блокируют дофаминовые рецепторы триггерной зоны продолговатого мозга, импульсы с которой стимулируют рвотный центр. Препараты предупреждают и снимают рвоту, вызванную лучевой и химиотерапией злокачественных новообразований, передозировкой препаратов наперстянки и др. Многие нейролептики оказывают гипотермическое действие. Они способны снижать не только повышенную, но и нормальную температуру тела, так как увеличивают теплоотдачу (блокада α-адренорецепторов приводит к расширению периферических сосудов) и уменьшают теплопродукцию (понижают активность дыхательных ферментов, вследствие чего падает потребление кислорода и тормозится интенсивность обменных процессов). Гипотермический эффект нейролептиков используется в хирургии для искусственного охлаждения организма при операциях на сердце, мозге. Некоторые препараты (аминазин,тизерцин и др.) обладают умеренным противовоспалительным действием: уменьшают проницаемость сосудов, понижая активность кининов и гиалуронидазы. Нейролептики через блокаду дофаминовых рецепторов нарушают контроль гипоталамуса за продукцией и высвобождением тропных гормонов (увеличивается секреция пролактина и снижается -кортикотропина, соматотропного гормона).Применение нейролептиков:
3. При абстинентном синдроме у алкоголиков.
5. Для создания искусственной гипотермии (при операциях на сердце, мозге).
6. Для купирования гипертонических кризов (дроперидол) и лечения гипертонической болезни (резерпин). Нейролептики, блокирующие a-адренорецепторы (аминазин, тизерцин, дроперидол и др.), при парентеральном введении могут вызвать снижение артериального давления, вплоть до коллапса. При длительном назначении некоторых препаратов (аминазин, резерпин) развиваетсядепрессия, проявляется гепато- и гематотоксичность. За счет действия на дофаминовые рецепторы гипоталамуса нейролептики могут приводить к эндокринным нарушениям (как правило, обратимым): увеличивается масса тела, вплоть до ожирения, нарушается менструальный цикл, снижается потенция и др. При длительном лечении, особенно препаратами из группы фенотиазина, появляется кожная сыпь, может развиться контактный дерматит, фотосенсибилизация. Вследствие образования меланина кожа окрашивается в желто-коричневый или красноватый цвет. Этот пигмент может появиться в печени, в почках, в мозге, сетчатке и роговице глаза. При пигментной ретинопатии изменяется зрение к тяжелым последствиям (вплоть до внезапной смерти) приводит пигментация внутренних органов. Каждая группа нейролептиков и отдельные препараты имеют свои особенности. Производные фенотиазина оказывают сильное успокаивающее действие и менее выраженное антипсихотическое. Сульпирид оказывает «регулирующее» действие: сочетает умеренную нейролептическуюактивность с антидепрессантными свойствами и слабым успокаивающим эффектом, однако при наличии у больных вялости и заторможенности, напротив, вызывает мягкую стимуляцию.В основном нейролептики назначают для подавления у человека симптоматики психозов, но в малых дозах их назначают довольно широко и при неврозах. Нейролептики обладают возможностью “убирать” навязчивости, тревогу, беспокойство, ажитацию. У нейролептических средств есть одно очень существенное отличие от транквилизаторов, они не обладют способностью вызывать у человека эйфорию, они не накапливают потенциал зависимости. Иными словами, нейролептики не вызывают привыкания. Но при повышенной чувствительности к препарату, неверно подобранный нейролептик или/и его дозировка есть вероятность развития нейролептического (экстрапирамидного) синдрома. Что такое экстрапирамидный синдром – это комплекс двигательных нарушений включающих в себя такие явления, как ригидность, тремор, брадикинезию. Поэтому при появлении “экстрапирамидки” прием нейролептика сразу прекращают или в крайнем случае уменьшают его дозу, и начинают прием противопаркинсонических препаратов, таких как циклодол, леводопа. Чаще экстрапирамидный синдром возникает при применении фенотиазинов (трифтазина), галоперидола. Реже при приеме атипичных нейролептиков – рисперидона, зипрексы, сероквеля. Поэтому не занимайтесь самолечением! Прежде чем начинать пить нейролептик, посоветуйтесь с лечащим врачом.
Разница между антидепрессантами и транквилизаторами
Когда сил организма недостаточно для того, чтобы поддерживать современный ритм жизни, на помощь нервной системе приходят специальные медикаменты — антидепрессанты и транквилизаторы, и в чем разница между ними, необходимо знать, чтобы сделать правильный выбор.
Антидепресанты
Эти психотропные лекарственные средства чаще всего применяются для лечения депрессии. Их действие направлено на регулирование количества нейромедиаторов, «гормонов счастья». На фоне приема антидепрессантов у больного пропадает бессонница, возвращается аппетит. Тоска и апатия уступают место нормальному настроению, вялость и навязчивые мысли уходят.
Если депрессии нет, то антидепрессанты не улучшат настроение. Они рассчитаны на борьбу с болезнью и не являются средством для мгновенного улучшения настроения.
Врачами в медицинской практике антидепрессанты делятся на несколько групп. В зависимости от спектра действия выбирают медикаменты той группы, что поможет справиться с наиболее выраженными клиническими проявлениями болезни.
Существует 3 основные группы антидепрессантов:
- седативные средства;
- стимуляторы;
- препараты широкого спектра действия.
Лекарства помогают от бессонницы, улучшают настроение или регулируют некоторые процессы мышления.
Эти препараты не рекомендуется принимать бесконтрольно и назначать себе самостоятельно. Даже для лечения легкой степени депрессии их не назначают. Некоторые ученые считают, что антидепрессанты способны нанести больше вреда пациенту, чем оказать помощи в лечении.

Такие медикаменты рассчитаны на длительный курс терапии. Первые улучшения могут наступить лишь спустя месяцы. Даже самые быстрые антидепрессанты начинают действовать не ранее чем чрез 7-10 дней после начала их приема. Поэтому важно придерживаться схемы лечения, рекомендованной врачом, и не ждать результата сразу.
Прием такого психотропного средства редко обходится без побочных действий. Особенно в первые 3-4 недели применения препарата. Возможно обострение суицидальных мыслей, усиление признаков агрессии. Если проявляются такие побочные эффекты, врач отменяет препарат или пересматривает его дозировки. Во избежание рецидива болезни нельзя резко отменять прием этих медикаментов.
Прекращают прием препарата, понижая его дозировку в течение как минимум 3-4 недель.
На фоне приема медикамента могут развиваться вялость, сонливость и тревожность. Прием некоторых антидепрессантов снижает концентрацию внимания и сексуальные функции пациента. При использовании некоторых препаратов запрещается управлять автомобилем.
Применение препарата под наблюдением специалистов, в назначенных дозировках и по рекомендованной схеме лечения безопасно и принесет пользу. Самолечение недопустимо и способно нанести вред здоровью.
Отличия от транквилизаторов
Сравнение антидепрессантов и транквилизаторов не совсем корректно. Это два различных по химическому составу и терапевтическому действию лекарства. Их применяют для лечения разных болезней. Только врач может принять решение, что лучше для терапии того или иного состояния.
Антидепрессанты назначают для лечения депрессивных состояний, тогда как транквилизаторы призваны бороться с тревогами и страхами разной степени тяжести. Большинство транквилизаторов оказывают релаксирующее воздействие, при этом седативный эффект отсутствует. Хотя существуют и специальные «ночные» лекарства, которые обладают снотворным действием.
Транквилизаторы отлично борются с такими тревожными состояниями, как страх, паника, беспокойство. Справляются с навязчивыми мыслями, помогают при обострении психопатии и нервозности. Не влияют на управление транспортными средствами, не притупляют внимание, а, напротив, усиливают мозговую деятельность. В этом свойстве проявляется их существенное отличие от антидепрессантов.
Транквилизаторы назначают непродолжительным курсом, с постепенной отменой препарата. Действие проявляется намного быстрее, чем при приеме антидепрессантов. Иногда транквилизаторы прописывают даже для эпизодического применения, например для купирования панической атаки.
Даже самые сильные подобные медикаменты практически не имеют выраженных побочных действий, в отличие от антидепрессантов. Если строго следовать рекомендациям врача по дозировкам и схеме лечения, то побочных явлений удастся избежать.
Если дозировка транквилизаторов подобрана неверно, возможны сонливость, заторможенность и рассеянность внимания. Может понизиться давление, появиться головокружение и тошнота. Острота зрения может также снизиться. Побочными проявлениями приема препарата могут стать астения и слабость или отсутствие полового влечения.

Самыми неприятными побочными действиями транквилизаторов являются синдром отмены и возможность привыкания. Кратковременность курса лечения транквилизаторами обусловлена возникновением устойчивой зависимости от препарата. Таких побочных эффектов при приеме антидепрессантов не возникает.
Антидепрессанты могут не оказать никакого эффекта на пациента, если депрессии нет. Тогда как транквилизаторы всегда действуют, даже если психика человека здорова.
Следует обратить внимание, что транквилизаторы и антидепрессанты нельзя назначать самостоятельно. Эти средства продаются в аптеках только по рецепту врача.
Отличия от нейролептиков
Нейролептики — это своего рода «большие» транквилизаторы. Они тоже призваны бороться с тревогами и страхами. Кроме того, НЛ способны снять психозы и острые проявления неврозов.
Большинство нейролептиков проявляют выраженный седативный эффект. Из-за этого при их приеме запрещено управление транспортными средствами. Нейролептики имеют большой список противопоказаний и способны нанести ощутимый вред здоровью при бесконтрольном применении, начиная от нейролептического синдрома и заканчивая проявлениями общей слабости и угнетенного состояния. При приеме таких медикаментов обязательно нужно следить за изменениями в крови пациента. Отменять следует так же, как и АД, — только постепенно, под врачебным контролем.

Нейролептики применяются в психиатрии для лечения таких тяжелых заболеваний, как шизофрения, БАР, психозы и различные поведенческие отклонения. Если антидепрессанты и транквилизаторы некоторые назначают себе самостоятельно, то нейролептики для самолечения применяют крайне редко.
Как и АД, нейролептики назначают только длительными курсами. Их действие проявляется не сразу, а по прошествии длительного времени. Хотя многое зависит от дозировки препарата, большие дозы способны быстро снять острый психоз.
Главное назначение нейролептиков — снять психоз, убрать агрессию и откорректировать тем самым поведение пациента. Несмотря на видимые отличия трех лекарственных групп, иногда специалисты выписывают пациенту сразу антидепрессанты, транквилизаторы и нейролептики. Такой комплексный подход дает хорошие результаты при борьбе с тяжелыми психическими состояниями.
Антидепрессанты, транквилизаторы и нейролептики — лекарственные средства, призванные вернуть человеку душевное равновесие и помочь снова получать от жизни положительные эмоции.
Статья мне нравитсяСтатья не нравитсяТранквилизаторы и антидепрессанты: в чем разница?

Широкое распространение психоневрологических заболеваний стало толчком для поиска препаратов, которые бы эффективно помогали в лечении болезней.
Сегодня фармакологический рынок представлен большим количеством лекарственных средств, которые относятся к разным группам, отличаются по механизму действия, сфере применения, количеству побочных реакций.
Все препараты по влиянию на ЦНС можно условно разделить на две большие группы:
- Средства с угнетающим действием (нейролептики, средства для наркоза, противоэпилептические средства, транквилизаторы, болеутоляющие и др.).
- Средства со стимулирующим действием (ноотропы, аналептики, антидепрессанты, психостимуляторы).
Антидепрессанты и транквилизаторы относятся к классу психотропных веществ, однако первые стимулируют работу ЦНС, а вторые – угнетают.
Транквилизаторы
 Транквилизаторы показаны там, где необходим угнетающий нервную систему эффект: при различных фобиях, тиках, судорожном синдроме и так далее.
Транквилизаторы показаны там, где необходим угнетающий нервную систему эффект: при различных фобиях, тиках, судорожном синдроме и так далее.Термин «транквилизаторы» произошел от латинского слова tranquillo, что означает спокойствие, безмятежность. Эра транквилизаторов началась с 1952 г., когда был синтезирован первый препарат — мепробомат.
Они применяются в лечении следующих состояний:
- Невротические реакции на стресс, страхи (фобии), эмоциональное напряжение.
- Неврозоподобные реакции (тики, анорексия, заикания).
- Нарушение сна.
- Премедикация (вспомогательная терапия перед наркозом).
- Гиперкинезы.
- Судорожные состояния.
Также в медицинской литературе для обозначения этой группы препаратов используют термины «анксиолитики» или «противотревожные средства», но обозначение «транквилизаторы» остается наиболее распространенным.
Молекулярное строение препаратов весьма различается, они могут относиться к разным группам химических соединений, но большинство средств оказывают (в разной степени) все ниже перечисленные эффекты.
Выделяют пять основных механизмов действия лекарственных средств данной группы:
- Анксиолитическое действие (противотревожное, антифобическое) проявляется уменьшением симптомов тревожности, страха.
- Снотворное действие. Препараты облегчают наступление сна, который по своим показателям близок к физиологическому.
- Седативное действие выражается в появлении у человека заторможенности, сонливости в дневные часы, снижения концентрации внимания. Лекарственные средства способствуют снижению скорости реакций, усиливают угнетающее действие алкоголя на центральную нервную систему.
- Миорелаксирующее действие связано с влиянием на ЦНС, что приводит к уменьшению напряжения.
- Противосудорожное действие.
Механизм действия связан с влиянием транквилизаторов на подкорковые структуры (гипоталамус, лимбическая система, ретикулярная формация и др.), которые отвечают за эмоциональное поведение человека.
Стоит отметить, что при приеме транквилизаторов достаточно быстро наступает купирование симптомов тревоги, страха невротического происхождения, но они не оказывают большого влияния на галлюцинации или бредовые состояния.
Классификация транквилизаторов основывается на их способности воздействовать на разные виды рецепторов в ЦНС.
- Агонисты бензодиазепиновых рецепторов (сибазон, феназепам и др.).
Связываются с ГАМК-рецепторами в ЦНС, усиливая тормозное влияние ГАМК на подкорковые структуры.
Бензодиазепины представлены большим количеством лекарственных средств, которые отличаются между собой по длительности действия, оказываемому эффекту.
Например, к препаратам, которые обладают длительным воздействием на организм, относят диазепам, феназепам, средняя продолжительность действия у лоразепама, короткая — у мидазолама. Снотворный эффект больше выражен у феназепама и диазепама, противосудорожный и миорелаксирующий — у сибазона и феназепама.
- Агонисты серотониновых рецепторов (буспирон).
Связываются с серотониновыми рецепторами, снижая синтез и высвобождение серотонина из клеток. Буспирон обладает выраженным анксиолитическим эффектом, но не оказывает миорелаксирующего, снотворного и противосудорожного действия.
- Средства с другим механизмом действия (амизил).
Несмотря на хорошую переносимость, транквилизаторы назначаются врачом строго по показаниям. Бесконтрольный прием в большинстве случаев приводит к развитию побочных эффектов.
- Развивается психическая и физическая зависимость, поэтому препараты нельзя назначать курсом более 2 месяцев.
- Частое развитие сонливости, шаткой походки, замедленности двигательных реакций. Эти параметры ограничивают прием лекарств у людей, профессия которых требует точных и быстрых реакций (водитель, крановщик и др.).
- Нарушается менструальный цикл, снижается либидо.
- Развиваются парадоксальные реакции возбуждения.
- Появляется снижение памяти, внимания.
Антидепрессанты
 Основная сфера применения антидепрессантов — лечение депрессий. Однако эти препараты применяются и при некоторых других патологических состояниях.
Основная сфера применения антидепрессантов — лечение депрессий. Однако эти препараты применяются и при некоторых других патологических состояниях.Первые лекарственные препараты, которые стали использовать в лечении депрессий, появились в 50-ые годы прошлого столетия. Родоначальником антидепрессантов был ипрониазид, который применялся в лечении туберкулеза и вызывал эйфорию у больных.
В медицинской литературе также используется термин «тимоаналептики».
Основная область применения лекарственных препаратов данной группы — это лечение депрессий, однако, препараты эффективно используются в лечении других патологических состояний:
- Депрессии различной этиологии.
- Маниакально-депрессивный психоз.
- Фобии (страхи).
- Шизофрения.
- При алкоголизме, наркомании, токсикомании.
- Анорексия, булимия.
- Функциональный энурез.
Существует несколько классификаций антидепрессантов. По механизму действия они подразделяются на следующие группы:
- Ингибиторы моноаминооксидазы (МАО).
- Необратимые ингибиторы МАО (пирлиндол, инказан и др.).
- Обратимые ингибиторы МАО (аурорикс, фепросиднин).
- Ингибиторы обратного нейронального захвата медиаторных моноаминов.
- Неизбирательные ингибиторы обратного нейронального захвата нейромедиаторов (инсидон, амитриптилин).
- Избирательные ингибиторы обратного нейронального захвата серотонина, норадареналина (доксепин, флуоксетин).
- Антидепрессанты разных групп (мирзатен, коаксил).
Действие антидепрессантов связывают с влиянием на медиаторы (биологически активные вещества в ЦНС), которые оказывают возбуждающее влияние на работу структур головного мозга. Часть препаратов блокирует высвобождение моноаминооксидазы, другие усиливают выброс норадреналина и адреналина, способствуют накоплению серотонина.
В клинической картине это может проявляться в виде следующих эффектов:
- Седативное действие проявляется в виде успокоения, снижения напряжения, двигательного беспокойства.
- Стимулирующий эффект проявляется активацией психической активности и снижением общей заторможенности.
Стоит отметить, что разные препараты из этой группы обладают разной степенью выраженности основных выше описанных эффектов.
В отличие от транквилизаторов, эффект антидепрессантов проявляется спустя несколько дней или недель от начала приема препаратов.
При приеме наиболее часто встречаются следующие побочные явления:
- Спутанность сознания, тревога, дезориентация в пространстве.
- Нарушение работы сердца (аритмии, внезапная остановка сердца, нарушение проводимости).
- Снижение артериального давления.
- Нарушение внимания, памяти, познавательной деятельности.
- Снижение или набор веса, потеря аппетита.
- Сонливость в дневные часы.
- Тошнота, рвота.
В чем разница?
Стоит отметить, что хотя эти группы относят к психотропным средствам, но показания к назначению у них различные.
Транквилизаторы, в отличие от антидепрессантов, вызывают зависимость, поэтому они назначаются небольшими курсами с перерывами. Антидепрессанты назначают на длительный период времени. Побочные эффекты со стороны антидепрессантов развиваются значительно чаще, чем со стороны транквилизаторов.
Психотропные средства должен назначать специалист в каждом случае индивидуально, учитывая заболевание, сопутствующую патологию, возраст пациента.
Познавательный видеоролик «Как работают антидепрессанты»:
ᐈ Что такое транквилизаторы, антидепрессанты – их отличия, действие ~ Психолог
Активно идет жизнь, развиваются технологии. Мир становится все более динамичным и требовательным к человеку. Ученые уже могут лечить все больше болезней. Однако человек не всегда выдерживает повышенную динамику жизни и просто сходит с дистанции. Возникает усталость, страх или другие неприятные ощущения. Что делать? Употребить нужную таблеточку и опять в строй? Многие, заметив вышеперечисленные симптомы, начинают сами принимать антидепрессанты или транквилизаторы. Так ли это безопасно? А чем отличаются транквилизаторы от антидепрессантов? Зачем нам нужны ноотропы? Попробуем разобраться в этом подробнее.
Что такое транквилизаторы?
Транквилизаторы. Слово «tranquilliser» появилось в медицине в 1957 г. Название пошло от латинского слова tranquillo – успокаивать.
Транквилизаторы – это психотропные лекарственные средства. Основная задача транквилизаторов – снятие тревоги, страха. Это так называемые «малые транквилизаторы», анксиолитики. При необходимости пользуются и «большими» транквилизаторами — это нейролептики. В большинстве стран они вышли из употребления, т.к. не оказывают седативное действие, а наоборот приводят человека в возбуждающее состояние. В отличие от седативных, транквилизаторы имеют более грубое действие. Транквилизаторы применяют не только для лечения депрессии.
Как действуют транквилизаторы на человека?
Транквилизаторы оказывают анксиолитическое, седативное, снотворное, миорелаксантное и противосудорожное действие.
Основной эффект транквилизаторов — противотревожный (анксиолитический). Транквилизаторы способствуют уменьшению беспокойства, тревоги, страха, снижают обсессивность (навязчивые мысли), в частности хорошо работают с ипоходрией (повышенная мнительность по здоровью). Транквилизаторы применяют при различных неврозах и психопатических состояниях, при которых наблюдается тревога, паника, страх, повышенная раздражённость и эмоциональная неустойчивость. Транквилизаторы используют также при психосоматических расстройствах.
Существуют так называемые дневные траквилизаторы – с ними нет сонливости и вялости, однако их действие иное нежели ночных, в составе которых предусмотрен снотворный эффект. Лекарства данной клинической группы не вызывают заторможенности, обладают психостимулирующим действием, усиливают мозговую активность и могут использоваться при выполнении работ, связанных с повышением внимания.
Существуют страхи, что транквилизаторы – это наркотики. Да tranquilliser — это сильнодействующие лекарства, но их боятся не следует, если назначение делает врач и продолжает контролировать изменения вашего здоровья. Сегодня транквилизаторы могут называть анксиолитиками (растворяющий страх и тревогу) или антиневротиками – направленные против невроза. Назначаются обычно в минимальных дозах, короткими курсами с постепенной отменой.
Побочные действия транквилизаторов
У транквилизаторов почти нет побочных действий, в отличие от нейролептиков и антидепрессантов. Для этого нужно строго соблюдать норму и длительность приема. При нарушении рекомендаций у пациента наблюдаются симптомы торможения деятельности нервной системы, может снижаться внимание, появится сонливость и нарушение координации движения, усталость, головокружения и снижается давление. При этом может снизиться зрение, уменьшиться половое влечение, может нарушиться формула крови, ухудшиться деятельность печени, возникнут астения и мышечная слабость.
Транквилизаторы могут и не «сработать». Они практически не оказывают действие при галлюцинациях, бредовых, аффективных и других продуктивных расстройствах, которые сопровождаются страхом и тревогой. Повторюсь, если назначение делает специалист, он обязательно учтет все аспекты вашего состояния.
Негативные последствия от лечения: синдром отмены, возникновение зависимости (психологической или физической) или привыкание. Лечение транквилизаторами должно проводится исключительно под наблюдением врача!
Что такое антидепрессанты?
Антидепрессанты – лекарства, которые имеют психотропное действие. Переводится как «душа, настроение» + «втягивающий». Это название ввели в 1958 году П. Кильхольц и Р. Баттегаи. Чаще всего препараты применяют для лечения депрессии. Они влияют на количество нейромедиаторов, чаще всего серотонина, норадреналина и дофамина. У человека с депрессией, после применения антидепрессантов уменьшается тоска, вялость, апатия, наличие навязчивых мыслей и тревога. Улучшается настроение. Исчезает беспокойство. Становится нормальным сон и появляется аппетит.
Если человек не страдает депрессией, то и антидепрессанты не вызовут улучшение настроения.
В античные времена бессонницу, тревожность и депрессию лечили препаратами зверобоя. И сегодня алкалоиды зверобоя используют в некоторых лечениях депрессии, бессонницы или тревожности. Лишь в тяжелых случаях он уступает стандартным антидепрессантам, таким как плацебо.
Существуют различные классификации антидепрессантов. Антидепрессанты по клиническому эффекту: седатики, сбалансированного действия и стимуляторы.
Антидепрессанты могут применять и при биполярном расстройстве. В клинических условиях антидепрессанты применяют для коррекции панических состояний, неврозов, обсессивно-компульсивных нарушениях, энурезах, хронических болевых синдромах, расстройстве сна. Как дополнительные лекарственные средства при булемии, табакокурении или ранней эякуляции.
Как действуют антидепрессанты?
Антидепрессанты практически не улучшают настроение у здорового пациента. Не рекомендуют применять антидепрессанты и при легкой депрессии. Некоторые ученые утверждают, что от приема антидепрессантов больше вреда, чем пользы. Нужно помнить, что антидепрессанты являются сильнодействующими препаратами. Они требуют индивидуального подбора. Нужно придерживаться дозы и длительности приема. Настойчиво не рекомендую принимать антидепрессанты самостоятельно, без назначения доктора, даже если вы решили возобновить прием после назначенного ранее лечения.
Действие препарата обычно чувствуется не сразу – между началом приема и заметным улучшением состояния должно пройти не менее 2-3 недель, хотя появление хорошего настроения, увидеть свет в конце тоннеля безысходности можно и раньше. Также существуют и «быстрые» антидепрессанты. Их эффект ощутим через 7 дней после начала терапии.
Побочное действе антидепрессантов
Побочные эффекты обычно появляются на начальных этапах лечения и иногда сохраняются до 3-4 недель приема. Ученые многих стран твердят, что антидепрессанты увеличивают возможность суицида. Группа риска – дети и подростки. Прием серотонинергических антидепрессантов может увеличить насилие. Безусловно, в таких случаях речь идет о прекращении проведения терапии под тщательным контролем лечащего врача.
Но следует помнить и о том, что и эти вещества нельзя перестать резко применять. Риск рецидива депрессии в такие случаи повышается на 20-50%. Антидепрессанты стоит отменять последовательно, около четырёх недель. При длительных сроках приема препаратов – еще дольше. Это обусловлено тем, чтобы не появился тот же самый синдром отмены.
Антидепрессанты могут вызывать вялость или сонливость. Снижать концентрацию внимания. Возможно обострение тревоги. Может развиться сексуальная дисфункция. После приема антидепрессантов, люди в возрасте могут страдать гипонатриемией — необходимо контролировать уровень натрия в крови.
Еще раз повторюсь, что назначение или отмена антидепрессантов должна проходить только под присмотром врача. В большинстве случаев антидепрессанты являются безопасными.
Считаете, что вам нужны антидепрессанты? Тогда обратитесь в государственную или частную клинику к соответствующему специалисту.
Что такое ноотропы?
Ноотропы – это препараты, которые оказывают определенное влияние на функции мозговых клеток, их еще можно назвать витаминами для головного мозга. Улучшается умственная деятельность, стимулируется познавательность, улучшается обучение и память — воздействие на когнитивные и мнестические функции организма. Повышается устойчивость мозга к экстремальным нагрузкам, гипоксии или к различным повреждающим факторам и стрессам, так сказать прокачка мозга.
Разработкой ноотропов занимались еще в 1963 году бельгийские ученые. Однако в 1972 году начал действовать термин «ноотропы» — он обозначил класс препаратов, который положительно воздействовал на высшие интегративные функции мозга.
На сегодня выделяют основные действия ноотропных средств: влияние на биоэнергетические и метаболические процессы в нервной клетке. А также взаимодействие с нейромедиаторными системами мозга. Клинические исследование доказали различные дополнительные механизмы, которые вносят вклад в ноотропную активность нейрометаболических стимуляторов.
Как действуют ноотропы?
После применения ноотропов восстанавливаются корковые функции, увеличивается уровень суждений и критических возможностей, улучшается мышление, внимание и речь. Повышается мнемотропное действие. Именно оно влияет на память и обучаемость. После принятия ноотропов, повышается уровень бодрствования. Становится ясное сознание. Повышается устойчивость организма к экстремальным факторам, так называемое адаптогенное действие. Уменьшается слабость, вялость, истощенность, уменьшается психологическая и физическая астения. Ноотропы имеют психостимулирующие действие. Они влияют на апатию, гипобулию, психическую инертность и психомоторную заторможенность. Нооторопы влияют на лечение депрессии. Имеют ноотропы седативное или траквилизирующее действие. Уменьшают раздражительность и эмоциональную возбудимость. Ноотропы воздействуют и на вегетативную систему. Могут корректировать нарушение при парксинсонизме или эпилепсии.
Раньше ноотропы применяли только для лечения пожилых людей. В последнее время широко используют новые технологии и при лечении: болезни Альцгеймера, педиатрии, концентрации внимания, вегетососудистой дистонии, задержке развития, умственной усталости и повышенном уровне стресса, дефиците внимания и многих других областях медицины.
Действие у ноотропов кумулятивное, то есть накапливаемое, как и у антидепрессантов. Ноотропы пьют курсами, от нескольких дней до нескольких недель. Поэтому, нет смысла пить волшебную таблеточку перед экзаменом или сдачей теста на IQ.
Побочные действия ноотропов
Отмечается, что принятие ноотропов не вызывает привыкания или пристрастия. Не сопровождается речевыми или двигательными нарушениями. В некоторых случаях: беспокойство, перевозбуждение, головная боль или нарушение сна. Иногда слабость и сонливость. Описанные побочные эффекты обычно исчезают при снижении дозы препарата, либо при отмене.
Ученые всего мира работают над тем, чтобы человек чувствовал себя комфортно во все более динамичном мире. Нужно все успеть. Держать свои чувства и эмоции под контролем. Все больше получать и обрабатывать информацию. Как вы заметили, что все препараты (транквилизаторы, антидепрессанты и ноотропы) должны помочь вам более комфортно работать и жить. Однако важно понимать и осознавать, что вы не можете быть себе доктором. Увидели определенные синдромы усталости или же истощенности (страхи, отсутствие сна, нарушения пищевого поведения и др.) – обратитесь к врачу.
Не затягивайте и не откладывайте поход к специалисту в долгий ящик. Мы с вами сможем определить степень вашего состояния. Жизнь – это книга, которая изготовлена и написана по вашему заказу. Работа, дети, друзья — подождут. Здоровье важнее.
Будем здоровы!
Нейролептики нового поколения без побочных действий: список, показания к применению
Нейролептик — психотропный препарат, который назначают при психотических, неврологических и психологических расстройствах разной степени тяжести.

Они успешно справляются с приступами шизофрении, олигофрении и при старческом слабоумии за счет действия следующих химических соединений: фенотиазин, бутирофенон и дифенилбутилпиперидин.
Благодаря содержанию этих веществ нейролептики блокируют дофаминовые рецепторы у человека, тем самым успокаивая его и избавляя от тревоги, навязчивых мыслей, панических атак или приступов агрессии.

Что это за препараты?
До того, как были изобретены химически синтезированные лекарства, для лечения психических заболеваний использовали препараты с растительными компонентами — красавку, белену, опиаты, наркотический сон, бромиды или соли лития.
Уже в 1950 году стал активно применяться первый нейролептик — хлорпромазин (аминазин).
Антипсихотики первого поколения появились спустя 8 лет после аминазина — алкалоид резерпин, трифтазин и галоперидол. Они не оказывали должного эффекта, вызывали неврологические расстройства и побочные эффекты (депрессию, апатию и т. д.).
Вплоть до 1967 года нейролептики называли «транквилизаторами» — они также оказывали выраженный седативный эффект, но разница между ними все-таки есть. Главное отличие нейролептиков от транквилизаторов состоит в том, что вторые не могут воздействовать на психотические реакции (галлюцинации, бред), оказывая лишь успокоительный эффект.Нейролептики снимают эмоциональное напряжение, усиливают действие обезболивающих лекарств, оказывают на организм антипсихотическое, когнитотропное и психоседативное действие.

Их назначают для купирования таких симптомов патологии, как:
Механизм действия нейролептиков заключается в подавлении нервных импульсов в тех системах (лимбических, мезокортикальных) головного мозга человека, которые отвечают за выработку дофамина и серотонина.
 Механизм действия нейролептиков
Механизм действия нейролептиковОни имеют короткий период полураспада и хорошо всасываются при любом способе введения, но период воздействия на нервную систему непродолжительный — поэтому назначаются в комплексе, для стимуляция друг друга.
Нейролептики, проникая через ГЭБ между центральной нервной и кровеносной системами, накапливаются в печени, где происходит полный распад препаратов, после чего выводятся через кишечник и мочеполовую систему. Период полувыведения антипсихотиков составляет от 18 до 40 часов, и даже 70 часов в случае с Галоперидолом.
При серьезных заболеваниях назначают нейролептики и пролонгированного действия, которые вводятся внутривенно и оказывают лечебный эффект около 3х недель.
Показания к применению

Все виды нейролептиков направлены на устранение продуктивной, депрессивной и дефицитарной симптоматики при следующих психических заболеваниях:
Препарат вводят при помощи уколов, капельниц или таблеток по желанию пациента. Прием лекарства регулирует врач, начиная с повышенной дозировки, постепенно уменьшая ее. После окончания терапии рекомендуется противорецедивный курс таблеток пролонгированного действия.
Применение нейролептиков имеет и ряд противопоказаний, а именно беременность и грудное вскармливание, возраст до 18 лет, индивидуальная непереносимость компонентов в составе, а также некоторые хронические заболевания.
Классификация
Во второй половине 20 века психотропные средства классифицировали на типичные (старого поколения) и атипичные (нового поколения) нейролептики, которые в свою очередь дифференцируются:
по главному действующему веществу и их производным в их химическом составе:
- тиоксантен (Хлорпротиксен, Зуклопентиксол)
- фенотиазин (Хлопромазин, Перициазин)
- бензодиазепин (Сульпирид, Тиаприд)
- барбитурат (Барбитал, Бутизол)
- индол (Дикарбин, Резерпин)
по клиническому воздействию:
- седативные
- стимулирующие
- инцизивные
Наиболее распространенные препараты среди типичных нейролептиков:
Наиболее распространенные препараты среди атипичных нейролептиков:
- Клопазин
- Оланзапин
- Кветиапин
- Рисперидон
- Зипрасидон
- Амисульприд
Также их можно классифицировать по длительности действия и доступности — одни выдаются строго по рецепту, другие находятся в свободной продаже в любой аптеке города.
Побочные эффекты
Чем больше дозировка и курс терапии антипсихотиками, тем выше вероятность заполучить неприятные последствия для организма.
Побочные действия нейролептиков связаны также с возрастным фактором, состоянием здоровья и взаимодействием с другими препаратами.
Они могут вызвать:
- нарушения работы эндокринной системы (пролактимения, аменорея, нарушение эрекции)
- нарушения работы ЦНС (акатазия, мышечная дистония, паркинсонизм)
- нейролептический синдром (заторможенность действий, невнятная речь, окулогирный криз, при котором происходит запрокидывание головы и закатываются глаза)
- нарушение аппетита, сонливость, потерю веса или увеличение
В 10% случаев проявляются проблемы с ЖКТ, сердечно-сосудистой и мочеполовой системами, а акатизия, вызванная нейролептиками, встречается у 26%. Но главное, чем они опасны для человека, это «синдром отмены», вызванный резким прекращением приема антипсихотиков. Пациент настолько привыкает к ежедневной дозе медикаментов, что не заполучив ее в очередной раз, впадает в состояние депрессии или постоянного дискомфорта. «Синдром отмены» имеет несколько разновидностей и может привести к психозам и поздней дискинезии.
Некоторые пациенты, не дождавшись улучшений после лечения, эффект которого наступает не сразу, пытаются справиться с депрессией при помощи спиртных напитков. Но совмещать нейролептики и алкоголь категорически запрещается, так как при взаимодействии они могут вызвать отравление и даже инсульт.
Нейролептики нового поколения без побочных действий
Благодаря активным разработкам исследователей, список антипсихотиков ежегодно пополняется нейролептиками нового поколения, которые теперь можно дифференцировать согласно длительности и выраженности клинического эффекта, механизму действия и химическому строению.
Современные препараты меньше влияют на мозг, не вызывают привыкания и побочных эффектов, но скорее являются антидепрессантами, устраняющими симптомы, нежели средством лечения.

К ним относятся: Абилифай, Кветиапин, Клозастен, Левомепромазин, Трифтазин, Флуфеназин, Флюанксол.
Преимущества:
- не проявляются нарушения психомоторных реакций
- безопасны для лечения детей
- снижается риск развития патологий
- легкая переносимость
- достаточно одной дозы препарата для достижения положительного результата
- помогают при кожных заболеваниях (недавние исследования показали, что лечение сухости кожи нейролептиками дает положительные результаты у пожилых людей, чьи заболевания связаны с невралгией)

Список препаратов без рецептов
Существует ряд нейролептиков, которые можно приобрести без рецепта.
Они считаются безопасными для пациента, помогают в снятии стресса, мышечных спазмов, при депрессии и психических расстройствах.
Большинство людей находится в заблуждении об опасности нейролептиков, однако фармакология не стоит на месте, и антипсихотики старого поколения уже почти не применяются в медицине.
Современные препараты практически не имеют побочных эффектов, а мозговая деятельность восстанавливается уже через трое суток после выведения препарата из организма.

Многие пациенты задаются вопросом о том, как восстановить мозг после нейролептиков, и ответ на него будет зависеть от степени поражения ими организма. Традиционно врачами назначается сбалансированный витаминно-минеральный комплекс, а также антиоксиданты и иммуномодуляторы для очищения крови.
При интоксикации антипсихотиками, неврастении и для купирования «синдрома отмены» назначают Цитофавин и Мексидол.
Видео
PPT — Нейролептики (основные транквилизаторы или нейролептики) PowerPoint Presentation
Нейролептики (основные транквилизаторы или нейролептики) Эти препараты полезны при лечении психозов, особенно шизофрении, противодействуют или минимизируют влияние на центры галлюцинаций и бреда или не подавляют сознание. (в отличие от седативных и снотворных средств). • не вызывать психологической или физической зависимости • передозировка не смертельна для взрослых.• обладают противорвотным и симпатолитическим действием. Механизм действия Включает антагонизм дофаминовых рецепторов мозга, особенно D2-типа.
Для атипичных агентов, таких как дибензодиазепин (клозапин) и бензизоксазолов, которые имеют меньше ЭПС, они взаимодействуют с дофаминовыми D2-рецепторами и другими рецепторами, например, ацетилхолином, гистамином и серотонином. Побочные эффекты нейролептиков • Их антагонизм можно отнести активность различных рецепторов ЦНС, в том числе: 1-блокада адренергических (a1 / a2) и гистаминовых (h2) рецепторов: гипотензия и седативный эффект 2-антагонизм мускариновых рецепторов ацетилхолина (M1): они вызывают антихолинергические действия на сердечную, офтальмологическую и желудочно-кишечную системы. , мочевой пузырь и ткань половых органов.
3- Антагонизм рецепторов D2 в нигростриатном пути: EPS. 4-Антагонизм D2-рецепторов в триггерной зоне хеморецепторов в стволе головного мозга отвечает за их противорвотные эффекты, например промазин 5- Метаболические и эндокринные побочные эффекты: увеличение веса, гиперпролактинемия и гинекомастия. 6- Усиливать действие депрессантов ЦНС. 7- Другие побочные реакции — желтуха, агранулоцитоз и судороги.
N.B. Антихолинергическое действие атипичного клозапина может быть полезным при отрицательных симптомах шизофрении.Структурные требования для всех нейролептических препаратов 1. Прямая цепь из трех атомов углерода, соединяющая азот основного кольца с атомом углерода, азота или кислорода. Этот атом может быть частью бензоильной группы, фенотиазина или тиоксантена (трициклическая система). 2. Шестичленное основное гетероциклическое кольцо, такое как пиперазин или пиперидин, замещенное в положениях 1 и 4; лучшими заместителями в положении 4 являются фенильный, анилино-, метильный или гидроксиэтильный фрагменты. Y = C, N, O
Таким образом, все нейролептики действуют на молекулярном уровне посредством блокады рецепторов D2, поскольку они обладают этими двумя характеристиками.• В комплексообразовании с дофаминовыми рецепторами может быть задействована «S-образная» конформация четырехатомной последовательности, которая связывает ароматическое кольцо с 3-м основным азотом в большинстве нейролептиков. (a) (b) (c) «S-образная» конформация пиперидилидентиоксантена (a) и дифенилбутиламинов (b) имеет такое же расстояние d, что и молекула дофамина (c) в ее расширенной конформации.
Классификация антипсихотических средств I. Производные фенотиазина и тиоксантена.II — Производные бутирофенона и дифенилбутилпиперидина. III — Производные бензамида. IV — Производные бензазепина. V — Производные индола. VI- Бензизоксазолы. VII- Антиманиакальные средства. I-Производные фенотиазина и тиоксантена A) Производные фенотиазина Они характеризуются липофильной конденсированной трициклической системой, связанной через атом азота центрального кольца через промежуточную цепь с гидрофильным 3-м основным амином.
Взаимодействие фенотиазинов и тиоксантенов с дофаминергическими рецепторами Фенотиазины взаимодействуют с дофаминовыми рецепторами в трех участках A, B и C, вызывая ответ.Порядок структурной специфичности в этих сайтах: B> C> A. Сайт B (промежуточная цепь) • Алкильная цепь должна содержать 3 атома углерода (н-пропильная цепь), которые являются оптимальными для активности. 2. Если два атома углерода, он дает фенотиазины с антихолинергической (этопропазин) или антигистаминной (прометазин) активностью без антипсихотических средств, так как их промежуточная изопропильная цепь не может принимать предпочтительную конформацию. Предполагаемая конформация в контакте с нейролептическими рецепторами X = Me прометазин X = Et этопропазин (противопаркинсонический препарат)
Группа R, расположенная на β-углероде, важна для структурной специфичности (необходима определенная степень свободного вращения) из-за ему вызывает стерические эффекты.а) Если R = H, проявляется хорошая нейролептическая активность. б) Если R = Ch4, он усиливает антигистаминный эффект и снижает нейролептическую активность. c) Если R = объемная группа (фенил или часть кольца), это снижает нейролептическую активность. Сайт A (гидрофильный 3-й основной амин) 1 — Сайт A отвечает за структурную специфичность, поскольку молекула должна входить в узкую щель. Таким образом, если два атома водорода, присоединенные к азоту, заменяются: а) метильными группами, активность не снижается.б) За счет объемных алкилов снижает активность (усиление стерического эффекта). 2- Замена концевой диметиламиногруппы пиперазиновой или N-метилпиперазиновой группой увеличивает активность.
3-Четвертичный атом азота в боковой цепи снижает растворимость липида и его проникновение в ЦНС и потерю активности. Сайт C (липофильное ядро фенотиазина): 1- Два плоских ароматических кольца расположены под прямым углом из-за сворачивания ядра фенотиазина. Таким образом, заместитель R-2 находится слишком далеко от рецептора и не оказывает никакого стерического влияния.2- Замена кольца H в положении 2 приводит только к увеличению активности; в противном случае снижает потенцию. 3- Наличие притягивающего электроны, но не ионизируемого gp в 2-позиционном увеличении потенции, например Cl (хлоропромазин) и CF3 (трифторпромазин). 4-Производные с 2-тиоалкилом сохраняют активность, в то время как производные 2-ОН слабо активны.
а) пропиламины 5- В предпочтительной конформации хлорпромазина его боковая цепь наклоняется к 2-хлорзамещенному кольцу из-за притяжения боковой цепи амина (протонированной при физиологическом pH) к кольцу, содержащему атом хлора.• Электроотрицательный атом хлора отвечает за придание асимметрии хлорпромазину. • Фенотиазины и родственные соединения, не содержащие хлора во 2-м положении, неактивны как нейролептики. Классификация фенотиазинов По углеводородной боковой цепи они классифицируются на: • пропиламины b) пиперидины c) пиперазины Промазин (спарин) хлоропромазин 2-Хлор-10- [3- (диметиламино) пропил] фенотиазин гидрохлорид
а) Пропиламины Хлорпромазин гидрохлорид (ларгактил).• Это прототип и используется для лечения шизофрении, контроля острых психозов и острой мании. • Он также используется как противорвотное средство при послеоперационной тошноте и рвоте. Анализ: неводное титрование 0,1 М хлорной кислотой. Синтез: б) Пиперидины Тиоридазин HCl (Меллерил). Обладает относительно низким EPS, низкой противорвотной активностью, но более высоким антихолинергическим действием.
Это 10- [2- (1-метил-2-пиперидил) этил] 2- (метилтио) фенотиазин в) пиперазин Трифтороперазин HCl (стелазин).• Это 2-трифторметил-10- [3- (4-мети-1-пиперазинил) пропил] фенотиазин. • Это сильнодействующий антипсихотик с высоким EPS и низким седативным и гипотензивным эффектами. Деканоат флуфеназина (длительного действия) • Продолжительность действия флуфеназина со свободным фрагментом ОН может быть увеличена путем приготовления сложных эфиров длинноцепочечных жирных кислот. • Один в / м каждые 2-3 недели с эфиром, чтобы избежать режима приема лекарств и нарушения всасывания. Тиоридазин HCl Трифлуоперазин HCl
B) Производные тиоксантена (модифицированные фенотиазины) • Изостерическое замещение атома N фенотиазина на углерод sp2 (метилиден) привело к тиоксантенам.• Тиоксантены также неполярны, в которых заместитель в положении 2 приводит к образованию цис (Z) или транс (E) изомеров. • Z-изомер более активен, чем транс-изомер или его насыщенный аналог, поскольку он накладывается на рецепторы дофамина. • Их фармакологическое действие и побочные эффекты очень похожи на производные фенотиазина. Хлорпротиксен (тарактан) • Это биологический изостер хлорпромазина. • Используется при лечении шизофрении. • Он также обладает антигистаминными, противорвотными и гипотензивными свойствами.Z-2-Хлор-9- (3-диметиламинопропилидин) тиоксантен
Метаболизм фенотиазина и тиоксантенов • 7-гидроксилированные фенотиазины, а также моно- и ди-десметилированные продукты являются активными Рецепторы D2, тогда как сульфоксид неактивен. • Большинство тиоксантенов не образуют производных с гидроксилированным кольцом. Таким образом, можно сделать вывод, что во всех трициклических соединениях структурными особенностями, связанными с высокой антипсихотической активностью, являются: • Трициклическое кольцо с шести- или семичленным центральным кольцом.• Боковая цепь из 3 атомов между центральным кольцом и концевой группой Nh3. • Группа, притягивающая электроны, такая как хлор или трифторметил, в положении 2 трициклического кольца.
II- Производные бутирофенона и дифенилбутилпиперидина a) Производные бутирофенона • В 1950 году Янссен в испытаниях приготовил пропиофенон и бутирофеноновые аналоги меперидина для повышения обезболивающего действия меперидина. • Аналог пропиофенона обладал в 200 раз анальгетической активностью по сравнению с меперидином, но аналог бутирофенона проявляет активность, напоминающую активность хлорпромазина, но менее токсичен.Аналог бутирофенона Меперидин Аналог пропиофенона
X = F или OCh4 Взаимосвязи между структурой и активностью Все бутирофеноны имеют следующую общую структуру: конформация галоперидола 7,3 Å. 2) Присоединение 3-й аминогруппы к 4-му атому углерода бутирофенонового скелета необходимо для активности. 3) Удлинение, укорачивание или разветвление снижает активность.4) Замена кето-фрагмента на тиокетон или уменьшение группы C = O снижает нейролептическую активность. 5) 3-й основной азот обычно включен в шестичленное кольцо (пиперидин или пиперазин), которое замещено в пара-положении.
Галоперидол (галдол) • Он связывается с высоким сродством с дофаминовыми D2 и серотониновыми 5-HT2 рецепторами в головном мозге. • Используется при лечении шизофрении и острых психозов. • Это вызывает высокую частоту экстрапирамидных реакций.Анализ: неводное титрование 0,05 М хлорной кислотой. • Галоперидол деканоат — травма длительного действия. (4-6 недель). Дроперидол • 1- {1- [3- (п-фторбензоил) пропил] — 1,2,3,6-тетрагидро-4-пиридил} — 2-бензимидазолинон. 4- [4- (п-Хлорфенил) -4-гидрокси) пиперидино] -4-фторбутирофенон
Это препарат короткого действия и используется в анестезии для седативного и противорвотного действия в комбинации (Innovar) с фентанилом ( наркотический анальгетик). б) Дифенилбутилпиперидиновые нейролептики • Модификация или частичное дублирование галоперидола путем введения 4-фторфенильного фрагмента привело к производным длительного действия, таким как пимозид и пенфлуридол (из-за их высокой гидрофобности).• Их принимают внутрь один раз в неделю при хронической шизофрении. III-Производные бензамида • О-метоксипрокаинамид — это соединение с местными анестезирующими свойствами и сильным противорвотным действием. • Дальнейшая модификация молекулы дала метоклопрамид. пимозид
1-Метоклопрамид (Примперан, Пласил) • Обладает противорвотным действием (изменяет перистальтику желудка). • Было обнаружено, что он противодействует дофаминовым D2-рецепторам в триггерной зоне хеморецепторов ствола головного мозга.2- Пирролидинилсодержащие бензамиды а) Сульпирид (Догматил) • Сульпирид оказывает слабое седативное действие и не имеет ЭПС, что объясняется преимущественным действием на лимбическую ткань по сравнению со стриарной тканью (экстрапирамидная). • Его гидрофильные свойства вызывают плохое всасывание во рту, ограниченное проникновение в ЦНС и, как следствие, низкую эффективность.
б) Ремоксиприд • Он хорошо всасывается при пероральном приеме и имеет почти такую же эффективность, как галоперидол, но с меньшим количеством экстрапирамидных и вегетативных побочных эффектов.• Он вызывает апластическую анемию, что может ограничивать его использование в качестве антипсихотического препарата. Метоклопрамид S — (-) — Сульпирид S — (-) — Ремоксиприд
IV- Производные бензазепина. • Клозапин (Клозарил) Это дибензазепиновый антипсихотик с минимальной ЭПС и облегчает негативные симптомы шизофрении. • Его серьезный недостаток — фатальный агранулоцитоз. • Он имеет низкое сродство к дофаминовым рецепторам D1 и D2 по сравнению с его сродством к адренергическому a1; и рецепторы a2, h2, мускаринового M1 и серотонина 5-HT2A, таким образом, его специальное использование может быть связано с взаимодействием с другими рецепторами.2) Локсапин (локситан) • 2-хлор-11- (4-метил-1-пиперазинил) дибенз [b, f] [1,4] оксазепин. • Это типичный нейролептик, обладающий в основном антидопаминергической активностью в отношении D2-рецепторов. Локспин (R = Ch4) Амоксапин (R = H)
3) Амоксапин (Азендин) • Локсапин подвергается N-деметилированию с образованием амоксапина, который клинически используется в качестве антидепрессанта • Он связывается с рецепторами D2 и ингибирует нейротранспин для блокирования обратного захвата норэпинефрина, коррелятора антидепрессивной активности.V-Производные и изостеры индола • Их антипсихотическая активность основана на том, что серотонин (5-гидрокситриптамин) участвует в развитии шизофрении; поэтому некоторые аналоги индоламина могут быть полезными нейролептическими агентами • По химической структуре некоторые нейролептики (дроперидол и пимозид) представляют собой индол или его изостер
Молиндон (Мобан): 3-этил-6,7-дигидро-2-метил -5- (морфолинометил) индол-4 (5H) он • Это производное тетрагидроиндолона, которое используется при острой и хронической шизофрении.• Он менее эффективен, чем галоперидол в блокировании рецепторов D2, однако может продуцировать ЭПС. • Он быстро всасывается и метаболизируется при пероральном приеме (длится более 24 часов). Сертиндол (Сердолект). • Это индол, который действует как антагонист серотониновых рецепторов 5-HT2 без сродства к дофаминергическим рецепторам D2.
Преимущества: • Он так же эффективен, как галоперидол, при лечении острой и хронической шизофрении, • значительно снижает частоту возникновения ЭПС. • Не успокаивает и длится долго (несколько дней).VI-Бензизоксазолы • Предположение, что комбинация антагонистов D2 / 5-HT2 может вызывать атипичный антипсихотический эффект. Рисперидон Это антагонист 5-HT2 / D2. 3- (4-пиперидинил) -1,2-бензизоксазол
Предполагается, что антисеротонинергические эффекты рисперидона не ингибируют дофаминергическую нейротрансмиссию в полосатом теле и коре головного мозга, уменьшая тяжесть ЭПС, вызванной антагонистом D2, и облегчение негативных симптомов шизофрении при сохранении блокады рецепторов D2 лимбической системы.Хорошо всасывается при приеме внутрь. VII- Антиманиакальные средства • Соли лития используются как антиманиакальные средства. • Хлорид лития не используется, поскольку он гигроскопичен и более раздражает ЖКТ, чем соли карбоната или цитрата.
Спасибо
границ | Гипофункциональное поглощение дофамина и шизофрения, устойчивая к лечению антипсихотиками
Введение
Шизофрения — это психическое заболевание, часто включающее сложную генетическую предрасположенность (1–3), а также уязвимость к определенным факторам окружающей среды (4), что в конечном итоге приводит к появлению симптомов, клинически определяемых как положительные. (возникающие симптомы, включая галлюцинации и бред) или отрицательные (характеризующиеся потерей определенной функции, включая апатию и отсутствие мотивации) (5–7).Кроме того, часть пациентов с шизофренией имеет нарушения при выполнении стандартных нейрокогнитивных задач (8), и это считается важным коррелятом тяжести заболевания (9–12). Основные нейробиологические нарушения, лежащие в основе симптомов шизофрении, до конца не изучены. Несмотря на это, считается, что субхроническая блокада части (60–80%) рецепторов допамина D 2/3 (которые мы будем обозначать как «D 2 ») лежит в основе эффективности лечения шизофрении (13).Предыдущая и недавняя литература поддерживает эффективность антагонизма D 2 по сравнению с любым альтернативным фармакологическим вмешательством (14-17). Однако блокирование дофаминовых рецепторов не является эффективным терапевтическим механизмом для всех людей с шизофренией (18–24). Например, некоторые пациенты с первым эпизодом психоза не отвечают на лечение антипсихотиками (25). Отсутствие ответа на лечение антипсихотиками также может быть «приобретенным» и может развиваться с течением времени при длительных схемах лечения (23, 26) или может развиваться после периода воздержания от лечения, например, при несоблюдении режима приема лекарств (27–30). ).Во многих из этих случаев пациенты, не отвечающие на лечение антипсихотиками первой линии, вместо этого реагируют на клозапин (18, 31, 32). Кроме того, существует дополнительная группа пациентов с шизофренией, которые не реагируют на клозапин или другие антипсихотические препараты. Эта категория пациентов определяется как «сверхрезистентные» (18, 33).
Неясно, все ли случаи резистентности к антипсихотикам имеют общий нейробиологический механизм (10, 24, 34–39), и нет точной поведенческой сигнатуры, указывающей на его клиническое проявление, поскольку критерии для определения устойчивости к лечению антипсихотиками были стандартизированы только недавно. (40).В задачи этого обзора не входит внесение вклада в поведенческое определение устойчивости к лечению при шизофрении. Скорее, фокус здесь сужается к предполагаемой роли клиренса дофамина в проявлении первичной резистентной к антипсихотикам шизофрении (т.е. пациентов с первым эпизодом психоза, которые никогда не реагировали на лечение). Мы не исключаем возможности того, что изменения в других системах нейротрансмиттеров также могут быть задействованы, а также не исключаем, что описанные здесь дофаминергические механизмы также применимы к другим формам устойчивости к антипсихотикам.Просто мы сосредотачиваемся на дофамине, потому что клинические наблюдения подчеркивают важность этого нейромедиатора в патофизиологии психоза (41–43) и его лечении (44). Наше внимание к клиренсу дофамина мотивировано недавними данными исследований ex vivo, и in vivo, с моделями животных, демонстрирующих, что антипсихотическая недостаточность сопровождается толерантностью к вызванному антипсихотиками увеличению базального дофамина и обмена дофамина и что переносчик дофамина ( DAT) является ключевым модератором внеклеточного дофамина и антипсихотического ответа (35, 38, 45).Связь между сохраненным или слегка повышенным дофаминергическим тонусом и антипсихотической реакцией также наблюдалась у людей с шизофренией (46). Недавняя интерпретация этих данных предполагает, что сохраненный внеклеточный дофаминергический тонус может играть важную фармакологическую роль в терапевтической эффективности антипсихотических средств (24). Эти наблюдения прямо или косвенно подтверждаются независимыми исследованиями (38, 47–50). Из-за ограниченного объема мы лишь кратко опишем дофаминергические биомаркеры, описанные в литературе, которые имеют отношение к пониманию антипсихотической реакции.В заключение мы предположим, что DAT может быть более мощным модератором антипсихотической эффективности и неэффективности, чем это считается в настоящее время. Изменения в экспрессии и / или функции DAT сами по себе могут изменить ожидаемую реакцию на антипсихотические препараты, что делает DAT очень важным белком с учетом дофаминергической природы устойчивой к антипсихотикам шизофрении.
Дофаминергическая дисрегуляция при шизофрении
Прежде чем обсуждать дофаминергические механизмы антипсихотической эффективности, важно описать дофаминергические нарушения передачи сигналов при шизофрении, на которые нацелены антипсихотические препараты.Как описано во введении, этиология и невропатология симптомов шизофрении до сих пор не ясны. Генетические исследования указывают на ассоциации с генами, регулирующими развитие нервной системы, иммунную систему, дофаминергическую и глутаматергическую передачу (2, 51), в то время как другие исследования демонстрируют потенциальную роль в нарушении множественных внутриклеточных сигнальных путей при шизофрении (52). Более того, факторы окружающей среды, связанные с шизофренией, такие как миграция или акушерская инфекция, могут изменять нейротрансмиссию дофамина (4) в дополнение к другим нейробиологическим системам (53–58).Несмотря на множество факторов, которые, по-видимому, способствуют развитию шизофрении, лечение было сосредоточено на коррекции дисрегуляции дофаминергической системы путем ингибирования дофаминергической передачи. Однако следует отметить, что эффективность фармакологического воздействия на дофаминергическую систему при шизофрении не является окончательным доказательством дофаминергической дисрегуляции. Дофамин играет мощную нейромодулирующую роль в головном мозге и, в частности, в базальных ганглиях, и он может регулировать двигательную активность, а также мотивацию и познание.Поскольку все эти функции нарушены при шизофрении, неудивительно, что многие антидофаминергические препараты эффективны (или вредны) для симптомов шизофрении, даже если наблюдаемые симптомы могут иметь какую-то другую первопричину (-ы). Таким образом, дофаминергическую систему следует рассматривать как путь лечения, способный влиять на поведенческие особенности, которые, по-видимому, нарушаются при шизофрении, но могут быть вызваны изменениями в других системах нейротрансмиттеров.
Механизмы антипсихотической реакции
Блокада дофаминовых рецепторов головного мозга рассматривается как механизм терапевтической эффективности антипсихотических препаратов уже более 60 лет (9, 59).Таким образом, очень часто исследователи сосредотачиваются на взаимодействиях между молекулой (ами) и рецептором (ами) для описания антипсихотических механизмов. Хотя такой подход в принципе правильный, на практике он может быть слишком упрощенным. Рецепторы не действуют изолированно. Рецепторы на нейронах связаны через синапсы и организованы в сети внутри нейронных цепей. Рецепторы также функционально связаны с внутриклеточными молекулярными сетями, которые контролируют возбудимость мембран, а также синтез, высвобождение и метаболизм нейромедиаторов, и с помощью этих механизмов нейроны могут регулировать свою собственную активность.Из-за природы нейронной передачи сигналов изменения в инактивации или активации нервных рецепторов с помощью антипсихотических препаратов или любого другого соединения, которые вызывают локальные внутриклеточные изменения, будут влиять на другие клеточные популяции через распространение сигнала по нервным путям. Таким образом, антипсихотические препараты могут влиять на синтез, высвобождение и метаболизм нейротрансмиттеров не только в нейронах, которые напрямую взаимодействуют с антипсихотиками, но и в тех нейронах, которые являются частью одной и той же нервной цепи.Следовательно, правильное понимание механизмов, лежащих в основе антипсихотической реакции, не должно просто описывать химические взаимодействия между нейролептическими препаратами и их рецепторами-мишенями, но должно учитывать модификации, индуцированные антипсихотиками на клеточном и круговом уровнях. Мы сосредоточимся на нейроадаптации, происходящей на клеточном уровне, которая связывает рецепторы с синтезом, высвобождением и поглощением внеклеточного дофамина.
Striatal D 2 Блокада рецепторов при лечении шизофрении
Striatal D 2 Блокада рецепторов считается наиболее эффективным механизмом для уменьшения психотических симптомов при шизофрении (60, 61).Экстрастриарные механизмы действия нейролептиков обсуждались ранее (62) и не будут здесь обсуждаться. Общая теория терапевтической эффективности антипсихотических средств основана на двух основных наблюдениях. Во-первых, клиническая эффективность антипсихотических средств, включая клозапин, напрямую связана с их сродством к дофаминовому рецептору D 2 in vitro (14, 15). Это подтверждается данными о том, что терапевтические концентрации нейролептиков в плазме или в спинномозговой жидкости точно соответствуют константе диссоциации антипсихотических средств (K d ) на рецепторах D 2 (63).Во-вторых, терапевтические концентрации всех антипсихотиков (типичных и атипичных) вызывают аналогичную занятость рецептора D 2 (13, 59, 64). Хотя это наблюдение не относится строго к клозапину (21) или кветиапину (65), было показано, что занятость рецептора D 2 в головном мозге человека колеблется от 70% до 80% в течение 2 часов после лечения и остается повышенной более 24 часа как для типичных, так и для атипичных нейролептиков (21, 66, 67). С другой стороны, занятость рецептора D 2 клозапином (20) и кветиапином (68, 69) значительно снижается в течение 24 часов.Основываясь на этих выводах, Seeman и Tallerico (63) предположили, что основное различие между типичными и атипичными нейролептиками заключается во временном ослаблении связывания нейролептиков с рецептором D 2 при воздействии эндогенного дофамина. Фактически, нейролептики конкурируют с эндогенным дофамином в синаптическом пространстве, и присутствие дофамина теоретически может повлиять на концентрацию антипсихотика, необходимую для достижения определенного диапазона занятости рецептора D 2 .Впоследствии было обнаружено, что константа скорости диссоциации, k от (а не константа скорости ассоциации, k от ), в значительной степени объясняет разницу в аффинности связывания при сравнении типичных и атипичных антипсихотиков (70). Это также означает, что на измерения занятости рецептора D 2 нейролептиками может влиять химический состав используемых радиолигандов (например, жирорастворимый спиперон, немонаприд по сравнению с водорастворимым дофамином, раклопридом) (71–73).D 2 Занятие рецептора атипичными антипсихотиками, такими как клозапин и кветиапин, будет снижаться на ( 11 C) раклоприда в меньшей степени, чем при использовании липидорастворимых радиолигандов, таких как ( 11 C) метилспиперон (63, 73, 74 ). Следовательно, различия в занятости рецептора D 2 между клозапином, кветиапином и другими антипсихотическими средствами могут зависеть от химии используемых радиолигандов (75). Эта интригующая интерпретация, разработанная с использованием анализов in vitro и , не получила функционального подтверждения.Типичные и атипичные нейролептики диссоциируют со сходной временной кинетикой при электрофизиологических оценках, предполагая, что изменение антагонизма рецептора D 2 типичными и атипичными антипсихотиками существенно не отличается (76, 77). Эти противоречивые результаты указывают на возможность того, что механизмы, отличные от занятости рецептора, также могут быть задействованы в результатах этих анализов, хотя мы не можем отрицать значимость кинетики связывания лиганда на рецепторах D 2 для достижения антипсихотической эффективности (24, 38).
Striatal D 2 Плотность рецепторов и блокада при резистентной к лечению шизофрении
Как уже упоминалось выше, блокада (или захват) части рецепторов D 2 не является действенным антипсихотическим механизмом для значительного числа пациентов с шизофренией (31). Фактически, примерно одна треть людей с шизофренией устойчивы к лечению антипсихотиками первой линии, несмотря на достаточную занятость рецептора D 2 (19).Клозапин, который действует при относительно низкой (~ 40%) занятости рецепторов полосатого тела D 2 (20, 21, 78, 79), является наиболее эффективным антипсихотическим средством у большинства пациентов, невосприимчивых к другим антипсихотическим препаратам (18, 32, 80). Если мы гипотетически примем предположение, что этот результат не связан с кинетикой связывания рецептора D 2 (77), мы начнем рассматривать другой дофаминергический механизм, который может объяснить это очевидное несоответствие. Все больше литературы поддерживает идею о том, что дополнительные дофаминергические механизмы могут лежать в основе терапевтической эффективности антипсихотических препаратов (24, 38).Некоторые пациенты, которые отвечают на лечение антипсихотиками первой линии, со временем испытывают снижение эффективности лечения (23), что может привести к несоблюдению режима лечения и рецидивам (81). Снижение антипсихотической эффективности также может происходить, несмотря на стабильную занятость рецептора D 2 (82). Эта динамика изображена на Рисунке 1. Противоположная ситуация также наблюдалась с длительной антипсихотической эффективностью, несмотря на снижение занятости рецептора D 2 (89–85).
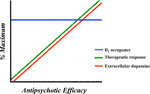
Рисунок 1 Представление нейрохимических факторов, влияющих на антипсихотический ответ у людей и животных моделей.Антипсихотический ответ оптимален в сочетании с повышенным уровнем внеклеточного дофамина. Занятие рецептора D 2 менее динамично и кажется стабильным в периоды времени, характеризующиеся как терапевтической эффективностью, так и неэффективностью антипсихотических препаратов.
Приобретенная устойчивость к нейролептикам (толерантность) может включать индуцированную антипсихотиками сверхчувствительность дофаминовых рецепторов, потенциально возникающую в результате активации рецептора D 2 , как следствие хронической блокады рецептора D 2 (34, 86, 87).Считается, что у пациентов с шизофренией сверхчувствительность к допамину, вызванная антипсихотиками, снижает эффективность лечения, способствует рецидиву психоза, а также ухудшает психотические симптомы (88–90). У лабораторных животных индуцированная антипсихотиками сверхчувствительность к дофамину вызывает потерю антипсихотической эффективности (35, 91, 92) и чрезмерную поведенческую реакцию на агонисты дофамина (35, 93–95). Однако связь с индуцированной антипсихотиками повышающей регуляцией D 2 в полосатом теле является сложной. Изменения уровней экспрессии дофаминовых рецепторов у пациентов не были достоверно воспроизведены независимыми исследовательскими группами (96, 97).Недавние исследования с использованием животных моделей также показывают толерантность к нейролептикам, несмотря на клинически репрезентативные уровни блокады полосатого тела D 2 рецептора, измеренные либо с помощью визуализации in vivo (38) или ex vivo рецептора авторадиографии (35, 91). Вызванная антипсихотиками сверхчувствительность дофамина и толерантность к антипсихотикам также могут быть отделены от изменений в плотности рецепторов полосатого тела D 2 (35). Таким образом, изменения в экспрессии стриарного рецептора D 2 не всегда могут служить предиктором изменений антипсихотической эффективности или появления антипсихотической сверхчувствительности к допамину (24, 35, 38, 98, 99), хотя высокие дозы антипсихотических средств могут активировать стриатальную активность. D 2 рецепторов (100).
Помимо изменений плотности рецепторов D 2 в полосатом теле, хроническое лечение антипсихотиками может также увеличивать функцию рецепторов D 2 , и это было связано со сверхчувствительностью к дофамину и приобретенной толерантностью к антипсихотикам. Когда рецепторы D 2 связаны с белками G i / o , они находятся в функциональном состоянии с высоким сродством к дофамину (обозначается как D 2 HIGH ). Когда рецепторы D 2 не связаны с белками G i / o , они находятся в функционально инертном состоянии с низким сродством к дофамину (D 2 LOW ).Таким образом, пропорция D 2 HIGH может модулировать передачу сигналов дофамина через рецепторы D 2 . Связь между толерантностью к антипсихотикам и изменениями в полосатом теле D 2 HIGH в значительной степени проистекает из работы на животных моделях, показывающей, что хроническое лечение антипсихотиками увеличивает уровни полосатого тела D 2 HIGH (35, 91, 101). Схемы лечения антипсихотиками, которые способствуют поведенческой сверхчувствительности к допамину и толерантности к лечению антипсихотиками, приводят к еще большему увеличению количества участков D 2 HIGH (91).D 2 ВЫСОКОЕ повышение уровня рецепторов и индуцированная антипсихотиками сверхчувствительность дофамина также имеют сходный временной ход (35). Однако количество сайтов D 2 HIGH может увеличиваться на ранних этапах лечения антипсихотиками, до появления каких-либо поведенческих свидетельств сверхчувствительности к допамину или толерантности к лечению (35). Кроме того, режимы дозирования антипсихотических препаратов, которые не вызывают сверхчувствительности к дофамину, могут по-прежнему увеличивать количество участков полосатого тела D 2 HIGH (91, 101).Кроме того, нет убедительных доказательств повышения D 2 HIGH рецепторов у пациентов с шизофренией [см. (102)]. Таким образом, вероятно существует связь между изменениями в сайтах D 2 HIGH и приобретенной толерантностью к лечению антипсихотиками, но это требует дальнейшего изучения.
Дофамин D 2 Изоформы рецепторов и шизофрения
Большинство клеток, экспрессирующих рецепторы D 2 в полосатом теле, представляют собой нейроны с клеточными телами среднего размера и шиповидными дендритами (средние шиповатые нейроны, MSN, около 95% всех клетки в этой области), которые являются постсинаптическими по отношению к дофаминергическим терминалам, выходящим из среднего мозга, среди других регионов; для обзора см. ссылки.(24, 103). Стриатум также содержит пресинаптические рецепторы D 2 , экспрессируемые на дофаминергических окончаниях аксона, которые составляют лишь небольшой процент от общего пула рецепторов D 2 , обнаруженных в полосатом теле, и могут иметь различную молекулярную структуру (104). Соответственно, существуют две изоформы рецепторов дофамина D 2 , полученные в результате альтернативного сплайсинга экзона 6 с образованием длинной (D 2L ) и короткой (D 2S ) форм белка (105–107) (рис. 2A – C).Обе изоформы, по-видимому, регулируют дофаминергическое возбуждение (108), но только D 2S контролирует аутоингибирование, опосредованное Ca 2+ (109, 110). Кроме того, постсинаптический D 2S , но не D 2L , контролирует возбудимость MSN у грызунов (111) и, вероятно, у людей (112), несмотря на его преобладающую пресинаптическую локализацию. Эти эффекты, вероятно, являются следствием различных молекулярных механизмов, связанных с изоформами рецептора D 2 (113–116) (рис. 2C).
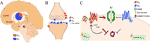
Рисунок 2 (A) Неравномерная экспрессия изоформ рецептора дофамина D 2 изоформ (короткая, D 2S и длинная, D 2L ) в среднем мозге человека (черная субстанция, SN) и полосатом теле ( хвостатое ядро и скорлупа).D 2L преобладает в полосатом теле, тогда как D 2S преимущественно экспрессируется в среднем мозге. Это несбалансированное соотношение D 2L / D 2S наблюдается у разных видов. (B) Схема синаптического контакта между дофаминергическим концом, выступающим из SN, и соматодендритным шипом в полосатом теле показывает несбалансированное соотношение D 2L / D 2S на нейронах среднего мозга и полосатого тела. (C) Отчетливые физиологические эффекты опосредуются двумя изоформами рецептора D 2 .Оба рецептора D 2S и D 2L ингибируют аденилатциклазу, хотя опосредованное D 2L ингибирование слабее, через G i α 1 и G i α 2 соответственно. Стимуляция D 2S приводит к фосфорилированию тирозингидроксилазы (TH) по серину 40 в нигростриатных дофаминергических нейронах, тогда как стимуляция D 2L приводит к фосфорилированию дофамина и цАМФ-регулируемого фосфопротеина 32 кДа (DARPP-32, треон-34) по треону-34. в средних шиповатых нейронах.D 2S , но не D 2L , активирует контролируемую G-белком внутренне выпрямляющую калиевую проводимость (GIRK), которая является чувствительной к Ca 2+ . D 2S , но не D 2L , подавляет возбуждение в ответ на токи глутамата (Glu).
Экспрессия изоформ D 2 в головном мозге млекопитающих распределена неравномерно (рис. 2А). Геномные исследования мРНК D 2 человека и грызунов, которые имеют примерно 95-99% гомологии (117), показывают, что, хотя мРНК D 2L и D 2S широко экспрессируются в головном мозге, мРНК D 2L является сильно выражен в полосатом теле (I.е., хвостатое ядро и скорлупа) относительно мРНК D 2S (117–120). Исследование экспрессии белка D 2 у приматов показывает, что D 2L высоко экспрессируется в полосатом теле и обнаруживается, в частности, на MSN и холинергических интернейронах, тогда как D 2S вместо этого экспрессируется на дофаминергических аксонах (121). В коре и среднем мозге D 2L в основном экспрессируется на соматах нейронов, тогда как D 2S обнаруживается на соматах, дендритах и окончаниях аксонов (121).Интересно, что высокоэффективные нейролептики (с высоким сродством к рецептору D 2 ), по-видимому, избирательно связывают те рецепторы, экспрессируемые в полосатом теле (структура с высоким соотношением D 2L / D 2S ) (122, 123), что подтверждает представление о том, что антипсихотические препараты могут связывать обе изоформы D 2 , но что эффективные дозы антипсихотиков будут связывать в основном D 2L и лишь небольшую часть всех рецепторов D 2S в головном мозге. Хотя эта возможность не полностью подтверждается исследованиями связывания с использованием клонированных рецепторов D 2 в культивируемых клетках (124–127), исследованиями насыщения связывания и исследованиями in vivo антипсихотиков ED50 с использованием трансгенных мышей (т.е.e., D 2L (мыши с нокаутом рецептора )), по-видимому, подтверждают антипсихотическую селективность в отношении D 2L (128–131). В соответствии с этими наблюдениями, исследования на людях показали, что более эффективные антипсихотические препараты имеют более высокую занятость рецептора D 2 в полосатом теле, чем в среднем мозге (SN). (132, 133).
Патологоанатомические исследования с использованием ткани головного мозга пациентов с шизофренией, получавших антипсихотическое лечение перед смертью, демонстрируют значительное увеличение мРНК D 2L в хвостатом ядре (134), что свидетельствует в пользу специфической адаптации D 2L в ответ на хроническая блокада антипсихотическими средствами.Исследования показали, что адаптация мРНК рецептора D 2 с хронической блокадой D2 может (135, 136) или не может (137) быть связана с экспрессией мембранного рецептора, предполагая, что посттранскрипционные механизмы могут более надежно контролировать перемещение рецептора D 2 (138 ). Вместо этого другие исследования демонстрируют прямую связь между транскрипцией гена и экспрессией рецептора D 2 избирательно в полосато-паллидальном пути (139). В настоящее время точное действие антипсихотических средств на изоформы рецептора D 2 все еще остается неубедительным, несмотря на убедительные доказательства этих исследований на трансгенных грызунах.
Синтез, высвобождение и поглощение дофамина
Считается, что уровни дофамина при шизофрении выше, чем у здоровых людей, особенно во время психотических эпизодов (140), а антипсихотические препараты предназначены для уменьшения этой повышенной передачи сигналов дофамина (13). Но неясно, как это могло произойти, если рассматривать только занятость рецептора D 2 (24). D 2 Рецепторы экспрессируются в дендритах, соматах и терминалах дофаминергических нейронов (ауторецепторы) и в постсинаптических нейронах (гетерорецепторы).Стимуляция дофамином ауторецепторов D 2 на терминалах снижает высвобождение синаптического дофамина, в то время как стимуляция соматических ауторецепторов D 2 вместо этого снижает активную активность этих клеток (141). Было обнаружено, что острое применение антипсихотических средств с высоким сродством к рецептору D 2 увеличивает высвобождение дофамина в областях проекции (142), и это увеличение дофамина лишь в минимальной степени обусловлено увеличением активности дофаминовых нейронов (143, 144), поскольку применение Нейролептики непосредственно на соматические ауторецепторы дофаминовых нейронов среднего мозга вызывают лишь умеренное высвобождение дофамина (145).Кроме того, постсинаптические гетерорецепторы D 2 могут умеренно регулировать внеклеточный дофамин в полосатом теле посредством передачи ГАМК, особенно если ауторецепторы гипофункциональны (131). В целом эти основополагающие исследования показывают, что антипсихотические препараты наиболее эффективно контролируют передачу дофамина, воздействуя на рецепторы в терминалях, обнаруженных в полосатом теле. Интересно, что поскольку большинство рецепторов полосатого тела являются гетерорецепторами и лишь незначительно контролируют высвобождение дофамина, увеличение или уменьшение внеклеточных уровней дофамина (35, 45), вероятно, опосредовано другими механизмами, на которые воздействуют нейролептики (38).Эти регуляторные механизмы включают модификации синтеза, высвобождения и поглощения дофамина.
Синтез: Ранние исследования продемонстрировали, что острое лечение антипсихотиками увеличивает синтез дофамина в препаратах in vitro, (146, 147) и ex vivo, (148), а также in vivo у грызунов (149, 150). Считалось, что это опосредовано прямой модификацией фермента тирозингидроксилазы (TH) (151, 152). Однако более поздние исследования не смогли обнаружить изменений в синтезе дофамина in vivo в полосатом теле человека, в то время как сопоставимые дозы антипсихотиков, по-видимому, увеличивали синтез дофамина у животных (153), что лишь частично подтвердило предыдущую работу (149).Хотя это несоответствие между данными о грызунах и людьми не было прояснено, другой ферментативный путь синтеза дофамина (TH против декарбоксилазы ароматических аминокислот, AAAD) у крыс и людей казался правдоподобным объяснением (153, 154). Регулирование внеклеточного дофамина посредством основанного на ауторецептора механизма синтеза дофамина с использованием антипсихотических средств является сложной задачей. Фактически, исследования показали, что снижение синтеза дофамина не имеет терапевтического антипсихотического эффекта (155), и хотя антипсихотическое лечение может увеличивать или уменьшать способность синтеза дофамина (DSC, опосредованное декарбоксилазой DOPA превращение L-DOPA в дофамин) независимо от D 2 блокада рецепторов (156), оба эффекта связаны с улучшением симптоматики (157–159).Эти противоположные результаты могут быть частично результатом очень сложного молекулярного механизма, который совместно регулирует ауторецепторы DAT, TH и D 2 (160–163), поэтому маловероятно, что антипсихотические препараты будут влиять на этот механизм предсказуемым образом.
Ранее мы обнаружили, что экспрессия TH не изменялась эффективными дозами типичных и атипичных антипсихотиков на животных моделях (38). Однако экспрессия TH увеличивалась, когда нейролептики перестали быть эффективными, и это положительно коррелировало с увеличением экспрессии DAT (38).Интересно, что хотя экспрессия TH не изменялась во время антипсихотической эффективности, внеклеточный дофамин увеличивался, а высвобождение везикулярного дофамина уменьшалось, что позволяет предположить, что антипсихотики способствовали модуляции внеклеточного дофамина через снижение поглощения , а не модифицированного синтеза. Таким образом, изменения внеклеточных уровней дофамина могут быть независимыми от скорости синтеза и могут больше зависеть от аутоингибирования и поглощения (38, 164) и / или компенсаторной активности TH (160).
Release : Идея о том, что антипсихотические препараты контролируют высвобождение дофамина в первую очередь за счет блокады ауторецепторов D 2 , впервые возникла в результате ранних экспериментов по молекулярной фармакологии (146, 147, 165–167), показывающих, что антипсихотики обращают ингибирующие эффекты апоморфина. Последующие микродиализные (142) и электрофизиологические (144) исследования подтвердили эти ранние молекулярные открытия. Однако большая часть результатов этих ранних исследований была получена с ограниченными экспериментальными препаратами, такими как синаптосомы (146, 165, 167), или включала использование нейротоксинов для разрушения постсинаптических нейронов при свободно движущемся микродиализе (142), что вызывает тяжелые поражения головного мозга.Таким образом, значительное взаимодействие нейролептиков с ауторецепторами D 2 , обнаруженное в этих ранних исследованиях, следует рассматривать в свете того факта, что эти манипуляции могут нарушить естественную организацию структур в головном мозге. Следовательно, не совсем ясно, контролируют ли терапевтические дозы антипсихотиков in vivo высвобождение дофамина однозначно через ауторецепторы D 2 (141). Современные исследователи, работавшие над этими ранними исследованиями, признали, что этот механизм был правдоподобным лишь отчасти (146, 147, 165).Более того, тот факт, что клозапин, который имеет умеренную аффинность связывания с рецепторами D 2 по сравнению с другими антипсихотиками (78), так же эффективен, как и высокие антипсихотические препараты, при усилении деполяризации за счет блокады ауторецепторов D 2 (144), вероятно, предполагает, что механизмы Помимо D 2 антагонизм ауторецепторов может участвовать в регуляции выработки дофамина антипсихотическими средствами. Одна из механистических возможностей состоит в том, что, по крайней мере, для атипичных антипсихотиков высвобождение дофамина модифицируется серотонинергическими механизмами.Но вряд ли это полностью объясняет вызванное антипсихотиками высвобождение дофамина, поскольку как типичные, так и атипичные нейролептики вызывают высвобождение дофамина (38), но типичные антипсихотики имеют гораздо более низкое сродство к рецепторам 5-HT по сравнению с терапевтическими средствами второго поколения [для обзора , см. ссылки. (168, 169)].
Другая возможность того, как антипсихотики регулируют продукцию дофамина в полосатом теле, заключается в их прямом воздействии на везикулярный экзоцитоз в активных зонах, связанных с каналами Ca 2+ (170, 171).Ранее мы сообщали, что типичные и атипичные нейролептики могут накапливаться в синаптических пузырьках культивируемых нейронов гиппокампа через кислотный механизм захвата и ингибировать каналы Na + при высвобождении. Ингибирование каналов Na + приводит к подавлению притока Ca 2+ по обратной связи и снижению высвобождения везикулярного дофамина (171). Мы протестировали этот механизм, используя схемы лечения антипсихотиками, отражающие клинически значимые результаты антипсихотической эффективности и устойчивости, и обнаружили, что опосредованное экзоцитозом высвобождение дофамина регулируется различными способами в разные моменты лечения галоперидолом (38).В частности, галоперидол подавлял экзоцитоз дофамина при субхронических режимах, т.е. ≤6 дней и во время эффективности лечения, в то время как экзоцитоз дофамина усиливался во время хронического антипсихотического лечения, связанного с потерей поведенческой эффективности (38). Эта четкая регуляция везикулярного высвобождения дофамина во время субхронического по сравнению с хроническим галоперидолом может отражать участие двух разных механизмов, в которых каналы K + опосредуют ингибирование везикулярного высвобождения, а каналы Na + противодействуют этому ингибированию (38).Антипсихотики могут регулировать высвобождение дофамина, напрямую связывая открытое состояние каналов K + (т.е. Kv4.3) во время деполяризации и ускоряя скорость распада инактивации (172–174). Этот механизм действия может регулировать высвобождение дофамина с течением времени независимо от блокады деполяризации, изменяя внутреннюю возбудимость дофаминергических нейронов (175). Кроме того, изменения проводимости K + могут шунтировать эффекты иннервирующих сигналов на дофаминергические нейроны, предотвращая изменения высвобождения дофамина.Еще один механизм, посредством которого нейролептики могут влиять на высвобождение дофамина, включает повышение внеклеточного дофамина как следствие блокады DAT, вызванной антипсихотиками (38), которая может активировать токи GIRK на окончаниях аксонов через взаимодействие между ауторецепторами D2 (24, 38) и каналами Kv1. (176). Мы обнаружили, что K + -опосредованное высвобождение дофамина по-разному влияет на антипсихотическую эффективность и неэффективность у свободно движущихся мышей, подвергающихся лечению, хотя пока не известно, связано ли это с прямым действием нейролептиков на каналы K + или вместо этого опосредуется опосредованно повышенным уровнем эндогенного дофамина.Таким образом, многочисленные доказательства указывают на способность антипсихотиков влиять на высвобождение дофамина, даже если они не обязательно могут влиять на синтез дофамина.
Поглощение : Чтобы понять основной механизм действия нейролептиков, важно понять, как антипсихотические препараты влияют на временную динамику передачи сигналов дофамина во внеклеточном пространстве в полосатом теле, локусе психоза (9). Данные ранних исследований, описанных выше, предоставили множество доказательств того, что нейролептики блокируют рецепторы D 2 и что этого достаточно для восстановления дисрегулируемой передачи сигналов дофамина у многих пациентов, по крайней мере, в течение некоторого периода времени.Однако в этих ранних исследованиях не проводилось должного различия между антипсихотическим действием на пре- и постсинаптические рецепторы D 2 (141), и поэтому неясно, какой тип рецептора D 2 определяет клинические исходы, вызываемые антипсихотиками (24 ). Точно так же неясно, что происходит с дофамином, высвобождающимся во внеклеточное пространство, когда антипсихотические препараты предотвращают его связывание с рецепторами D 2 (24, 38, 169). В нормальных физиологических условиях большая часть внеклеточного дофамина рециркулируется посредством повторного захвата DAT, а оставшийся медиатор диффундирует прочь (177).Повторное поглощение дофамина прекращает передачу дофаминергических сигналов и предотвращает токсические последствия чрезмерного употребления дофамина (178). Соответственно, внеклеточная концентрация дофамина и доступность DAT напрямую коррелируют (179). В отсутствие DAT-опосредованного обратного захвата дофамина никакой другой механизм не может поддерживать гомеостатический контроль пресинаптической функции (180), хотя побочный эффект дофамина также, по-видимому, играет решающую роль в дезактивации передачи сигналов дофамина (181). Как только дофамин собирается в пресинаптических окончаниях, большая его часть перерабатывается и упаковывается в пузырьки (182).Остальная часть ферментативно метаболизируется в цитозоле (180, 183). Следовательно, внеклеточная концентрация дофамина является результатом высвобождения и клиренса дофамина (184, 185), и понимание того, как антипсихотики изменяют этот баланс, имеет терапевтическое значение (38).
Антипсихотическое действие на DAT
Предыдущие метааналитические исследования не обнаружили убедительных доказательств изменений DAT при шизофрении (186), а авторадиографические исследования не обнаружили вызванных антипсихотиками изменений в плотности DAT, меченных [ I25 I] RTI-121 ([125I] Изопропиловый эфир 2-бета-карбоновой кислоты-3-бета- (4-иодфенил) тропан) (187, 188).Однако другие исследования, описанные выше, сообщают, что прямая блокада поглощения дофамина способствует повышению внеклеточного дофамина в ответ на острые нейролептики (146, 147, 165, 189), хотя технология в то время не позволяла четко различать высвобождение и кинетика поглощения. Более поздние исследования с использованием быстрой сканирующей вольтамперометрии показали, что нейролептики с высоким сродством к рецепторам D 2 увеличивают период полужизни дофамина почти на 50% за счет прямой блокады DAT и антагонизма ауторецепторов D 2 (190–192).Соответственно, отсроченный период полувыведения дофамина является результатом прямого ингибирования DAT, поскольку фаза затухания стимулированного перетока дофамина полностью зависит от поглощения (193). В подтверждение этого, записи срезов полосатого тела показали, что антипсихотические препараты не увеличивают высвобождение дофамина после первой стимуляции (192), что противоречит идее о том, что антагонизм ауторецепторов D 2 нейролептиками блокирует аутоингибирование в срезах. Прямое ингибирование DAT нейролептиками происходит при низком сродстве, и антипсихотики менее эффективны, чем более селективные блокаторы DAT, такие как номифензин (194–196).Это помогает нам интерпретировать очевидное отсутствие связи между антипсихотиками и изменениями DAT, о которых сообщалось в предыдущих исследованиях с использованием методов низкой чувствительности (187, 188). Поскольку поглощение является основным путем элиминации внеклеточного дофамина (180, 197), а кинетика диффузии не зависит от высвобождения и поглощения (177), то блокада DAT антипсихотиками может объяснить увеличение количества дофамина и метаболитов дофамина, наблюдавшееся в предыдущих исследованиях микродиализа. (198–202), а также увеличенный период полувыведения дофамина, стимулируемый K + (189).
Дополнительные результаты исследований ex vivo подтверждают прямое взаимодействие между антипсихотиками и DAT. В нормальных физиологических условиях повышенное высвобождение дофамина быстро увеличивает экспрессию мембраны DAT (203, 204). Эффективные дозы антипсихотических препаратов, вводимые субхронически (то есть в течение 2–6 дней), подавляют продукцию мРНК DAT, но не изменяют экспрессию мембраны DAT в полосатом теле (38). Эти эффекты меняются (т. Е. Повышается регуляция мРНК и белка DAT) во время хронического лечения антипсихотиками, связанного с потерей поведенческой эффективности (38).Мы и другие (205) обнаружили аналогичные DAT-адаптации in vivo (38). Визуализация MicroPET с использованием [18F] FP-CMT ([18F] N-3-фторпропил-2-бета-карбометокси-3-бета- (4 ‘метилфенил)) нортропана с превосходными свойствами для визуализации DAT в живом мозге (38 , 206), применяли к крысам на исходном уровне и при последующем наблюдении (т.е. во время потери антипсихотической эффективности). Крысы демонстрируют увеличение доступности DAT (потенциал связывания; BP ND ) во время неэффективности антипсихотических препаратов, что свидетельствует о предполагаемой значимости клиренса дофамина для достижения терапевтического ответа на антипсихотические препараты, по крайней мере, в моделях на животных.Интересно, что изменения, влияющие на экспрессию DAT и соответствующие поведенческие реакции на антипсихотические препараты, сопровождаются стабильной и клинически значимой блокадой рецептора D 2 (69%) и повышением или понижением внеклеточного дофамина в полосатом теле во время проявления антипсихотической эффективности и неэффективности. соответственно (35, 45). Кроме того, важность функции DAT для антипсихотической эффективности подтверждается генетическими исследованиями, показывающими связь между эффективностью клозапина и полиморфизмом гена DAT (207).Что касается вопроса о том, куда идет дофамин, когда пресинаптические и постсинаптические рецепторы D 2 заблокированы, эти исследования предполагают, что он может быть захвачен DAT, который активируется клиническими дозами антипсихотических средств (38). Однако вопреки очевидным теоретическим ожиданиям, что снижение дофамина может оптимизировать терапевтический ответ на антипсихотические препараты, мы обнаружили, что это совпадало с потерей эффективности антипсихотиков. Этот противоречивый результат был развит в другом месте (24, 38), но он будет кратко повторен в следующем разделе и обсужден в контексте шизофрении, устойчивой к антипсихотикам.
Аутоингибирование дофамина как признак антипсихотической реакции
Ранее мы предложили модель антипсихотической эффективности, основанную на потенциальных терапевтических свойствах эндогенного дофамина, с учетом ряда факторов, встречающихся в клинике и в экспериментальных исследованиях на людях. и животные (24, 38). Мы предположили, что антипсихотический эффект
.психических расстройств | Определение, типы, лечение и факты
Психическое расстройство , любое заболевание со значительными психологическими или поведенческими проявлениями, которое связано либо с болезненным или тревожным симптомом, либо с нарушением в одной или нескольких важных сферах деятельности.
Британская викторина
Медицинские термины и викторина для первопроходцев
Кто открыл основные группы крови и разработал систему определения группы крови ABO, которая сделала переливание крови обычной медицинской практикой?
Психические расстройства, в частности их последствия и способы их лечения, сейчас вызывают большее беспокойство и получают больше внимания, чем в прошлом.Психические расстройства стали более заметным объектом внимания по нескольким причинам. Они всегда были обычным явлением, но с искоренением или успешным лечением многих серьезных физических заболеваний, от которых раньше страдали люди, психические заболевания стали более заметной причиной страданий и составляют более высокую долю инвалидов по болезни. Более того, общественность ожидает, что медицинские и психиатрические профессии помогут ей улучшить качество жизни как в умственном, так и в физическом плане.И действительно, наблюдается распространение как фармакологических, так и психотерапевтических методов лечения. Перевод многих психиатрических пациентов, некоторые из которых все еще проявляют заметные симптомы, из психиатрических больниц в общину также повысил осведомленность общественности о важности и распространенности психических заболеваний.
Не существует простого определения психического расстройства, которое бы удовлетворило всех. Отчасти это связано с тем, что психические состояния или поведение, которые считаются ненормальными в одной культуре, могут считаться нормальными или приемлемыми в другой, и в любом случае трудно провести четкую границу, отделяющую здоровое от ненормального психического функционирования.
Узкое определение психического заболевания настаивает на наличии органического заболевания мозга, структурного или биохимического. Чрезмерно широкое определение могло бы определять психическое заболевание как просто отсутствие или отсутствие психического здоровья, то есть состояние психического благополучия, баланса и устойчивости, при котором человек может успешно работать и функционировать и в котором он может как противостоять, так и научиться справляться с конфликтами и стрессами, встречающимися в жизни.Более общее полезное определение относит психическое расстройство к психологическим, социальным, биохимическим или генетическим дисфункциям или нарушениям у человека.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняПсихическое заболевание может влиять на все аспекты жизни человека, включая мышление, чувства, настроение и мировоззрение, а также на такие области внешней деятельности, как семья и супружеская жизнь, сексуальная активность, работа, отдых и управление материальными делами.Большинство психических расстройств негативно влияют на то, как люди относятся к себе, и снижают их способность участвовать во взаимовыгодных отношениях.
Психопатология — это систематическое изучение важных причин, процессов и симптоматических проявлений психических расстройств. Тщательное изучение, наблюдение и исследование, которые характеризуют дисциплину психопатологии, в свою очередь, являются основой психиатрической практики (т. Е. Науки и практики диагностики и лечения психических расстройств, а также борьбы с их профилактикой).Психиатрия, психология и смежные дисциплины, такие как клиническая психология и консультирование, охватывают широкий спектр методов и подходов к лечению психических заболеваний. К ним относятся использование психоактивных препаратов для коррекции биохимического дисбаланса в головном мозге или иным образом для снятия депрессии, беспокойства и других болезненных эмоциональных состояний.
Другая важная группа методов лечения — это психотерапия, которая направлена на лечение психических расстройств психологическими средствами и включает вербальное общение между пациентом и обученным человеком в контексте терапевтических межличностных отношений между ними.Различные режимы психотерапии по-разному фокусируются на эмоциональном опыте, когнитивной обработке и явном поведении.
В этой статье обсуждаются типы, причины и лечение психических расстройств. При заболеваниях нервной системы лечат неврологические заболевания ( см. неврология) с поведенческими проявлениями. Алкоголизм и другие расстройства, связанные с употреблением психоактивных веществ, обсуждаются в контексте алкоголизма и употребления наркотиков. Расстройства полового функционирования и поведения лечатся в сексуальном поведении человека.Тесты, используемые для оценки психического здоровья и функционирования, обсуждаются в психологическом тестировании. Различные теории структуры и динамики личности рассматриваются в рамках личности, в то время как человеческие эмоции и мотивация обсуждаются в контексте эмоций и мотивации. См. Также расстройство личности; психофармакология; психотерапия.
.PPT — Нейролептические препараты = антишизофренические препараты, антипсихотические препараты или основные транквилизаторы. Презентация в PowerPoint
Фармакология, Раздел 10, нейролептики. наркотиков или основных транквилизаторов
Шизофрения
В чем разница? ПСИХОЗ Психоз — это расстройство мышления, характеризующееся нарушениями реальности и восприятия, нарушением когнитивных функций и несоответствующим или ослабленным аффектом (настроением).Психоз обозначает множество психических расстройств. ШИЗОФРЕНИЯ Шизофрения — это особый вид психоза, характеризующийся, главным образом, ясной сенсорией, но выраженным нарушением мышления.
Шизофрения Шизофрения характеризуется глубоким нарушением познания и эмоций, затрагивающих самые фундаментальные человеческие атрибуты: язык, мышление, восприятие, аффекты и самоощущение
Распространенность шизофрении 1,1% населения старше в возрасте 18 лет 51 миллион человек во всем мире страдают шизофренией 12 миллионов человек в Китае (приблизительная оценка, основанная на численности населения) 8.7 миллионов человек в Индии (приблизительная оценка, основанная на численности населения) 2,2 миллиона человек в США 285 000 человек в Австралии Более 280 000 человек в Канаде Более 250 000 диагностированных случаев в Великобритании
Этиология шизофрении Идиопатические биологические корреляты • Генетические факторы • Аномалии развития нервной системы. • Экологические стрессоры.
Риск заболеть шизофренией
Дофаминовая теория шизофрении Многие свидетельства указывают на аномально повышенную активность дофаминергической системы как критическую для симптоматики шизофрении.
Дофаминергическая система Существует 4 основных пути дофаминергической системы в мозгу: мезолимбический путь от черной субстанции к лимбической системе, функции памяти, эмоций, возбуждения и удовольствия Мезокортикальный путь от черной субстанции до неокортекса, познание, социальное поведение, планирование, решение проблем, мотивация и подкрепление в обучении Нигростриатный путь от черной субстанции к полосатому телу, координация непроизвольных движений Тубероинфундибулярный путь от гипоталамуса к гипофизу, секреция определенных гормонов (пролактин)
ДОПАМИНЕРГИЧЕСКАЯ СИСТЕМА
Катехоламины Тирозин Тирозингидроксилаза L-допа Допа-декарбоксилаза Допамин (DA) Допамин гидроксилаза-метилэпинолин-норадреналин (NEO) Норадреналин-EP ) (Адреналин)
Тирозин e Допаминовый синапс Тирозин L-DOPA DA
Дофаминовые рецепторы • Существует как минимум пять подтипов рецепторов: • Дофаминовые рецепторы D1, D5 — цАМФ путем активации аденилатциклазы D1 — скорлупа, acumbhalamus D5 — гипоталамус , гиппокамп • Рецепторы допамина D2, D3, D4 — цАМФ путем ингибирования аденилатциклазы, ингибирует каналы Ca2 + и открывает каналы K + D2 — хвостатое ядро - скорлупа, ядро acumbens D3 — лобная кора, продолговатый мозг, средний мозг
Гипотеза допамина (1): Большинство антипсихотических препаратов сильно блокируют постсинаптические рецепторы D2 в ЦНС (мезо-лимбической системе). Лекарства, повышающие дофаминергическую активность, усугубляют шизофрению и вызывают психоз de novo. Повышенная плотность дофаминовых рецепторов была обнаружена посмертно в мозгу шизофреников
Гипотеза дофамина (2): ПЭТ показала повышенную плотность рецепторов дофамина у шизофреников Успешное лечение У шизофреников изменяется количество гомованилиновой кислоты — метаболита дофамина в спинномозговой жидкости, плазме и моче.
Дисфункция DA-ергической системы: Гиперактивность DA-системы (мезолимбический путь) Гипоактивность лобной коры (мезокортикальный путь) Дисфункция 5-HT, ГАМК и глутамат -ергической системы SCHIZOPHRENIA
Течение шизофрении
Раннее вмешательство и раннее использование новых лекарств приводит к улучшению медицинских результатов на человек • Кто-то раньше с шизофренией диагностируется и стабилизируется после лечения, тем лучше долгосрочный прогноз их болезни. • Самоубийства среди подростков — растущая проблема, и подростки с шизофренией имеют примерно 50% -ный риск попытки самоубийства. • Антипсихотические препараты являются обычно рекомендуемым лечением шизофрения !!! • Если лечение шизофрении прекращается, частота рецидивов составляет около 80 процентов в течение 2 лет.При продолжении медикаментозного лечения только около 40 процентов выздоровевших пациентов будут иметь рецидивы.
Исходы шизофрении После 30 лет диагностики шизофрения 25% Полное выздоровление 35% Значительно улучшилось, относительно независимо 15% Улучшилось, но требуется широкая сеть поддержки 10% Госпитализировано, неулучшено 15% Погибло (в основном самоубийство)
Симптомы шизофрении (1): Положительные, по всей видимости, отражают избыток или нарушение нормальных функций: * бред (параноидальный, эталонный, соматический, мания величия) * галлюцинации (визуальные, слуховые, тактильные, обонятельные, вкусовые) * неорганизованная речь = «Словесный салат» * дезорганизованное или кататоническое поведение Отрицательное, по-видимому, отражает снижение или потерю нормальных функций: * отсутствие эмоций * низкая энергия * эмоциональное уплощение * низкая мотивация * несоответствующие социальные навыки * алогия
Термины «положительный «и» отрицательный «могут сбивать с толку.Их не следует рассматривать как «хорошие» и «плохие» симптомы.
Симптомы шизофрении (2): Когнитивное дезорганизованное мышление медленное мышление трудности с пониманием плохой концентрации плохая память трудности с выражением мыслей трудности с объединением мыслей, чувств и поведения
Симптомы шизофрении (3): Неорганизованные симптомы (?) * Расстройство мышления * спутанность сознания * дезориентация * проблемы с памятью. Неорганизованные симптомы могут отражать лежащую в основе дисфункцию, общую для нескольких психотических расстройств, а не уникальную для шизофрении.
Активная фаза Галлюцинации и бред являются выраженными симптомами Остаточная фаза Шизофрения
Диагностические критерии США для шизофрении (1) • A. Характерные симптомы: ≥2 в течение 1-месячного периода: бредовые галлюцинации, расстройства речи, галлюцинации Негативные симптомы дезорганизованного поведения
Диагностические критерии США для шизофрении (2) Только один критерий Симптом требуется, если бред причудливы или галлюцинации состоят из голоса, который постоянно комментирует поведение или мысли человека, или два или два больше голосов разговаривают друг с другом.
Диагностические критерии шизофрении в США (3) B. Социальная / профессиональная дисфункция работа межличностные отношения самопомощь C. Продолжительность непрерывных признаков нарушения сохраняется не менее 6 месяцев, включая 1 месяц симптомов из критерия A и продромальные симптомы)
Диагностические критерии США для шизофрении (4) D. Исключение шизоаффективных расстройств и аффективных расстройств не было серьезных депрессивных, маниакальных или смешанных эпизодов с симптомами активной фазы E.Исключение психоактивных веществ / общего состояния здоровья F. Связь с распространенным нарушением развития
Типы шизофрении Параноидальная шизофрения Дезорганизованная шизофрения (гебефреническая) Кататоническая шизофрения Остаточная шизофрения (гебефреническая) Кататоническая шизофрения Остаточная шизофрения 9000 9000 9000 9000 9000 DR 9000 9000 9000 DR 9000 9000 9000 DR 9000 9000 9000 9000 DR 9000 9000 9000 9000 9000 DR 9000 9000 9000 9000 9000 DR 9000 типичные нейролептики атипичных нейролептиков фенотиазины бензизоксазолы тиоксантены дибензо диазепинов BUTYRO-PHENONES
фенотиазины хлорпромазин Флуфеназин Прохлорперазин прометазин тиоридазин
Другие группы типичных нейролептиков тиоксантен Thiothixene бутирофенон галоперидол
Типичные нейролептики — механизм действие
Механизмы действия нейролептиков
Нетипичный n euroleptics Бензизоксазолы Рисперидон Зипразидон Дибенодиазепины Клозапин Кветиапин Оланзапин
Атипичные нейролептики — механизм действия
В чем состоит клиническая разница между более старыми лекарствами? Было показано, что новые антипсихотические препараты более эффективны для лечения негативных симптомов, чем старые.
Действия нейролептических препаратов (1) Дофаминовый рецептор все, в частности: галоперидол, флуфеназин, тиотиксен Мускариновый рецептор тиоридазин, хлорпромазин — Адренергический рецептор хлорпромазин Серотониновый рецептор рисперидон, клозапин h2 — гистаминовый рецептор прометазин, хлорпромазин
Действие нейролептиков (2) Антипсихотические действия: уменьшают галуцинации, уменьшают спонтанные физические движения, возникают после 4-6 недель лечения. поздняя дискинезия
Действия нейролептических препаратов (3) Противорвотный эффект (кроме тиоридазина) Антимускариновый эффект: помутнение зрения, сухость во рту, седативный эффект, спутанность сознания, угнетение ЖКТ и гладких мышц мочевого пузыря Другие эффекты: гипотензия, головокружение
Нейролептические препараты не излечивают и не устраняют фундаментальное расстройство мышления , но часто позволяют психотическому пациенту функционировать в поддерживающей среде
Терапевтическое применение Шизофрения Другие психозы Шизоаффективные расстройства Бред Предотвращение сильной тошноты и рвота (головокружение, укачивание, химио- и лучевая терапия рака) Транквилизаторы В сочетании с наркотическими анальгетиками для лечения хронической боли с сильной тревожностью Непреодолимая икота
Фармакокинетика Нейролептики всасываются после перорального приема Пройти через гематоэнцефалический барьер Связать хорошо связывается с белками плазмы, хорошо растворимы в жирах Метаболизируются в печени системой P-450
Острая Острая дистония Среднесрочная акатизия Паркинсонизм Хроническая поздняя дискинезия Поздняя дистония Побочные эффекты (1) • Неврологические эффекты из-за блокады рецепторов D2 e
Острая дистония • В начале лечения • Часто встречается у молодых мужчин • Лечение антихолинергическими препаратами (проциклидин 5-10 мг или бензтропин i.m или iv) Фиксированные позы мышц со спазмом: • сжатые мышцы челюсти • высунутый язык • опистотонус • кривошея • окулогирный криз (рот открыт, голова назад, глаза смотрят вверх)
Akathisia • двигательное беспокойство • влияет на нижнюю конечность • очень огорчает пациента • Лечение — снижение дозы препарата.



