Антидепрессанты эффективные: Психиатры назвали самые эффективные антидепрессанты — Naked Science
1. Купирующая терапия ДЭ на 1 этапе / КонсультантПлюс
1. Купирующая терапия ДЭ на 1 этапе
— Для пациентов, удовлетворяющих современным диагностическим критериям ДЭ и РДР (МКБ-10), рекомендуется применение тимоаналептической фармакотерапии: назначение АД в эффективных дозах [59, 60, 61].
Уровень достоверности доказательств 1 (уровень убедительности рекомендации A).
Комментарии. АД следует назначать в минимальных эффективных дозах; при отсутствии побочных эффектов или при редукции побочных эффектов в течение нескольких дней рекомендуется производить увеличение дозы в пределах стандартных дозировок до тех пор, пока симптоматика не начнет ослабевать. В случае отсутствия динамики или недостаточного эффекта (степень редукции симптоматики от 25% до 50%) через 3 — 4 недели рекомендуется наращивание дозы до максимальной (табл. 2) [61].
Тимоаналептический эффект обычно возникает через 3 — 4 недели лечения, однако в некоторых случаях, особенно при применении СИОЗС, улучшение развивается более постепенно и достижение полноценного эффекта наблюдается на 4 — 6-й или даже 8-й неделе.
Современные критерии депрессивного синдрома могут включать довольно гетерогенные группы больных с различными типами депрессий в диапазоне от биологически детерминированных состояний (так называемых эндогенных или меланхолических депрессий) до в разной степени ситуационно спровоцированных или связанных с личностной патологией (так называемых реактивных или невротических депрессий). К сожалению, большинство рандомизированных контролируемых исследований (РКИ) лекарственных средств с антидепрессивным эффектом использовало обобщенные недифференцированные критерии ДЭ, и не представляется возможным выделить их доказательную эффективность в отношении отдельных клинических вариантов, например, при тревожной, меланхолической (с соматическими симптомами), атипичной, заторможенной (с кататоническими симптомами), сезонной или с преобладанием когнитивных нарушений).
Не существует доказательных данных о большей эффективности или более быстром начале действия АД какого-либо одного класса, хотя при тяжелых, требующих госпитализации, депрессиях некоторые ТЦА (амитриптилин** и кломипрамин**) и венлафаксин оказываются несколько эффективнее, чем селективные ингибиторы обратного захвата серотонина (СИОЗС) [64, 65]. В отношении АД второго поколения сравнительный метаанализ 117 РКИ, включавший 25,928 больных, показал, что миртазапин, эсциталопрам, венлафаксин и сертралин** были несколько более эффективны, чем дулоксетин, флуоксетин**, флувоксамин и пароксетин** [66]. АД прежде всего различаются по профилю побочных эффектов, потенциалу взаимодействия с другими препаратами и опасности передозировки. АД из классов СИОЗС, СИОЗСН, а также другие АД второго и третьего поколений в целом переносятся лучше, чем препараты первого поколения (ТЦА), что способствует уменьшению вероятности самостоятельного отказа пациентов от их приема.
Таблица 2. Рекомендуемые дозы АД
Генерическое название | Стартовая доза (мг/с) | Диапазон доз (мг/с) |
Селективные ингибиторы обратного захвата серотонина | ||
Пароксетин** | 20 | 20 — 50 |
Сертралин** | 50 | 50 — 200 |
Флувоксамин | 50 — 100 | 100 — 300 |
Флуоксетин** | 20 | 20 — 80 |
Циталопрам | 20 | 20 — 40 |
Эсциталопрам | 10 | 10 — 20 |
Селективные ингибиторы обратного захвата серотонина и норадреналина (в соответствии с АТХ — другие антидепрессанты) | ||
Венлафаксин | 75 | 75 — 375 (> 225 в стационарных условиях) |
Дулоксетин | 60 | 60 — 120 |
Милнаципран | 100 | 100 |
Неселективные ингибиторы обратного захвата моноаминов (трициклические АД) | ||
Амитриптилин** | 50 — 75 | 150 — 300 (> 150 в стационарных условиях) |
Имипрамин** | 25 — 75 | 150 — 300 (> 200 в стационарных условиях) |
Кломипрамин** | 50 — 75 | 100 — 250 |
Пипофезин** (в соответствии с АТХ — другие антидепрессанты) | 25 — 50 | 150 — 500 |
Норадренергические и специфические серотонинергические АД (в соответствии с АТХ — другие антидепрессанты) | ||
Миансерин | 30 | 60 — 90 |
Миртазапин | 15 — 30 | 15 — 45 |
Специфические серотонинергические АД (в соответствии с АТХ — другие антидепрессанты) | ||
Тразодон | 100 | 150 — 600 (> 450 в стационарных условиях) |
Ингибиторы моноаминоксидазы типа A | ||
Пирлиндол (в соответствии с АТХ — другие антидепрессанты) | 50 — 75 | 150 — 400 |
Мелатонинергические АД (в соответствии с АТХ — другие антидепрессанты) | ||
Агомелатин** | 25 | 25 — 50 |
Серотонинергические модуляторы (в соответствии с АТХ — другие антидепрессанты) | ||
Вортиоксетин | 10 | 10 — 20 |
Открыть полный текст документа
Эндогенная депрессия, препараты.
 Эффективные антидепрессанты при депрессии
Эффективные антидепрессанты при депрессииК сожалению, от депрессивного состояния не застрахован никто. Поэтому очень важно понимать, что представляет собой депрессия, и как с ней справиться.
Что такое эндогенная депрессия и каковы пути ее лечения
Депрессия – это расстройство психики человека, которое сопровождается угнетенным настроением, утратой способности радоваться, снижением работоспособности, нарушением умственных процессов и т.д.
Специалисты выделяют два вида депрессии:
1. Экзогенная или реактивная. Причина ее возникновения – это факторы, находящиеся вне человека. Обычно, это реакция человека на какую-то психотравму: болезнь или смерть близкого человека, неудачи в семейной жизни или карьере, серьезный конфликт, постоянные стрессы.
2. Эндогенная. Причина наступления данной депрессии связана с внутренним состоянием человека. В большинстве случаев, к развитию эндогенной депрессии приводит недостаток гормонов (норадреналина, серотонина, дофамина).
Для эндогенной депрессии характерны такие симптомы:
− подавленность, чувство пустоты, тоски;
− постоянная усталость;
− заторможенность или возбуждение движений, речи;
− постоянная сонливость или, наоборот, бессонница;
− потеря аппетита или повышенный аппетит.
Эндогенная депрессия в идеале нуждается в комплексном лечении: психотерапия + антидепрессанты. Данные препараты помогают человеку справиться с этими расстройствами и вернуться к нормальной жизни.
Для того чтобы правильно подобрать антидепрессант, нужно четко понимать, какой вид депрессии у вас, внешними или внутренними причинами он а вызвана, и на какой стадии находится заболевание. Если вы не можете определить это самостоятельно, необходимо обратиться к специалисту.
Какие антидепрессанты лучше принимать при депрессии: что нужно учесть
Лучшие антидепрессанты для лечения затяжной депрессии – это, в первую очередь, правильно подобранные препараты. Вы должны знать, что эффективные антидепрессанты при депрессии – это достаточно сильнодействующие лекарства, которые продаются по рецептам врача. Людям с алкогольной или наркотической зависимостью, перед приемом необходимо проконсультироваться с врачом. Осторожными нужно быть и пациентам, страдающим хроническими заболеваниями.
Людям с алкогольной или наркотической зависимостью, перед приемом необходимо проконсультироваться с врачом. Осторожными нужно быть и пациентам, страдающим хроническими заболеваниями.
Антидепрессанты при легкой депрессии можно подобрать из препаратов продающихся без рецепта. Один из таких препаратов – Нормотим. Он позволяет предупредить наступление депрессии, эффективно борется с легкими депрессивными состояниями.
Не допустить развития тяжелой формы депрессии вам помогут успокоительные препараты.
зачем попугаю антидепрессанты, а соколу — дроны / Новости города / Сайт Москвы
Почти 40 лет назад, 19 февраля 1983 года, было организовано Всесоюзное орнитологическое общество при Академии наук СССР. С тех пор в этот день отмечается День орнитолога. Это знаковый праздник для всех сотрудников орнитария в парке «Сокольники», в том числе и для тех, кто не учился на орнитолога, но работает с птицами по велению души.
О том, как в орнитарий попадают птицы и кто о них заботится, — в материале mos.
На территории орнитария — множество вольеров с птицами. На улице даже зимой живут огромные черные вороны, сороки, ястребы, неясыти, пустельги и балобаны — они не боятся низких температур.
Для соколов обустроили двор с присадами — специальными кольцами, на которых птицы могут сидеть, при необходимости свободно расправляя крылья. Как объяснил директор орнитария Вадим Мишин, присады — дань вековой традиции содержания ловчих птиц, именно они помогают сохранять их оперение в идеальном состоянии.
В «Сокольниках» также находится самая большая в Москве голубятня — ее площадь составляет 250 квадратных метров. На крыше есть специальные отверстия, благодаря которым птицы могут свободно вылетать и прилетать обратно.
В теплом здании содержатся перелетные птицы — до прихода весны они не живут на улице. Среди них — чеглоки, осоеды и ястреб-перепелятник. Здесь же располагаются помещения для сотрудников.
Орнитарий в «Сокольниках» появился восемь лет назад. Его создатель Вадим Мишин по профессии никак не был связан с птицами, а идея организовать соколиный двор возникла спонтанно.
«Однажды меня товарищ спросил: “Как же так, “Сокольники” — и без соколов?” Ведь исторически это место, где цари занимались соколиной охотой. Так появилась идея создать соколиный двор, я пришел с ней к директору парка, и он меня поддержал», — говорит Вадим Мишин.
Ловчих птиц приобретают в питомниках. Специалисты, которые обучают взрослых древнему искусству соколиной охоты, держат здесь и своих питомцев.
Изначально планировали сделать упор именно на соколиный двор, но выяснилось, что орнитарий нужен и как место реабилитации, лечения и содержания птиц. Сюда попадают пернатые, которые нуждаются в постоянном уходе. Кого-то приносят владельцы, которые понимают, что не могут самостоятельно заботиться о крылатом питомце.
Важно, что проект открытый: птиц можно навещать, узнавать об их состоянии, помогать деньгами или кормом. Принимают в орнитарии всех, независимо от вида, ценности и редкости птицы.
«Всех берем — и голубей, и ворон. Мы никого не сортируем по ценности. Наша задача — вылечить, выходить и выпустить. Поэтому если мы понимаем, что птица сможет вернуться на волю, стараемся к ней не привязываться, даже имя не даем. Важно, чтобы птица не стала совсем ручной», — объясняет Вадим Мишин.
Некоторых птиц берут на содержание волонтеры. Однако не всем можно доверить такую ответственность — доброволец должен уметь ухаживать за птицей, знать потребности и особенности конкретного вида.
Остаются зимовать: каких водоплавающих птиц заметили на столичных водоемах
Пломба для дятла и антидепрессанты для попугаяДля вновь прибывших постояльцев есть карантинное отделение — в нем птицы живут, пока у них берут анализы и выясняют, нужна ли им медицинская помощь (и если нужна, то какая). Если после карантина птица все еще не может жить на воле, ее переводят в стационар. Здесь крылатые пациенты получают необходимое лечение. Птицы, чьи травмы вылечить нельзя, остаются жить в орнитарии.
Если после карантина птица все еще не может жить на воле, ее переводят в стационар. Здесь крылатые пациенты получают необходимое лечение. Птицы, чьи травмы вылечить нельзя, остаются жить в орнитарии.
Например, среди постоянных жильцов — ворон со сломанным крылом. Оперировать его не стали — такие манипуляции птицы переносят плохо, к тому же ворон все равно не смог бы снова летать. Уже четыре года здесь живет осоед, ставший жертвой браконьеров. Птица попала в силки и сильно повредила лапы.
Совсем недавно в птичьем приюте оказалась самка беркута по имени Кайлас. Ей уже 15–16 лет — солидный возраст для беркутов, которые в природе живут до 20. Кайлас перенесла черепно-мозговую травму, у нее сахарный диабет, сердечная и легочная недостаточность.
Лечит пернатых пациентов и помогает ухаживать за ними ветеринар-орнитолог Наталья Анисимова. Иногда ей приходится изобретать нестандартные методы. Например, для дятла с расслоившимся клювом она придумала сделать «гипс» из того же материала, который используют стоматологи для пломбирования зубов. Это помогло — у дятла нарастает новый целый клюв, и вскоре он сможет вернуться в естественную среду обитания.
Это помогло — у дятла нарастает новый целый клюв, и вскоре он сможет вернуться в естественную среду обитания.
«С маленькими птичками нередко случаются черепно-мозговые травмы, потому что они ударяются о стекла, — рассказывает Наталья. — Бывает, что птиц сбивают машины, на голубей часто нападают хищники. К сожалению, многие птицы, особенно вороны, становятся жертвами жестоких забав — люди используют их как живые мишени».
Как отмечают сотрудники, пневматическое оружие, которое продается без лицензии, для птиц опаснее всего. Пули от него не убивают их сразу, но дробят кости и остаются в теле. Если птица не попадает в руки ветеринара, то погибает медленно и мучительно.
Даже в офисе администрации — клетки с попугаями, которых не смогли оставить у себя бывшие владельцы. Незнакомых людей они встретили хлопаньем крыльев и поддерживали беседу на своем птичьем языке.
«Когда здесь тихо, то и птицы молчат, — пояснил Вадим Мишин. — А поскольку мы разговариваем, то и они хотят участвовать в беседе».
Как и люди, птицы могут страдать от психических расстройств. Выражаются такие проблемы в том, что птицы выдергивают себе перья. Поэтому, например, одному из попугаев жако приходится принимать антидепрессанты. Сейчас пациент чувствует себя гораздо лучше и может похвастаться красивым, недавно отросшим, серо-голубым оперением.
У птиц хорошая память, они помнят добро и зло. Пернатые, пострадавшие от людей, могут получить серьезную психологическую травму. Со временем, уже после лечения, такие птицы могут спокойно реагировать на сотрудников и посетителей парка, но вернуть доверие к людям полностью не удается.
Некоторые постояльцы птичьего приюта, наоборот, настолько привязываются к людям, что не хотят покидать их, даже выздоровев.
Однажды принесли гнездо с тремя скворчатами. Их выходили, двое улетели, а один остался. Назвали его Сынок. Скворец садился к людям на плечо, повсюду ходил за ними и как-то раз участвовал в проверке билетов посетителей. Когда пришло время улетать в теплые края, он покинул орнитарий, но несколько лет подряд возвращался и жил в скворечнике на его территории.
«Жил у нас дубонос, которого мы выпускали раз пять. Так он находил какого-нибудь человека в парке и начинал долбить его клювом, пока его не относили обратно в орнитарий», — рассказывает Вадим Мишин другую забавную историю.
Редкая утка: в Москве зимой заметили краснокнижного чирка-свистункаОсоед и серая утка: в Москву вернулись исчезнувшие редкие животные
Гордые и верныеПрофессия сокольника считается одной из самых редких, поэтому в орнитарии очень ценят сотрудничество с мастерами. Искусство соколиной охоты — это, прежде всего, умение наладить контакт с ловчей птицей. Нужно стать ей другом, а не хозяином, найти с ней общий язык — именно этому сокольник должен посвящать большую часть времени. Не только человек выбирает птицу, с которой будет работать, но и птица — человека.
К ловчим птицам нужен особый подход: метод кнута и пряника, который применяют для дрессировки животных, здесь не подойдет. Каждый сокольник знает: если на гордую птицу кричать или наказывать ее, она может ответить агрессией или вовсе улететь. Поэтому при дрессировке специалисты только поощряют питомцев.
Поэтому при дрессировке специалисты только поощряют питомцев.
Сегодня соколиная охота почти утратила свое практическое назначение. Именно поэтому в планах организовать спортивную соколиную охоту, в которой вместо живых жертв будут дроны-муляжи. Для участия в таком виде спорта птица должна быть обучена охоте именно на муляж, а к дронам будут прикреплять кусочки мяса в качестве поощрения.
Ловчие птицы приносят пользу не только на охоте: соколиные службы используют для того, чтобы разгонять пернатых, например, рядом с крупными зернохранилищами. Стаи птиц, которые гнездятся рядом с аэропортами, тоже несут опасность: попадая в турбины самолета, они могут спровоцировать аварию. Единственный эффективный способ разгонять их — держать хищников.
Вадим Мишин убежден, что разнообразие видов птиц необходимо сохранять.
«Мы, скажем, занимаемся цветоводством, выводим новые сорта цветов, пестуем их на клумбах, выхаживаем — из-за чего? Из-за красоты, из-за нашей в ней потребности.Птицы — это, можно сказать, цветы небесные. И во многих ситуациях, особенно в городских условиях, если мы оставим их без помощи, то они с нами сосуществовать не будут. Останутся, может быть, только вороны и голуби, но ведь этого мало», — рассуждает он.
Орнитарий открыт для посетителей со вторника по воскресенье (понедельник — санитарный день). В будние дни орнитарий работает с 11:00 до 19:00, а в выходные дни — с 11:00 до 20:00.
ТОП 15 препаратов при климаксе (менопаузе)
Менопауза – сложный период в жизни каждой женщины, который сопровождается угнетенным состоянием и неприятными симптомами. Климакс характеризуется гормональной перестройкой организма. Репродуктивная система постепенно снижает свою активность. Для поддержания организма при климаксе врачи рекомендуют принимать гормональные или негормональные препараты. Их эффективность направлена на укрепление женского здоровья и нормализацию общего состояния.Предлагаем рейтинг препаратов при климаксе, основанный на мнении врачей и отзывах покупателей. Перед покупкой лекарств рекомендуется проконсультироваться со специалистом. Только врач может подобрать подходящий медикамент, опираясь на результаты проведенной диагностики.
Перед покупкой лекарств рекомендуется проконсультироваться со специалистом. Только врач может подобрать подходящий медикамент, опираясь на результаты проведенной диагностики.
Классификация препаратов при климаксе
Виды используемых препаратов:
- Гормональные. Направлены на повышение уровня эстрогена – устранение самой причины. Позволяют сохранить детородную функцию дольше. Гормон нормализует состояние, устраняя неприятные симптомы. Гормональный фон организма при этом остается неизменным.
- Негормональные. Носит симптоматическое лечение, значительно уменьшая неприятные симптомы. Результат появляется не сразу, а спустя некоторое время. Самочувствие улучшается постепенно. Негормональные средства имеют накопительный эффект. Из аптек отпускаются без рецепта врача.
Гормональные средства имеют массу противопоказаний и побочных эффектов. Их недопустимо принимать без предварительной сдачи анализов. Именно по этой причине мы подобрали список наиболее щадящих средств, которые не причиняют организму вреда, эффективно устраняя проблему.

Критерии сравнения препаратов при климаксе основаны на составе таблеток и отзывах покупателей. Немаловажное значение имеет стоимость медикаментов. На основании этой информации мы представили рейтинг негормональных препаратов при климаксе.
Особенности климактерического периода
Существует три основных стадии климакса:
- Пременопауза. Начинается с 40-45 лет и длится на протяжении 10 лет. Характеризуется появлением приливов, снижением полового влечения, частыми головными болями и депрессивным состоянием.
- Менопауза. Наступает в возрасте 50-55 лет. Сопровождается прекращением работы яичников и окончанием менструаций. В этот период заметно стареет кожа, костные структуры становятся хрупкими
- Постменопауза. Наступает в возрасте от 55 лет. Неприятная симптоматика исчезает и больше не появляется.
Среди основных симптомов климакса следует выделить приливы (ощущение жара), чрезмерное потоотделение и изменения внешности (кожа теряет упругость и становится сухой). Также характерна эмоциональная нестабильность, изменение восприятия окружающего мира и бессонница.
Также характерна эмоциональная нестабильность, изменение восприятия окружающего мира и бессонница.
Рейтинг препаратов при менопаузе
№1 – «Менорил Плюс» (капсулы)
Разработан на основе биофлавоноидов – веществ растительного происхождения или их синтетических аналогов. Оказывает воздействие, аналогичное эффективности эстрогенов женского организма:
- Витамин D3. Нормализует состояние костных структур, кишечника и паращитовидной железы. Принимает участие в процессах абсорбции кальция.
- Витамин К1. Принимает участие в восстановлении костей, предотвращая развитие остеопороза.
- Ресвератрол. Фитоалексин является мощным антиоксидантом, который по активности превосходит витамин Е.
«Менорил Плюс» является лучшим препаратом для симптоматического лечения климакса. Уменьшает частоту приливов, нормализует показатели артериального давления, уменьшает слабость и избавляет от головных болей.
№2 – «Doppelherz Актив Менопауза» (таблетки)
Биологически активная добавка к пище, которая является источником кальция, фолиевой кислоты, биотина, изофлавонов сои и витаминов D3, B1, 2, 6 и 12.
 Обладает общеукрепляющим эффектом, что необходимо женщинам в пре- и постменопаузальный период.
Обладает общеукрепляющим эффектом, что необходимо женщинам в пре- и постменопаузальный период.Устраняет последствия менопаузы, предотвращая развития психоэмоциональных расстройств и вегетососудистых нарушений. Способствует улучшению качества жизни, сохраняя красоту и здоровье.
№3 – «Менопейс Плюс» (капсулы и таблетки)
Разработан на основе изофлавоноидов, флаволигнанов, витаминов и минеральных веществ. Нормализует гормональный уровень, восполняя дефицит необходимых веществ для нормальной жизнедеятельности.
Фармакологическое действие «Менопейс Плюс»:
- гормональная регуляция;
- поддержка нервной системы;
- образование коллагена;
- укрепление сосудов и сердца;
- поддержка здоровья костей.
Является лучшим препаратом от приливов при климаксе. Назначается для предупреждения симптомов менопаузы и их облегчения. Поддерживает организм и предотвращает развитие остеохондроза.

№4 – «Lady`s Formula Менопауза День-Ночь» (таблетки)
Антиклимактерическое, адаптогенное средство, регулирующее гормональный баланс. Биокомплекс направлен на улучшение качества жизни женщин, находящихся в пери- и постменопаузальном периоде. Помогает облегчить симптомы психоэмоционального характера (лабильность настроения, слезливость, навязчивые идеи и пр.). Поддерживает энергичность днем и помогает бороться с бессонницей.Рекомендуется использовать при наличии наследственного отягощения остеопорозом и при функциональных расстройствах ЦНС. Назначается также при иммунодефицитных состояниях и женщинам, у которых имеются вредные привычки. Имеются противопоказания в виде индивидуальной непереносимости компонентов, артериальной гипертензии и выраженного атеросклероза.
№5 – «Lady`s Formula Менопауза Усиленная формула» (таблетки)
Натуральный биокомплекс разработан на основе запатентованной растительной формулы. Направлен на устранение симптомов менопаузы и предотвращение развития осложнений.

Особенности усиленной формулы заключается в снижении частоты и выраженности приливов. Это лучшие таблетки при климаксе, с помощью которых удается уменьшить раздражительность и частоту смены настроения. Незаменимы в период ранней менопаузы, в т. ч. и при удалении яичников.
№6 – «Менопейс» (капсулы)
Содержит минералы и витамины, регулирующие гормональный баланс. Поливитамины отличаются комбинированным действием:
- Пантотеновая кислота. Регулирует уровень продукции эстрогенов надпочечниками.
- Витамины группы В и аскорбиновая кислота. Принимают участие в синтезе гамма-линоленовой кислоты, ослабляющей симптомы менопаузы и регулирующей гормональный баланс.
- Витамин Е. Способствует нормализации процесса теплорегуляции, снижает распад прогестерона и устраняет нервозность.
Практически не имеет противопоказаний. Не рекомендуется использовать при индивидуальной непереносимости компонентов.
№7 – «Ци-Клим» (таблетки)
Противоклимактерическое средство растительного происхождения. Активный компонент – экстракт цимицифуги. Лучший препарат при менопаузе, который используется для проведения негормональной терапии.
Устраняет дефицит эстрогенов, помогает справиться с приливами, ночными потами, приступами сердцебиения. Предотвращает ранее старение, сухость кожного покрова и слизистых оболочек.
№8 – «Климадинон» (таблетки, покрытые оболочкой)
Разработан на основе сухого экстракта корневищ цимицифуги. Фитопрепрат назначается для облегчения климактерического синдрома:
- при вегето-сосудистых расстройствах;
- для борьбы с усиленным потоотделением;
- с целью уменьшения повышенной возбудимости.
Побочные эффекты связаны с появлением аллергической реакции и повышением массы тела. В более редких случаях отмечается появление боли в эпигастральной области, менструальноподобные кровотечения и напряжение в области молочных желез.
№9 – «Клималанин» (таблетки)
Действующий компонент – бета-аланин. Аминокислота предотвращает резкое высвобождение гистамина, но не оказывает антигистаминной активности. Расширяет периферические кожные сосуды, что лежит в основе вегетативных реакций в период менопаузы. Данные вазомоторные реакции обусловлены чрезмерной активностью терморегуляторных центров в гипоталамусе, что происходит при нарушении баланса церебральных нейротрансмиттеров. Возникает это на фоне прекращении секреции гормонов яичниками. Благодаря бета-аланину удается насытить периферические рецепторы нейротрансмиттеров.
«Клималанин» — лучший препарат от потливости при климаксе. Нужно с осторожностью принимать при почечной и печеночной недостаточности.
№10 — «Климактоплан Н» (таблетки для рассасывания)
Гомеопатическое средство, комплексное действие которого обусловлено вхождением в состав сразу нескольких активных компонентов. Назначается при климактерическом синдроме, который сопровождается усиленным сердцебиением, повышенным потоотделением, зудом, головокружением и нервным напряжением.

Курс терапии составляет от 3 до 4 месяцев. Рекомендуется принимать в комплексной терапии. Возможны побочные действия со стороны желудочно-кишечного тракта. Не исключены аллергические реакции. Среди противопоказаний – непереносимость лактозы и недостаточность лактазы.
№11 – «Климаксан» (таблетки для рассасывания)
Гомеопатическое средство смягчает психоэмоциональное напряжение при климактерическом синдроме. Направлено н снижение выраженности вегетативных реакций, таких как приливы, потливость, головная боль и сердцебиение.
Не имеет утвержденных терапевтических показании. Традиционно используется в качестве симптоматического средства при проведении терапии. Длительность лечения составляет 6 месяцев. По рекомендации врача возможны повторные курсы. При передозировке возможно возникновение диспепсических явлений (нарушений со стороны пищеварения).
№12 – «Тайм-фактор» (капсулы)
БАД является источником фолиевой кислоты, витамин Е и С.
 содержит рутин, аукубин и гингеролы. Назначается для нормализации менструального цикла, регулирования деятельности репродуктивной системы и поддержание гормонального баланса.
содержит рутин, аукубин и гингеролы. Назначается для нормализации менструального цикла, регулирования деятельности репродуктивной системы и поддержание гормонального баланса.Самое лучшее негормональное средство, которое не имеет противопоказаний, за исключением индивидуальной непереносимости компонентов. При соблюдении рекомендаций производителя побочных реакций не возникает.
№13 – «Тайм Эксперт Коэнзим Q10 с витамином Е» (таблетки)
БАД, действие которого направлено на длительное сохранение красоты и молодости. Не является лекарственным средством. Замедляет процессы старения. Витаминный комплекс рассчитан специально для женщин преклонного возраста. Помогает продлить репродуктивные функции, нормализуя общее состояние организма.
№14 – «Индинол» (капсулы)
Селективный модулятор эстрогенных рецепторов подавляет индукцию эстроген-зависимых генов. В связи с этим клетка перестает получать чрезмерную стимуляцию.
Универсальный корректор предупреждает развитие гиперпластических процессов в тканях и органах женской репродуктивной системы.
 уничтожает трансформированные клеточные структуры с аномально высокой пролиферативной активностью.
уничтожает трансформированные клеточные структуры с аномально высокой пролиферативной активностью.№15 – «Менсе» (капсулы)
Биологически активная добавка к пище, которая разработана на основе комплекса витаминов и минералов, необходимых в климактерическом периоде. Предупреждает появление менопаузы и смягчает его симптомы. Концентрация активных компонентов не превышает допустимых суточных показателей, поэтому передозировки исключены.
Капсулы «Менсе» завершают рейтинг препаратов при менопаузе. Выступают в роли природного антидепрессанта. Не вызывают побочных реакций, исключая нарушения со стороны функций внутренних органов.
Выводы
Воспользовавшись рейтингом, каждый сможет выбрать лучшее негормональное средство, которое поможет справиться с приливами. Перед покупкой рекомендуется проконсультироваться с врачом, который посоветует как принимать таблетки.
Негормональные препараты нового поколения незаменимы на любом этапе климакса. В ТОПе представлены средства, разработанные преимущественно на основе растительных компонентов. Они заменяют ЗГТ, отличаясь отсутствием побочных реакций и противопоказаний. Единственный минус заключается в том, что действие наступает постепенно и менее выражено.
В ТОПе представлены средства, разработанные преимущественно на основе растительных компонентов. Они заменяют ЗГТ, отличаясь отсутствием побочных реакций и противопоказаний. Единственный минус заключается в том, что действие наступает постепенно и менее выражено.
Список литературы:
https://www.rlsnet.ru/mkb_index_id_6316.htm
https://www.vidal.by/patsientam/entsiklopediya/gynecology/menopauza.html
https://www.vidal.ru/encyclopedia/gynecology/menopauza
https://medum.ru/mkb-n95.1
Депрессия: Насколько эффективны антидепрессанты? — InformedHealth.org
Как и психотерапия, антидепрессанты являются ключевой частью лечения депрессии. Они направлены на облегчение симптомов и предотвращение возвращения депрессии.
Существуют разные мнения о том, насколько эффективны антидепрессанты в облегчении симптомов депрессии. Кто-то сомневается, что они хорошо работают, а кто-то считает их необходимым. Но, как и многие другие методы лечения, эти лекарства могут помочь в одних ситуациях и не помочь в других.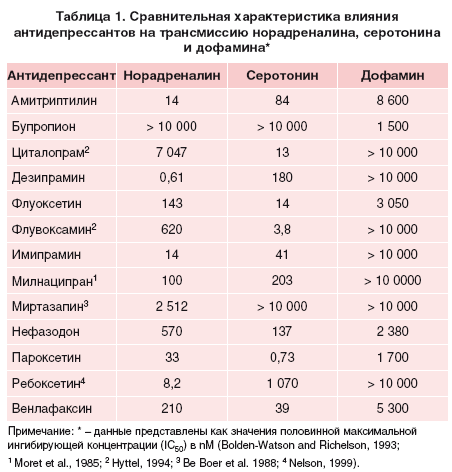 Они эффективны при умеренной, тяжелой и хронической депрессии, но, вероятно, не в легких случаях. Они также могут иметь побочные эффекты. Важно обсудить плюсы и минусы антидепрессантов с врачом.
Они эффективны при умеренной, тяжелой и хронической депрессии, но, вероятно, не в легких случаях. Они также могут иметь побочные эффекты. Важно обсудить плюсы и минусы антидепрессантов с врачом.
Основной целью лечения антидепрессантами является облегчение симптомов тяжелой депрессии, таких как чувство подавленности и истощения, и предотвращение их повторного появления. Они предназначены для того, чтобы вы снова почувствовали себя эмоционально стабильными и помогли вам следовать обычному распорядку дня. Их также принимают для облегчения таких симптомов, как беспокойство, тревога и проблемы со сном, а также для предотвращения суицидальных мыслей.
Эта информация касается использования лекарств для лечения наиболее распространенной формы депрессии, известной как униполярная депрессия. Варианты лечения маниакальной депрессии (биполярного расстройства) здесь не обсуждаются.
Какие антидепрессанты доступны?
Существуют различные лекарства для лечения депрессии. Их можно разделить на разные группы. Эта статья в основном о наиболее часто используемых антидепрессантах:
Их можно разделить на разные группы. Эта статья в основном о наиболее часто используемых антидепрессантах:
трициклические антидепрессанты (TCAS)
Селективный селективные ингибиторы серотонина (SSRIS)
селективные ингибиторы селективного серотонина.
Трициклические антидепрессанты существуют на рынке дольше всех.Они считаются антидепрессантами первого поколения. СИОЗС и СИОЗСН являются антидепрессантами второго поколения.
Следующие предписаны реже:
Антагонисты рецепторов адренергических альфа
Monoamine Oxidase (MAO) ингибиторы
селективный норадреналин регенерации ингибиторы
селективный норадреналин / дофамин повторно ингибиторы
Агонисты мелатониновых рецепторов и антагонисты серотониновых 5-HT2C рецепторов
зверобой.
Как действуют антидепрессанты?
Нервные клетки нашего мозга используют различные химические вещества для передачи сигналов. Несмотря на то, что известны не все детали, эксперты считают, что депрессия вызвана дисбалансом определенных химических мессенджеров (нейротрансмиттеров), таких как серотонин, что означает, что сигналы не могут правильно передаваться по нервам. Антидепрессанты направлены на увеличение доступности этих химических веществ. Различные препараты делают это по-разному.
Несмотря на то, что известны не все детали, эксперты считают, что депрессия вызвана дисбалансом определенных химических мессенджеров (нейротрансмиттеров), таких как серотонин, что означает, что сигналы не могут правильно передаваться по нервам. Антидепрессанты направлены на увеличение доступности этих химических веществ. Различные препараты делают это по-разному.
В чем заключается лечение?
Антидепрессанты обычно принимают ежедневно.Цель в первые несколько недель и месяцев — облегчить симптомы и, по возможности, избавиться от депрессии. Как только это будет достигнуто, лечение продолжают в течение как минимум четырех-девяти месяцев. Эта поддерживающая терапия необходима, чтобы предотвратить возвращение симптомов. Лекарство иногда принимают дольше, чтобы предотвратить рецидивы. Продолжительность лечения также зависит от того, как симптомы продолжают развиваться с течением времени и есть ли вероятность возвращения депрессии. Некоторые люди принимают антидепрессанты в течение многих лет.
При приеме антидепрессантов важно регулярно посещать врача. Там можно рассказать о том, улучшились ли симптомы и есть ли побочные эффекты. При необходимости доза будет скорректирована. Ни в коем случае нельзя уменьшать дозу или прекращать прием лекарства самостоятельно. Это может сделать таблетки менее эффективными или вызвать больше побочных эффектов.
К концу лечения дозу постепенно снижают в течение нескольких недель.У вас могут возникнуть временные проблемы со сном, тошнота или беспокойство после прекращения приема антидепрессантов. Эти симптомы особенно вероятны, если вы внезапно прекратите прием антидепрессантов. Иногда люди перестают принимать лекарства, как только начинают чувствовать себя лучше, но это увеличивает риск возвращения депрессии. В отличие от многих снотворных и седативных средств, антидепрессанты не вызывают физической зависимости или привыкания.
Насколько эффективно антидепрессанты облегчают симптомы?
Существует множество различных лекарств для лечения депрессии. Но трудно предсказать, насколько хорошо то или иное лекарство поможет человеку. Поэтому врачи часто сначала предлагают принять препарат, который они считают эффективным и относительно хорошо переносимым. Если это не помогает так сильно, как ожидалось, можно перейти на другое лекарство. Иногда приходится перепробовать несколько разных препаратов, прежде чем найдешь тот, который работает.
Но трудно предсказать, насколько хорошо то или иное лекарство поможет человеку. Поэтому врачи часто сначала предлагают принять препарат, который они считают эффективным и относительно хорошо переносимым. Если это не помогает так сильно, как ожидалось, можно перейти на другое лекарство. Иногда приходится перепробовать несколько разных препаратов, прежде чем найдешь тот, который работает.
Исследования показывают, что польза обычно зависит от тяжести депрессии: чем тяжелее депрессия, тем больше будет польза.Другими словами, антидепрессанты эффективны против хронической, умеренной и тяжелой депрессии. Они не помогают при легкой депрессии.
Различные антидепрессанты сравнивались во многих исследованиях. В целом, широко используемые трициклические антидепрессанты (СИОЗС и СИОЗСН) оказались одинаково эффективными. Исследования с участием взрослых с умеренной или тяжелой депрессией показали следующее:
Без антидепрессантов: от 20 до 40 из 100 человек, принимавших плацебо, заметили улучшение своих симптомов в течение шести-восьми недель.

С антидепрессантами: примерно от 40 до 60 из 100 человек, принимавших антидепрессанты, заметили улучшение своих симптомов в течение шести-восьми недель.
Другими словами, антидепрессанты улучшили симптомы примерно у 20 человек из 100.
Антидепрессанты также могут облегчать длительные симптомы хронического депрессивного расстройства (дистимии) и хронической депрессии и способствовать их полному исчезновению.
Антидепрессант может дать эффект уже через одну-две недели.Но для улучшения симптомов может потребоваться больше времени.
Депрессивные симптомы также можно лечить комбинацией двух препаратов. Это может привести к заметному улучшению. Некоторым людям может потребоваться много времени, чтобы лекарство начало помогать. У других людей все еще есть симптомы, даже после того, как они попробовали несколько разных лекарств. Затем вы можете обсудить с врачом другие возможные варианты лечения.
Насколько хорошо антидепрессанты предотвращают рецидивы?
Антидепрессанты обычно принимают в течение одного-двух лет, а иногда и дольше, для предотвращения рецидивов. Профилактика рецидивов может быть хорошей идеей для людей, у которых
Профилактика рецидивов может быть хорошей идеей для людей, у которых
уже было несколько рецидивов,
абсолютно хотят избежать рецидива или
Исследования с участием взрослых показали, что прием часто используемых антидепрессантов, таких как ТЦА, СИОЗС или СИОЗСН могут снизить риск рецидивов, но не могут полностью их предотвратить:
Без профилактического лечения: примерно у 50 из 100 человек, принимавших плацебо, возник рецидив в течение одного-двух лет.
С профилактическим лечением: Примерно у 23 из 100 человек, принимавших антидепрессант, в течение одного-двух лет возник рецидив.
Другими словами, прием антидепрессанта в течение длительного периода времени успешно предотвратил рецидив в среднем у 27 человек из 100.
Каковы побочные эффекты антидепрессантов?
Как и все лекарства, антидепрессанты могут иметь побочные эффекты. Более половины всех людей, принимающих антидепрессанты, имеют побочные эффекты. Обычно они возникают в течение первых нескольких недель лечения и реже в дальнейшем.
Обычно они возникают в течение первых нескольких недель лечения и реже в дальнейшем.
Считается, что некоторые из этих побочных эффектов являются прямым следствием воздействия лекарства на мозг и относительно схожи между различными лекарствами в одной группе. Примеры включают сухость во рту, головные боли, головокружение, беспокойство и сексуальные проблемы. Такие проблемы часто воспринимаются как побочные эффекты лекарств. Но некоторые из них могут быть вызваны самой депрессией.
Есть ли у кого-то побочные эффекты, какие побочные эффекты они имеют и как часто они возникают, зависит от препарата, используемой дозы и от того, начал ли человек его принимать только что или принимает в течение некоторого времени. И все по-разному реагируют на наркотики. Риск побочных эффектов увеличивается, если вы одновременно принимаете другие лекарства. Один из препаратов может усугубить побочные эффекты другого. Эти виды лекарственного взаимодействия распространены у пожилых людей и людей с хроническими заболеваниями, которые принимают несколько различных видов лекарств.
По этой причине важно тщательно обсудить плюсы и минусы различных лекарств со своим врачом.
Некоторые побочные эффекты более характерны для определенных препаратов:
СИОЗС чаще, чем трициклические антидепрессанты, вызывают диарею, головные боли, проблемы со сном и тошноту.
По сравнению с СИОЗС, трициклические антидепрессанты чаще вызывают проблемы со зрением, запор, головокружение, сухость во рту, дрожь и затрудненное мочеиспускание.
Побочные эффекты трициклических антидепрессантов часто хуже, чем у СИОЗС и СИОЗСН. Из-за этого все больше людей склонны прекращать прием трициклических антидепрессантов: исследования показали, что около 15 из 100 человек, принимавших трициклические антидепрессанты, сделали это, по сравнению с примерно 10 из 100 человек, принимавших СИОЗС. Существует также больший риск серьезных побочных эффектов при передозировке трициклических антидепрессантов.
Серьезные побочные эффекты
Антидепрессанты могут вызывать головокружение и неустойчивость, повышая риск падений и переломов костей, особенно у пожилых людей. Взаимодействие с другими лекарствами может увеличить этот риск.
Взаимодействие с другими лекарствами может увеличить этот риск.
У очень небольшого числа людей были проблемы с сердцем, эпилептические припадки или повреждение печени во время приема антидепрессантов. Считается, что это были редкие побочные эффекты антидепрессантов. Различные исследования показывают, что подростки чаще думают о самоубийстве (совершении самоубийства) при приеме СИОЗС или СИОЗСН, а также чаще пытаются покончить с собой. Из-за этого подростки должны чаще посещать своего врача или терапевта в начале лечения, чтобы можно было выявить любой риск самоубийства на ранней стадии.
На что следует обратить внимание при принятии решения о приеме антидепрессантов?
Выбор антидепрессантов зависит от таких факторов, как тяжесть симптомов. Другие аспекты также могут сыграть роль в решении:
Собираетесь ли вы на психотерапию или планируете?
Принимали ли Вы раньше антидепрессанты и помогали ли они?
Насколько плохи, по вашему мнению, потенциальные побочные эффекты по сравнению с возможными преимуществами?
Вопрос о побочных эффектах также может быть ключевым при выборе препарата: Некоторые люди могут быть более заинтересованы в том, чтобы избежать проблем с пищеварением. Другие могут предпочесть избегать головокружения, снижения полового влечения или проблем с эрекцией.
Другие могут предпочесть избегать головокружения, снижения полового влечения или проблем с эрекцией.
Применять антидепрессанты имеет смысл только при правильном диагнозе. Специалисты считают, что некоторым людям антидепрессанты назначают без надобности. Тот факт, что сегодня гораздо больше людей принимают антидепрессанты, говорит о том, что это правда. Иногда их уже назначают при более легких симптомах, хотя неясно, помогают ли они при легкой депрессии.
Но по-прежнему важно убедиться, что тяжелая депрессия правильно диагностируется и лечится.Здесь могут помочь антидепрессанты, а для некоторых людей это единственный способ вернуться к повседневной жизни или начать ходить на психотерапию.
Источники
- 9
- 9002
IQвиг Информация о здоровье написана с целью помощи люди понимают преимущества и недостатки основных вариантов лечения и здоровья услуги по уходу.

Поскольку IQWiG является немецким институтом, некоторая информация, представленная здесь, относится к Немецкая система здравоохранения. Пригодность любого из описанных вариантов у конкретного случае можно определить, поговорив с врачом. Мы не предлагаем индивидуальные консультации.
Наша информация основана на результатах качественных исследований. Это написано команда медицинских работников, ученых и редакторов, а также проверенных внешними экспертами. Ты сможешь найти подробное описание того, как наша медицинская информация создается и обновляется в наши методы.
Могут ли они работать на меня?
Антидепрессанты — распространенный способ лечения депрессии. Но они работают немного по-разному для всех. Это может заставить вас задуматься, будут ли они работать на вас.
На кого лучше всего действуют антидепрессанты?
Однозначного ответа нет. Но появляется все больше доказательств того, что антидепрессанты работают лучше, чем плацебо («поддельный» препарат) для большинства тех, кто их принимает.
Но вы, возможно, слышали, что они более эффективны для людей с серьезной депрессией.
Джерард Санакора, доктор медицинских наук, директор Йельской программы исследования депрессии, говорит, что в исследовании есть нюансы. Он говорит, что дело не столько в том, что антидепрессанты лучше действуют на людей с серьезной депрессией.
«Дело в том, что антидепрессанты работают лучше, чем плацебо, что немного сложно», — говорит он. «Это означает, что с менее тяжелой депрессией плацебо работает чертовски хорошо».
Другой способ взглянуть на это так: если у вас легкие симптомы, вы, вероятно, поправитесь с помощью других вариантов.
«Возможно, сначала стоит попробовать немедикаментозное лечение, такое как когнитивно-поведенческая терапия [КПТ] или другая психотерапия», — говорит Санакора.
Правильный выбор антидепрессанта
Эксперты обычно не знают, какой из них будет работать лучше всего.
«Было бы неплохо, если бы у нас был простой алгоритм, показывающий, что этот более эффективен, чем тот», — говорит Санакора. «Но у нас этого нет. Это действительно переменная».
«Но у нас этого нет. Это действительно переменная».
С учетом сказанного он говорит, что большинство врачей обычно придерживаются одного и того же подхода.
Ваше лечение может включать:
Селективные ингибиторы обратного захвата серотонина (СИОЗС). Они работают с одним нейротрансмиттером — химическим мессенджером между нервными клетками — серотонином. СИОЗС — это обычно первое, что попробует ваш врач. Есть несколько причин, почему.
«Они, как правило, хорошо переносятся, и это недорогое лекарство», — говорит Санакора. «И у нас также есть данные о безопасности за 30 лет».
Обычно используемые SSRIS включают в себя:
- CitaloPram (Celexa)
- Escitalopram (LexAPro)
- Флуоксетин (Prozac)
- Серралин (Zoloft)
- Sertraline (Zoloft)
Селективный серотонин и ингибиторы обратного захвата Norepinephrine (SNRIS). Воздействуют на два нейротрансмиттера: серотонин и норадреналин. Санакора говорит, что есть некоторые доказательства того, что СИОЗСН могут быть более эффективными, чем СИОЗС для некоторых людей.
Санакора говорит, что есть некоторые доказательства того, что СИОЗСН могут быть более эффективными, чем СИОЗС для некоторых людей.
«Но моя способность предсказывать это для одного человека не очень сильна», — говорит он.
Возможно, у вас не возникнет проблем с SNRI. Но Санакора говорит, что они обычно являются вторым выбором, потому что они, как правило, имеют больше побочных эффектов.
Обычно используются СНрис для депрессии включают в себя:
- desvenlafaxine (pristiq)
- Дюлоссетин (Cymbalta)
- Левомилнаципран (Фетзима)
- Venlafaxine (Effexor XR)
Add-on Наркотики или другие терапии. Приблизительно от 30% до 50% людей с депрессией могут сохранять симптомы, когда они принимают антидепрессанты. Если это произойдет с вами, Санакора говорит, что ваш врач может одновременно назначить вам другой вид лечения. Это могут быть такие вещи, как:
- Атипичные антидепрессанты
- Атипичные нейролептики
- Кетаминовый назальный спрей (анестетик)
Другим вариантом являются методы стимуляции мозга, в том числе:
- Электрошоковая терапия (ECT) ТМС)
- Стимуляция блуждающего нерва (ВНС)
Циклические антидепрессанты. Это самые старые антидепрессанты. У них гораздо больше побочных эффектов, чем у новых лекарств. Ваш врач может предложить их, если другие методы лечения не работают.
Это самые старые антидепрессанты. У них гораздо больше побочных эффектов, чем у новых лекарств. Ваш врач может предложить их, если другие методы лечения не работают.
Вопросы к врачу
Данеш Алам, доктор медицинских наук, специалист в области психиатрии в Northwestern Medicine, говорит, что «депрессия — одно из самых сложных заболеваний, с которыми мы сталкиваемся в медицине». И чтобы получить наилучшее лечение, важно быть на одной волне со своим врачом.
«Вы должны достичь целевой дозы и определить целевые симптомы», — говорит он.«Часто на эти детали не обращают внимания. Тогда это становится несоответствием ожиданиям. Это то, что я бы назвал терапевтической неудачей, а не лекарственной неудачей».
Вот несколько вопросов об антидепрессантах, которые вы, возможно, захотите задать:
- Когда я должен увидеть результаты?
- Почувствую ли я себя хуже, прежде чем почувствую себя лучше?
- Как часто мне следует наблюдаться?
- Каковы общие побочные эффекты? Как долго они длятся?
- Как узнать, серьезны ли побочные эффекты?
- Что произойдет, если лекарство перестанет действовать?
- Как долго я должен принимать антидепрессанты?
- Как узнать, нужно ли мне изменить дозу?
- Что такое немедикаментозное лечение депрессии?
- Каков план прекращения приема препарата?
Не сдавайтесь слишком рано
Хотеть быстро почувствовать себя лучше — это нормально. Но для того, чтобы антидепрессанты подействовали, нужно время. Эксперты точно не знают, почему. Одна из теорий состоит в том, что этим препаратам могут потребоваться дни или недели, чтобы изменить химические пути, ведущие к депрессии. Нам нужно больше исследований, чтобы знать наверняка.
Но для того, чтобы антидепрессанты подействовали, нужно время. Эксперты точно не знают, почему. Одна из теорий состоит в том, что этим препаратам могут потребоваться дни или недели, чтобы изменить химические пути, ведущие к депрессии. Нам нужно больше исследований, чтобы знать наверняка.
Хотя все люди разные, может пройти в среднем 4-6 недель, прежде чем вы заметите значительные улучшения.
«Но чтобы действительно сказать, что лекарство не работает, нужно дать ему 8 недель», — говорит Алам.
И не сдавайтесь, если ваш первый антидепрессант вам не подходит.Исследования показывают, что ваши шансы на успех возрастают, если вы пробуете более одного подхода.
«Важным сообщением является то, что лекарства и лечение депрессии эффективны», — говорит Алам. «Но вы должны продолжать заниматься лечением».
Эффективность антидепрессантов: доказательный миф, созданный на основе тысяч рандомизированных испытаний? | Философия, этика и гуманитарные науки в медицине
Немногие лекарства были такими успешными блокбастерами, как класс антидепрессантов. В совокупности сотни миллионов пациентов принимали эти лекарства, а селективные ингибиторы обратного захвата серотонина (СИОЗС) и препараты нового поколения, в частности, пользовались огромной популярностью.Антидепрессанты отражают одно из основных проявлений медикализации современного общества [1]. В 2006 г. 5 из 35 наиболее продаваемых в США препаратов были антидепрессантами, и объем продаж каждого из них в этом году составил 1,08–2,25 млрд долл. (табл. 1) [2]. Около 30% стоимости депрессии в США (80 млрд долларов в год) приходится на расходы на лекарства [3].
В совокупности сотни миллионов пациентов принимали эти лекарства, а селективные ингибиторы обратного захвата серотонина (СИОЗС) и препараты нового поколения, в частности, пользовались огромной популярностью.Антидепрессанты отражают одно из основных проявлений медикализации современного общества [1]. В 2006 г. 5 из 35 наиболее продаваемых в США препаратов были антидепрессантами, и объем продаж каждого из них в этом году составил 1,08–2,25 млрд долл. (табл. 1) [2]. Около 30% стоимости депрессии в США (80 млрд долларов в год) приходится на расходы на лекарства [3].
Это не эпидемия, для которой не хватает доказательных материалов, подтверждающих ее.Немногие лекарства прошли такую длинную цепочку двойных слепых плацебо-контролируемых испытаний, чтобы продемонстрировать их эффективность и пройти, казалось бы, строгое одобрение регулирующих органов. Рандомизированная литература по антидепрессантам, по-видимому, является одной из самых богатых доказательной базой данных. В то время как для большей части медицинских вмешательств у нас никогда не проводилось клинических испытаний или проводилось очень мало клинических испытаний, для антидепрессантов их, вероятно, более тысячи. PsiTri, онлайн-библиотека клинических испытаний психических расстройств [4], содержит 4058 клинических испытаний депрессии, и большая часть из них (более четверти от общего числа, точное количество зависит от критериев приемлемости) относится к рандомизированным испытаниям антидепрессантов. .Систематический обзор испытаний СИОЗС по различным показаниям до 2003 г. [5] выявил 702 испытания (411 сравнений между СИОЗС и плацебо, 220 сравнений между СИОЗС и трициклическими антидепрессантами и 159 сравнений между СИОЗС и активной терапией, отличной от плацебо или трициклических антидепрессантов). В другом обзоре [6] 12 антидепрессантов, в котором участвовали только двойные слепые плацебо-контролируемые исследования по различным показаниям у взрослых, спонсоры предоставили FDA данные о 406 исследованиях с участием примерно 100 000 рандомизированных пациентов.
В то время как для большей части медицинских вмешательств у нас никогда не проводилось клинических испытаний или проводилось очень мало клинических испытаний, для антидепрессантов их, вероятно, более тысячи. PsiTri, онлайн-библиотека клинических испытаний психических расстройств [4], содержит 4058 клинических испытаний депрессии, и большая часть из них (более четверти от общего числа, точное количество зависит от критериев приемлемости) относится к рандомизированным испытаниям антидепрессантов. .Систематический обзор испытаний СИОЗС по различным показаниям до 2003 г. [5] выявил 702 испытания (411 сравнений между СИОЗС и плацебо, 220 сравнений между СИОЗС и трициклическими антидепрессантами и 159 сравнений между СИОЗС и активной терапией, отличной от плацебо или трициклических антидепрессантов). В другом обзоре [6] 12 антидепрессантов, в котором участвовали только двойные слепые плацебо-контролируемые исследования по различным показаниям у взрослых, спонсоры предоставили FDA данные о 406 исследованиях с участием примерно 100 000 рандомизированных пациентов.
Формально неоднократно демонстрировались статистически значимые преимущества, и медицинская литература наводнена несколькими сотнями «положительных» испытаний, как до, так и после утверждения. Теоретически это прототип доказательной медицины, где лечение проходит тщательное рандомизированное тестирование и пользуется огромным успехом как на арене клинической науки, так и на рынке.
Эта картина блаженства недавно была подвергнута сомнению в результате двух крупных хорошо проведенных метаанализов [7, 8].В этом обзоре я сначала исследую, что было обнаружено в ходе этих метаанализов, и каковы некоторые возможные ограничения этих исследований. Затем я пытаюсь проанализировать, из каких компонентов сложилась, казалось бы, основанная на фактических данных картина того, что антидепрессанты настолько эффективны, и почему эта картина может оказаться проблематичной при ближайшем рассмотрении. В конце концов я попытаюсь выяснить, широко ли показаны антидепрессанты для лечения депрессии и неэтично ли уничтожать живой миф. Наконец, я делаю несколько предложений о том, как мы можем получить соответствующие доказательства по этим наркотикам.
Наконец, я делаю несколько предложений о том, как мы можем получить соответствующие доказательства по этим наркотикам.
Расстроены метаанализами
Выборочная отчетность
В первом метаанализе использовались данные, представленные в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) по 12 антидепрессантам, одобренным в период с 1987 по 2004 год [7]. Это были бупропион SR (Wellbutrin SR, GlaxoSmithKline), циталопрам (Celexa, Forest), дулоксетин (Cymbalta, Eli Lilly), эсциталопрам (Lexapro, Forest), флуоксетин (Prozac, Eli Lilly), миртазапин (Remeron, Organon), нефазодон ( Serzone, Bristol-Meyers Squibb), пароксетин (Paxil CR, GlaxoSmithKline), сертралин (Zoloft, Pfizer), венлафаксин (Effexor, Wyeth) и венлафаксин XR (Effexor XR, Wyeth).Основное преимущество использования данных, представленных в FDA, заключается в том, что они включают все испытания, зарегистрированные каждой компанией в качестве доказательства в поддержку разрешения на продажу или изменения маркировки. Эта регистрация позволяет узнать обо всех этих испытаниях, независимо от того, были они в конечном итоге опубликованы или нет. Кроме того, процесс регулятивной проверки таков, что меньше возможностей для манипулирования анализами и искажения результатов в данных, введенных в таблицы реестра FDA.
Эта регистрация позволяет узнать обо всех этих испытаниях, независимо от того, были они в конечном итоге опубликованы или нет. Кроме того, процесс регулятивной проверки таков, что меньше возможностей для манипулирования анализами и искажения результатов в данных, введенных в таблицы реестра FDA.
Мета-аналитики обнаружили 74 подходящих исследования, зарегистрированных FDA, с участием 12 564 пациентов.Среди них треть (n = 26 испытаний [31%] с 3449 пациентами) осталась неопубликованной. FDA определило, что половина зарегистрированных испытаний (38 из 74) выявила статистически значимые преимущества антидепрессанта («положительные» испытания). Все, кроме одного, из этих испытаний были опубликованы в журналах. И наоборот, из другой половины испытаний (36/74), которые FDA сочло «отрицательными», каждое третье было опубликовано как «отрицательный» результат; были опубликованы еще 11 испытаний, но результаты были представлены таким образом, чтобы казаться «положительными», а 22 «отрицательных» испытания замалчивались и никогда не публиковались в литературе.
Мета-аналитики изучили расчетную эффективность этих препаратов при объединении данных из отчетов FDA и при объединении данных из опубликованной литературы. Для всех препаратов в опубликованной литературе величина эффекта завышена. Инфляция колебалась от 11% до 69% и в среднем составила 32%. Данные FDA предполагают, что эти агенты имели небольшие, скромные преимущества (стандартизированный размер эффекта [ES] = 0,31 в среднем). И наоборот, для 4 из 12 агентов, если бы кто-то случайно провел только метаанализ опубликованных данных, суммарный результат предполагал бы клинически значимую эффективность (ES>0.5). Это не было верно для любого агента на основе более полных данных FDA.
Лечение и эффект плацебо в зависимости от исходной степени тяжести
Во втором метаанализе PLoS Medicine также использовались данные, представленные в FDA по 6 антидепрессантам нового поколения, и в итоге использовалась информация о четырех из них (5 исследований по флуоксетин, 4 — венлафаксин, 8 — нефазодон и 16 — пароксетин) [8]. Для двух других препаратов (сертралин и циталопрам) некоторые испытания были просто зарегистрированы даже в базах данных FDA как имеющие незначительные результаты.В отличие от другого мета-анализа, исследователи этого мета-анализа не хотели приписывать данные, когда была такая отсутствующая информация.
Для двух других препаратов (сертралин и циталопрам) некоторые испытания были просто зарегистрированы даже в базах данных FDA как имеющие незначительные результаты.В отличие от другого мета-анализа, исследователи этого мета-анализа не хотели приписывать данные, когда была такая отсутствующая информация.
В ходе метаанализа PLoS Medicine был задан вопрос: существует ли связь между исходной тяжестью депрессии и разницей в эффективности между лекарством и плацебо? Мета-регрессионный анализ выявил такую взаимосвязь. Различия между препаратом и плацебо, как правило, были небольшими, но они увеличивались с увеличением исходной тяжести.Мета-аналитики использовали предыдущий консенсус [9], чтобы предположить, что клинически значимое различие должно составлять не менее 3 баллов по шкале Гамильтона или ES>0,50. Разница между препаратом и плацебо стала достаточно большой, чтобы иметь клиническое значение только в небольшой части групп пациентов с тяжелой депрессией (исходный балл, превышающий 28 в исследуемой популяции). Даже у этих пациентов с тяжелой депрессией разница между препаратом и плацебо заключалась в том, что плацебо становилось менее эффективным; не было доказательств того, что антидепрессанты стали более эффективными.Авторы пришли к выводу, что большая часть пользы от антидепрессантов дублируется эффектом плацебо. Это заключение было предложено также на основе более раннего метаанализа [9]. Более того, в текущем метаанализе добавлено понимание того, что эти препараты могут иметь клиническое применение только у людей с тяжелой депрессией, что составляет незначительное меньшинство по сравнению с огромным населением, принимающим антидепрессанты в настоящее время. Даже у нескольких пациентов с крайне депрессивным состоянием конечная польза была обусловлена недостаточной реакцией на плацебо, а не повышенной реакцией на антидепрессанты.
Даже у этих пациентов с тяжелой депрессией разница между препаратом и плацебо заключалась в том, что плацебо становилось менее эффективным; не было доказательств того, что антидепрессанты стали более эффективными.Авторы пришли к выводу, что большая часть пользы от антидепрессантов дублируется эффектом плацебо. Это заключение было предложено также на основе более раннего метаанализа [9]. Более того, в текущем метаанализе добавлено понимание того, что эти препараты могут иметь клиническое применение только у людей с тяжелой депрессией, что составляет незначительное меньшинство по сравнению с огромным населением, принимающим антидепрессанты в настоящее время. Даже у нескольких пациентов с крайне депрессивным состоянием конечная польза была обусловлена недостаточной реакцией на плацебо, а не повышенной реакцией на антидепрессанты.
Ограничения в мета-анализах
Оба мета-анализа имеют некоторые ограничения. Многие другие испытания проводятся после утверждения или вне процесса утверждения FDA. Более того, в реестры разрешенных препаратов не включены антидепрессанты, которые, возможно, проходили клинические испытания в США, но не попали в них (предположительно из-за более «отрицательных» результатов), хотя прошли и были одобрены в других странах, напр. флуоксамин, милнаципран или миансерин. Среди испытанных в США антидепрессантов только самые «повезло» с большим ЭС попали в FDA и получили одобрение.Отсутствие всеобъемлющей глобальной базы данных является серьезным недостатком, поскольку мы можем упустить испытания, проведенные в странах, где общие результаты для конкретного агента были не очень многообещающими или откровенно отрицательными. На рисунке 1 показано простое моделирование: предположим, что лекарство тестируется в 40 странах, и в каждой стране проводится 5 небольших испытаний для целей лицензирования. Предположим, что в среднем препарат имеет истинный эффект, который мал (ES = 0,20). Ожидается, что каждое из совершенно беспристрастных исследований обнаружит в среднем ES = 0.
Более того, в реестры разрешенных препаратов не включены антидепрессанты, которые, возможно, проходили клинические испытания в США, но не попали в них (предположительно из-за более «отрицательных» результатов), хотя прошли и были одобрены в других странах, напр. флуоксамин, милнаципран или миансерин. Среди испытанных в США антидепрессантов только самые «повезло» с большим ЭС попали в FDA и получили одобрение.Отсутствие всеобъемлющей глобальной базы данных является серьезным недостатком, поскольку мы можем упустить испытания, проведенные в странах, где общие результаты для конкретного агента были не очень многообещающими или откровенно отрицательными. На рисунке 1 показано простое моделирование: предположим, что лекарство тестируется в 40 странах, и в каждой стране проводится 5 небольших испытаний для целей лицензирования. Предположим, что в среднем препарат имеет истинный эффект, который мал (ES = 0,20). Ожидается, что каждое из совершенно беспристрастных исследований обнаружит в среднем ES = 0. 20 и может быть некоторая изменчивость. Мы можем исследовать ситуации с различными уровнями изменчивости вокруг этого среднего, что соответствует стандартным отклонениям 0,20, 0,40 и 0,60. Чем меньше испытаний и чем больше разнообразие популяций и реакции на лекарство, тем больше ожидаемая вариабельность около среднего значения ES = 0,20. Предположим, что лекарство одобрено только в странах, где 5 испытаний показывают средний показатель ES не менее 0,20. Ожидается, что это произойдет примерно в половине стран. На рисунке 1 показано, каковы средние оценки ES в исследованиях, зарегистрированных в странах, где препарат был одобрен: ES заметно завышена.Аналогичные соображения применимы, если мы рассматриваем не только многие страны, но и многие лекарства, испытанные во многих странах.
20 и может быть некоторая изменчивость. Мы можем исследовать ситуации с различными уровнями изменчивости вокруг этого среднего, что соответствует стандартным отклонениям 0,20, 0,40 и 0,60. Чем меньше испытаний и чем больше разнообразие популяций и реакции на лекарство, тем больше ожидаемая вариабельность около среднего значения ES = 0,20. Предположим, что лекарство одобрено только в странах, где 5 испытаний показывают средний показатель ES не менее 0,20. Ожидается, что это произойдет примерно в половине стран. На рисунке 1 показано, каковы средние оценки ES в исследованиях, зарегистрированных в странах, где препарат был одобрен: ES заметно завышена.Аналогичные соображения применимы, если мы рассматриваем не только многие страны, но и многие лекарства, испытанные во многих странах.
Ожидаемое среднее значение и диапазон средней величины эффекта (ES) для исследований в странах, где лекарство одобрено, когда истинная средняя эффективность ES = 0,20, а стандартное отклонение (SD) расчетной ES в испытаниях составляет 0,20, 0,40 и 0,60. В расчетах предполагается, что испытания имеют одинаковый размер и вес. В каждой из трех настроек было смоделировано сорок пакетов утверждения с 5 испытаниями в каждом, и данные показывают ES в успешных пакетах (тех, где средний ES составляет не менее 0.20).
В расчетах предполагается, что испытания имеют одинаковый размер и вес. В каждой из трех настроек было смоделировано сорок пакетов утверждения с 5 испытаниями в каждом, и данные показывают ES в успешных пакетах (тех, где средний ES составляет не менее 0.20).
Даже если сосредоточиться на исследованиях, зарегистрированных FDA, их данные не обязательно полностью беспристрастны. Врожденные предубеждения в дизайне исследования и анализе не могут быть исправлены простой регистрацией. Сбор данных, арбитраж измерений и результатов, а также несколько вариантов анализа оставляют место для избирательности и представления более оптимальных выводов — даже в отношении результатов, зарегистрированных FDA. Во-вторых, даже эти данные оказываются неполными в важных деталях. Это убедительно продемонстрировано значительным количеством исследований, которые были просто зарегистрированы как имеющие «отрицательные» результаты без дополнительных подробностей о размерах эффекта, а также дополнительной отсутствующей информацией, которую мета-аналитики должны были использовать даже для данных, зарегистрированных FDA. В-третьих, в этих испытаниях не было доступной информации на индивидуальном уровне, а сбор данных и оценка результатов и измерений оставались вне досягаемости метааналитиков. Для значительной части пациентов, которые не завершили исследования, обычно применялись методы переноса последнего наблюдения (LOCF), но они имеют ограничения и могут привести к переоценке эффектов лечения в некоторых обстоятельствах [10].
В-третьих, в этих испытаниях не было доступной информации на индивидуальном уровне, а сбор данных и оценка результатов и измерений оставались вне досягаемости метааналитиков. Для значительной части пациентов, которые не завершили исследования, обычно применялись методы переноса последнего наблюдения (LOCF), но они имеют ограничения и могут привести к переоценке эффектов лечения в некоторых обстоятельствах [10].
Все эти ограничения, скорее всего, привели к завышению стоимости лечения, хотя существует значительная неопределенность в отношении точной систематической ошибки.Следует отметить, что в метаанализе PLoS Medicine [8] была отмечена асимметрия графика воронки, т.е. небольшие испытания имели больший эффект, чем более крупные испытания. Асимметрия графика воронки обычно считается признаком предвзятости публикации (небольшие «отрицательные» испытания остаются неопубликованными), но это явно вводящее в заблуждение упрощение [11]. Здесь систематическая ошибка публикации теоретически невозможна для данных, зарегистрированных FDA. Авторы приписали асимметрию путанице из-за более высоких показателей тяжести в небольших исследованиях [8].Однако альтернативное объяснение заключается в том, что даже для испытаний, зарегистрированных FDA, результаты все еще могут быть предвзятыми. Исключение или включение конкретных пациентов и данных из-за сомнительных критериев приемлемости или измерений серого, выбор методов условного исчисления, использование или нет или корректировки, а также выборочное сообщение результатов позволяют манипулировать оценкой размера эффекта. В небольших испытаниях такое же количество манипуляций будет увеличивать размер эффекта больше, чем в больших испытаниях, другими словами, вибрация размера эффекта больше [12, 13].Процесс пересмотра FDA, конечно, снизит аналитическую гибкость, но оценка депрессии предполагает нечеткие результаты, а анализы не высечены в камне. В целом, во всяком случае, ожидание этих предубеждений еще больше усиливает сообщение о том, что антидепрессанты менее эффективны, чем предполагалось.
Авторы приписали асимметрию путанице из-за более высоких показателей тяжести в небольших исследованиях [8].Однако альтернативное объяснение заключается в том, что даже для испытаний, зарегистрированных FDA, результаты все еще могут быть предвзятыми. Исключение или включение конкретных пациентов и данных из-за сомнительных критериев приемлемости или измерений серого, выбор методов условного исчисления, использование или нет или корректировки, а также выборочное сообщение результатов позволяют манипулировать оценкой размера эффекта. В небольших испытаниях такое же количество манипуляций будет увеличивать размер эффекта больше, чем в больших испытаниях, другими словами, вибрация размера эффекта больше [12, 13].Процесс пересмотра FDA, конечно, снизит аналитическую гибкость, но оценка депрессии предполагает нечеткие результаты, а анализы не высечены в камне. В целом, во всяком случае, ожидание этих предубеждений еще больше усиливает сообщение о том, что антидепрессанты менее эффективны, чем предполагалось.
Более серьезное ограничение связано с использованием методов метарегрессии в метаанализе PLoS Medicine . В основном анализе использовалась метарегрессия с фиксированными эффектами, и только во вторичном анализе использовался подход со смешанными эффектами.Последнее, которое может быть более подходящим, чем фиксированные эффекты [14], дало менее убедительные результаты. Мета-регрессионное моделирование может быть предвзятым [15]. Когда испытания имеют лишь небольшие различия в средних значениях серьезности (как в этом случае), на наклон членов регрессии могут влиять выбросы и проблемы с кредитным плечом. Наиболее важное ограничение проистекает из экологической ошибки [16, 17]. Регрессия использовала в качестве модерирующей переменной среднюю исходную тяжесть депрессии в каждой группе участников в каждой группе исследования.Однако это прокси, который не одинаково хорошо представляет всех участников. Например, средний исходный балл может составлять 28, но сюда могут входить пациенты с баллами 17, 27, 32 и 36. Отношение могло бы быть другим, если бы данные можно было проанализировать для отдельных пациентов. Это означает, что хотя чистая эффективность (отличие препарата от плацебо), по-видимому, увеличивалась с увеличением средней степени тяжести, в конкретном испытании эффективность могла снижаться с увеличением степени тяжести.Экологическое заблуждение является основной причиной, по которой мета-регрессионный анализ со средним значением по группе воспринимается скептически [17].
Отношение могло бы быть другим, если бы данные можно было проанализировать для отдельных пациентов. Это означает, что хотя чистая эффективность (отличие препарата от плацебо), по-видимому, увеличивалась с увеличением средней степени тяжести, в конкретном испытании эффективность могла снижаться с увеличением степени тяжести.Экологическое заблуждение является основной причиной, по которой мета-регрессионный анализ со средним значением по группе воспринимается скептически [17].
Наконец, метаанализ PLoS Medicine описывает конец спектра тяжести в проанализированных исследованиях как пациентов, которые находятся в «самой крайней депрессии» или, альтернативно, в «очень тяжелой» депрессии. Фактически, «очень тяжелая» депрессия соответствует пациентам с еще более тяжелым депрессивным статусом, в первую очередь тем, кто госпитализирован из-за большой депрессии.На самом деле, проанализированные нормативные испытания, как правило, избегали включения госпитализированных пациентов с действительно настолько тяжелой депрессией, потому что эти новые препараты уже на раннем этапе показали свою неэффективность — или, по крайней мере, менее эффективны, чем старые препараты — у таких пациентов.
Понимание построения мифа об эффективности антидепрессантов
Признавая эти предостережения, уроки, которые мы извлекаем из этих мета-анализов и из предыдущей литературы по антидепрессантам, показывают нам, что есть много компонентов, которые помогли создать впечатление, что антидепрессанты очень эффективен и достоин того, чтобы быть настолько популярным среди населения в целом.
Статистическая и клиническая значимость
Типичное испытание в области антидепрессантов представляет собой небольшое исследование с участием от нескольких десятков до нескольких сотен участников. Тем не менее, в этих испытаниях использовались исходы, позволяющие выявить формально статистически значимые различия между сравниваемыми группами даже при таких малых размерах выборки. Типичным выбором являются шкалы депрессии, такие как рейтинговая шкала депрессии Гамильтона. Такие непрерывные исходы могут показывать формально статистически значимые результаты (p < 0.05) даже для небольших и тривиальных различий. Статистическую значимость путают с клинической значимостью. Согласно консенсусу Национального института клинического мастерства (NICE), для достижения клинически значимого эффекта необходима разница не менее 3 баллов по шкале Гамильтона или, что эквивалентно, ES = 0,50 [9]. Тем не менее, результаты нескольких одиночных исследований со статистически значимыми результатами и результаты практически всех мета-анализов со статистически значимыми результатами 90 383 исключают 90 384, что и ES = 0.50 может быть присвоено антидепрессантами, когда мы изучаем 95% доверительные интервалы эффектов. Здесь следует признать, что в пороге ES = 0,50 нет ничего абсолютного, и некоторые исследователи могут не согласиться с этим порогом. Обычно предлагаемые в литературе пороги для малых, средних и больших эффектов для непрерывных исходов составляют 0,2, 0,5 и 0,8 стандартных отклонения, но даже это является произвольным [18].
Статистическую значимость путают с клинической значимостью. Согласно консенсусу Национального института клинического мастерства (NICE), для достижения клинически значимого эффекта необходима разница не менее 3 баллов по шкале Гамильтона или, что эквивалентно, ES = 0,50 [9]. Тем не менее, результаты нескольких одиночных исследований со статистически значимыми результатами и результаты практически всех мета-анализов со статистически значимыми результатами 90 383 исключают 90 384, что и ES = 0.50 может быть присвоено антидепрессантами, когда мы изучаем 95% доверительные интервалы эффектов. Здесь следует признать, что в пороге ES = 0,50 нет ничего абсолютного, и некоторые исследователи могут не согласиться с этим порогом. Обычно предлагаемые в литературе пороги для малых, средних и больших эффектов для непрерывных исходов составляют 0,2, 0,5 и 0,8 стандартных отклонения, но даже это является произвольным [18].
Дизайн исследования и отбор исследуемых групп
Индустрия рандомизированных испытаний антидепрессантов за многие годы создала длинную цепочку практик и «стандартов» дизайна, направленных на максимизацию шансов на получение большей пользы от данных лекарств. Эти методы и стандарты включают, помимо прочего, использование плацебо-контроля, подготовительные периоды плацебо и набор критериев исключения для набранных участников.
Эти методы и стандарты включают, помимо прочего, использование плацебо-контроля, подготовительные периоды плацебо и набор критериев исключения для набранных участников.
Плацебо-контроль, конечно же, диктуется регулирующими органами, и для этого есть серьезные основания. Эмпирические данные, даже до мета-анализов, обсуждавшихся выше, неоднократно показывали, что эффект плацебо при депрессивных симптомах велик, вариабелен и, по-видимому, усиливается в более поздних исследованиях [19].Однако это также порождает парадокс: несмотря на то, что мы признаем, одобряем и массово продаем препараты, которые считаем более эффективными, чем плацебо, мы продолжаем проводить испытания, требующие, чтобы некоторые участники принимали то, что мы считаем неэффективным лечением [20]. . В качестве компромисса в некоторых исследованиях пациентов рандомизируют в соотношении 2:1 или даже 3:1, 4:1 и 5:1 в группу активного препарата и плацебо, что противоречит принципу равновесия, который должен пронизывать этику проведения клинических испытаний. Очевидно, что плацебо-контролируемые исследования имеют больше шансов продемонстрировать большую пользу с точки зрения абсолютных эффектов; непосредственные сравнения обычно показывают отсутствие или очень небольшие различия в общей эффективности одного антидепрессанта по сравнению с другим, независимо от того, используются ли старые или новые препараты [21–23].Например, тщательный систематический обзор флуоксетина по сравнению с другими антидепрессантами пришел к выводу, что даже если в некоторых сравнениях были замечены некоторые номинально значимые результаты, «клиническое значение этих различий неясно, и нельзя сделать никаких окончательных выводов для клинической практики» [21]. .
Очевидно, что плацебо-контролируемые исследования имеют больше шансов продемонстрировать большую пользу с точки зрения абсолютных эффектов; непосредственные сравнения обычно показывают отсутствие или очень небольшие различия в общей эффективности одного антидепрессанта по сравнению с другим, независимо от того, используются ли старые или новые препараты [21–23].Например, тщательный систематический обзор флуоксетина по сравнению с другими антидепрессантами пришел к выводу, что даже если в некоторых сравнениях были замечены некоторые номинально значимые результаты, «клиническое значение этих различий неясно, и нельзя сделать никаких окончательных выводов для клинической практики» [21]. .
Использование начального плацебо исключает пациентов, которые демонстрируют хороший ответ на плацебо в течение короткого периода времени до участия в надлежащем испытании. Теоретически это может увеличить разницу между препаратом и плацебо у пациентов, которые в конечном итоге будут включены в исследование, если хороший ответ на плацебо в начальном периоде коррелирует с хорошим ответом на плацебо также в течение более длительного периода наблюдения.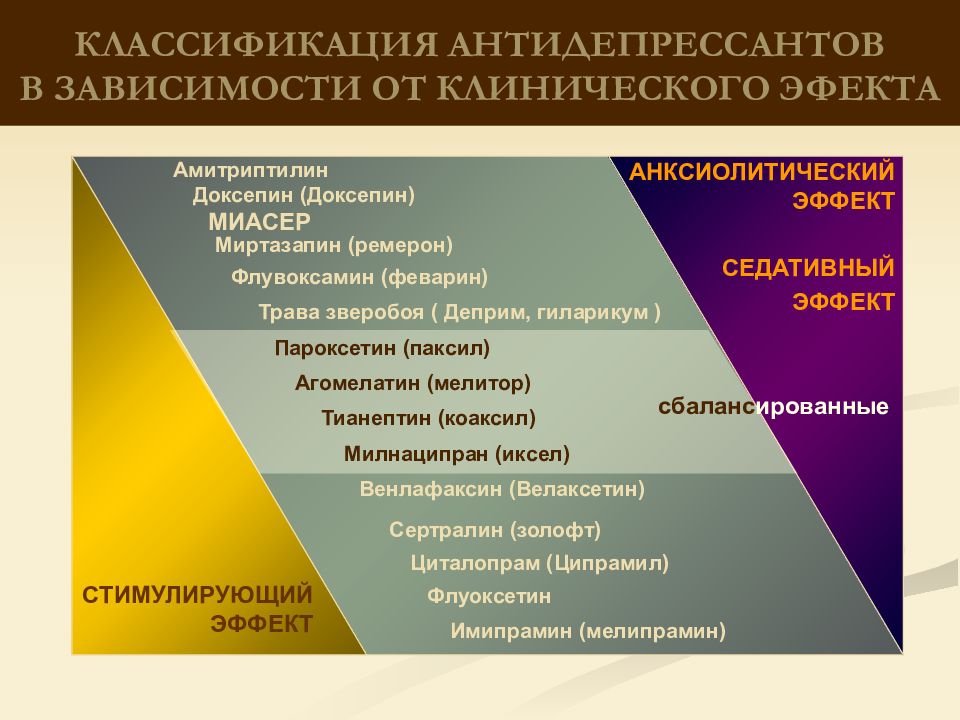 пробный.Наличие и сила этой корреляции дискуссионны [24].
пробный.Наличие и сила этой корреляции дискуссионны [24].
Наконец, корпус испытаний антидепрессантов молча принял ряд критериев исключения. Эмпирическая оценка показала, что общими критериями исключения являются короткая продолжительность эпизода, легкая степень тяжести заболевания, сопутствующие психиатрические заболевания, большая продолжительность заболевания, сопутствующие медицинские заболевания и предшествующее отсутствие ответа на лечение [24]. На самом деле существует мало эмпирических данных о том, что любой из этих критериев, возможно, за исключением короткой продолжительности эпизода, действительно влияет на величину чистого эффекта лечения.И наоборот, все они снижают обобщаемость результатов испытаний. Основываясь на их обширных продажах, мы должны сделать вывод, что антидепрессанты используются гораздо шире в клинической практике по сравнению с узкими условиями клинических испытаний, определяемыми такими ограничительными критериями приемлемости.
В целом, мы мало знаем о том, как конструктивные особенности могут влиять на результаты. Например, сообщалось, что даже график дозирования (гибкий или фиксированный), количество групп лечения и процент женщин-пациентов связаны с величиной лечебного эффекта в исследованиях [25].
Например, сообщалось, что даже график дозирования (гибкий или фиксированный), количество групп лечения и процент женщин-пациентов связаны с величиной лечебного эффекта в исследованиях [25].
Кратковременное наблюдение
Большинство исследований антидепрессантов имеют ограниченную продолжительность наблюдения, обычно 6 недель и редко превышающую 8 недель. Некоторые испытания даже длятся всего 3–4 недели. Даже при таком коротком периоде наблюдения в этих исследованиях очень часто встречается отсев (выбывание из наблюдения и/или прекращение приема исследуемого препарата) [26]. Вменение результатов, когда информация отсутствует из-за отсева, непростая задача и оставляет место для предвзятости.
В основном имеют значение различия в долгосрочных тяжелых клинических исходах (самоубийство, потеря работы, другие важные личные или социальные события), потому что эти препараты иногда используются пациентами в обществе в течение гораздо более длительного времени. основа.Доказательства долгосрочной поддерживающей терапии были рассмотрены с помощью метаанализа исследований, в которых пациенты, ответившие на лечение в острой фазе, были рандомизированы в группу поддерживающей терапии по сравнению с плацебо [27]. Несмотря на то, что было продемонстрировано значительное снижение вероятности рецидива, эти 31 испытание по-прежнему являются небольшими (всего n = 4410), в большинстве из них период наблюдения не превышает 12 месяцев, они сосредоточены на тех, кто дал острый ответ и не смог устранить другие тяжелые последствия депрессии.
Несмотря на то, что было продемонстрировано значительное снижение вероятности рецидива, эти 31 испытание по-прежнему являются небольшими (всего n = 4410), в большинстве из них период наблюдения не превышает 12 месяцев, они сосредоточены на тех, кто дал острый ответ и не смог устранить другие тяжелые последствия депрессии.
Избирательное и искаженное сообщение
Как показал метаанализ New England Journal of Medicine [7], избирательное и искаженное сообщение результатов является серьезной проблемой в литературе по антидепрессантам.Даже со всеми вышеперечисленными манипуляциями и потенциально избирательным анализом только половина испытаний антидепрессантов достигает общепринятой статистической значимости. Другая половина либо исчезает, либо еще больше искажается, чтобы публиковаться с впечатлением, что они также нашли «положительные» результаты. Таким образом, метаанализ опубликованной литературы может дать вводящее в заблуждение впечатление об эффективности этих препаратов.
Неизвестный вред
Испытания антидепрессантов не направлены на демонстрацию возможного вреда этих лекарств.Несоответствие акцента между эффективностью и вредом в дизайне и отчетности рандомизированных исследований неоднократно демонстрировалось в различных медицинских специальностях [28], включая вмешательства в области психического здоровья [29]. Небольшие испытания вряд ли выявят какой-либо серьезный вред, даже относительно распространенный, не говоря уже о необычных вредах, которые опасны для жизни и могут привести к смерти. Таким образом, антидепрессанты лицензируются почти в полном вакууме информации о вреде. Вред может быть обнаружен впоследствии с помощью метаанализов, крупных реестров или других средств постмаркетингового наблюдения, но все эти методы имеют ограничения и несовершенную чувствительность и специфичность.Широкие дебаты о нераспознанном риске суицида у детей, принимающих антидепрессанты, являются одним из примеров того, как очень серьезный вред может остаться незамеченным [30–32]. Позднее добавление предупреждений в виде черного ящика увеличивает чувство неопределенности в отношении этих препаратов [33]. Неопределенность в отношении вреда никому не помогает, даже отрасли. Репутация отрасли может быть испорчена даже постулируемым ущербом, которого может не быть, например. как в дебатах о росте самоубийств среди взрослых.
Позднее добавление предупреждений в виде черного ящика увеличивает чувство неопределенности в отношении этих препаратов [33]. Неопределенность в отношении вреда никому не помогает, даже отрасли. Репутация отрасли может быть испорчена даже постулируемым ущербом, которого может не быть, например. как в дебатах о росте самоубийств среди взрослых.
Расширение рынка
Как описано выше, клинические испытания антидепрессантов охватывают очень ограниченные группы пациентов и обычно используют краткосрочное введение.Однако после получения лицензии антидепрессанты широко используются среди населения в целом и часто назначаются для очень длительного применения [1–3]. Антидепрессанты — яркий пример чрезмерной медикализации нашего общества [1]. Прямая реклама для потребителей, вероятно, в значительной степени способствует такому распространению использования. Фармакоэкономическая оценка показала, что прямая реклама антидепрессантов потребителю может привести к такому широкому охвату людей, что 94% использования антидепрессантов из-за прямой рекламы потребителю приходится на лиц, не страдающих депрессией [34]. В той же оценке сделан вывод, что это более чем уравновешено накопленными социальными преимуществами, которые дает лечение пациентов с истинной депрессией, которых иначе не лечили бы [34]. Однако этот вывод основан на предположении о высокой эффективности антидепрессантов, что, вероятно, не соответствует современным данным.
В той же оценке сделан вывод, что это более чем уравновешено накопленными социальными преимуществами, которые дает лечение пациентов с истинной депрессией, которых иначе не лечили бы [34]. Однако этот вывод основан на предположении о высокой эффективности антидепрессантов, что, вероятно, не соответствует современным данным.
Создание поддерживающего научного мифа
Помимо рандомизированных испытаний, промышленность использовала биологические аргументы для продвижения идеи в более широком сообществе о том, что антидепрессанты имеют механизмы действия, которые корректируют основные химические дисбалансы в мозге [1].Типичным примером является маркетинг СИОЗС, основанный на серотониновой гипотезе. Несправедливо или даже неправильно подводить итоги десятилетий нейробиологических исследований, показывая, что депрессия вызывается дисбалансом того или иного нейротрансмиттера (серотонина, норадреналина или другого) в головном мозге. Во всяком случае, развитие знаний в области биологии показывает, что депрессия представляет собой чрезвычайно сложный поведенческий фенотип, регулируемый большим количеством биологических путей, внешних воздействий и генетических факторов, каждый из которых вносит небольшой вклад [1, 35]. Ожидается, что лекарства, которые предположительно воздействуют на один путь, будут иметь небольшое влияние на общую биологию депрессии и будут уравновешены балансирующими изменениями. Таким образом, ожидается, что клинические эффекты также будут в среднем небольшими.
Ожидается, что лекарства, которые предположительно воздействуют на один путь, будут иметь небольшое влияние на общую биологию депрессии и будут уравновешены балансирующими изменениями. Таким образом, ожидается, что клинические эффекты также будут в среднем небольшими.
Ответы на основные практические вопросы
Показаны ли антидепрессанты при депрессии?
Исходя из приведенных выше соображений, антидепрессанты, вероятно, показаны только избранным пациентам с большой депрессией, вероятно, предпочтительно тем, у кого есть тяжелые симптомы и которые не реагируют ни на что другое.Для большинства пациентов с некоторыми депрессивными симптомами, которые в настоящее время принимают антидепрессанты, использование этих препаратов не было бы предпочтительным вариантом, плацебо было бы практически таким же хорошим, если не лучшим, и позволило бы снизить токсичность и стоимость.
Текущее одобрение определенных антидепрессантов регулирующими органами означает, что были соблюдены определенные критерии, которые демонстрируют некоторые номинально статистически значимые результаты в некоторых испытаниях и по некоторым шкалам, но это не эквивалентно доказательству значительной клинической пользы, эффективности в более широкой популяции. уровень.Проводимые испытания не обязательно являются научными упражнениями, а скорее упражнениями, предназначенными для демонстрации определенного эффекта в нормативных/правовых целях.
уровень.Проводимые испытания не обязательно являются научными упражнениями, а скорее упражнениями, предназначенными для демонстрации определенного эффекта в нормативных/правовых целях.
Некоторые другие метааналитики обнаружили еще более мрачные результаты, чем два метаанализа, рассмотренные выше. Например, после включения как опубликованных, так и неопубликованных данных (29 и 11 исследований соответственно), в одном метаанализе недавно не было обнаружено абсолютно никакого преимущества пароксетина по сравнению с плацебо, когда основное внимание уделялось «тяжелому» клиническому исходу прекращения лечения [36].Некоторый лечебный эффект, вероятно, присутствует в «более мягких» исходах, основанных на шкале, но он, вероятно, будет небольшим, и, возможно, оценки эффекта завышены по сравнению с правдой. Кумулятивные метаанализы показывают, что для медикаментозного лечения по показаниям для психического здоровья в целом эффект лечения имеет тенденцию к снижению со временем, поскольку проводится больше исследований [37]. Эмпирические данные свидетельствуют также о том, что большая часть эффекта плацебо в исследованиях антидепрессантов связана просто с количеством посещений пациентов во время исследования [38].Испытания, в которых пациенты должны чаще посещать врачей для оценки во время исследования, улучшаются больше, независимо от того, получают ли они лекарство или плацебо. Каждое дополнительное посещение в ходе исследования улучшается на 0,6–0,9 балла по шкале Гамильтона.
Эмпирические данные свидетельствуют также о том, что большая часть эффекта плацебо в исследованиях антидепрессантов связана просто с количеством посещений пациентов во время исследования [38].Испытания, в которых пациенты должны чаще посещать врачей для оценки во время исследования, улучшаются больше, независимо от того, получают ли они лекарство или плацебо. Каждое дополнительное посещение в ходе исследования улучшается на 0,6–0,9 балла по шкале Гамильтона.
Возможно, большинству людей, получающих антидепрессанты при симптомах депрессии, просто нужно внимание со стороны врача и людей, с которыми можно поговорить и позаботиться о них. Антидепрессанты могут в значительной степени покрывать утраченное плацебо человеческого взаимодействия и взаимодействия пациента и врача, которое стало таким редким в современном обществе.Однако я не буду здесь комментировать, являются ли формальные методы психотерапии такими же или более эффективными, чем антидепрессанты. Доказательная база психотерапии ничем не лучше, она относится к таким же небольшим исследованиям, затронутым большинством тех же проблем (и даже больше), и сама по себе потребовала бы целого отдельного обзора [39].
Убивать живой миф неэтично?
Если большая часть эффективности антидепрессантов отражает просто эффект плацебо, и если большинство людей получают ровно столько, сколько позволяет эффект плацебо, то неэтично ли уничтожать живой миф? Кто-то может возразить, что если население будет информировано о том, что антидепрессанты на самом деле неэффективны, это может свести на нет преимущества, которые мы получаем от эффекта плацебо, когда принимаем эти лекарства.Однако не этично ли лгать пациентам, что вмешательство эффективно, когда это не так? Более того, если мы хотим использовать этот эффект плацебо, почему оправдано, что это должно стоить обществу в совокупности больше миллиарда долларов, чем почти любое другое (действительно эффективное) фармацевтическое вмешательство для любого другого состояния? Было бы странно, если бы наше общество пошло на компромисс с мнением, что кто-то должен наживаться на продаже официальных плацебо.
Фармацевтическая промышленность переживает тяжелые времена [40]. Поскольку в настоящее время истекает срок действия эксклюзивных лицензий на большинство крупных блокбастеров, есть опасения, что, если крупной фармацевтике не удастся сохранить свою прибыль, ее исследования и разработки будут остановлены. Еще более циничная точка зрения состоит в том, что, поскольку наше общество нацелено на получение прибыли, если мы не позволим фармацевтической промышленности получать большие прибыли, даже за счет продажи в основном неэффективных лекарств населению, то какая-то другая отрасль будет привлекать капиталовложения. и будет процветать вместо этого. Это может быть в предпринимательской сфере, которая менее полезна или даже очень вредна для общества, например.г. оружейная промышленность. Я отвечаю, что фармацевтическую промышленность следует поощрять и поддерживать в проведении высококачественных исследований в области антидепрессантов и не только. Серьезные исследования в области наук о жизни, проводимые корпоративными, государственными и академическими исследователями, должны стать приоритетом в качестве общественных целей, но ожидания должны быть реалистичными: большинство крупных обещаний не материализуются [41], крупные открытия редки, лекарства не являются чудесами, и мы должны быть честными в том, как многого мы достигли и чего мы можем достичь.
Поскольку в настоящее время истекает срок действия эксклюзивных лицензий на большинство крупных блокбастеров, есть опасения, что, если крупной фармацевтике не удастся сохранить свою прибыль, ее исследования и разработки будут остановлены. Еще более циничная точка зрения состоит в том, что, поскольку наше общество нацелено на получение прибыли, если мы не позволим фармацевтической промышленности получать большие прибыли, даже за счет продажи в основном неэффективных лекарств населению, то какая-то другая отрасль будет привлекать капиталовложения. и будет процветать вместо этого. Это может быть в предпринимательской сфере, которая менее полезна или даже очень вредна для общества, например.г. оружейная промышленность. Я отвечаю, что фармацевтическую промышленность следует поощрять и поддерживать в проведении высококачественных исследований в области антидепрессантов и не только. Серьезные исследования в области наук о жизни, проводимые корпоративными, государственными и академическими исследователями, должны стать приоритетом в качестве общественных целей, но ожидания должны быть реалистичными: большинство крупных обещаний не материализуются [41], крупные открытия редки, лекарства не являются чудесами, и мы должны быть честными в том, как многого мы достигли и чего мы можем достичь. Ложь, чтобы конкурировать с более недобросовестными производителями лжи в нашем обществе, — это не путь к научному прогрессу.
Ложь, чтобы конкурировать с более недобросовестными производителями лжи в нашем обществе, — это не путь к научному прогрессу.
Работают ли антидепрессанты? — The New York Times
Больше людей в Соединенных Штатах принимают антидепрессанты в процентах от населения, чем в любой другой стране мира. И все же эффективность лекарств вызывает горячие споры.
Некоторые считают, что краткосрочные выгоды гораздо скромнее, чем принято считать, и что в долгосрочной перспективе вред может перевесить пользу.Другие считают, что они работают и могут изменить жизнь.
Уладить этот спор оказалось намного сложнее, чем вы думаете.
Дело не в том, что нам не хватает исследований. Много, много исследований антидепрессантов можно найти в рецензируемой литературе. Проблема в том, что это был яркий пример предвзятости публикации: положительные исследования, скорее всего, будут опубликованы, а отрицательные, скорее всего, будут похоронены в ящике стола.
В 2008 году группа исследователей сделала этот вывод, проведя метаанализ испытаний антидепрессантов, которые были зарегистрированы Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов в качестве доказательства в поддержку разрешений на продажу или изменений в маркировке. Компании должны были представить результаты зарегистрированных испытаний в F.D.A. независимо от результата. В этих испытаниях также, как правило, меньше массирования данных — например, выборки результатов — чем это было бы возможно в журналах.
Компании должны были представить результаты зарегистрированных испытаний в F.D.A. независимо от результата. В этих испытаниях также, как правило, меньше массирования данных — например, выборки результатов — чем это было бы возможно в журналах.
Исследователи нашли 74 исследования лекарств, одобренных в период с 1987 по 2004 год, в которых приняли участие более 12 500 пациентов. Около половины этих испытаний имели «положительные» результаты в том, что антидепрессант работал лучше, чем плацебо; другая половина была «отрицательной». Но если бы вы смотрели только в опубликованной литературе, вы бы получили совсем другую картину.Почти все положительные исследования есть. Только три отрицательных исследования фигурируют в литературе как отрицательные. 22 никогда не публиковались, а 11 были опубликованы, но переупакованы так, чтобы они выглядели положительными.
Второй метаанализ, опубликованный в том же году, также использовал F.D.A. данные вместо рецензируемой литературы, но задал другой вопрос.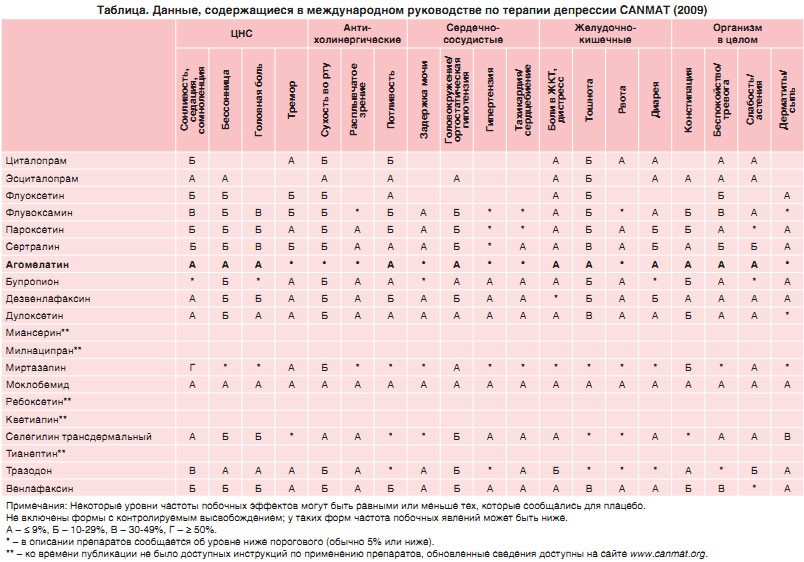 Исследователи задались вопросом, была ли эффективность исследования связана с исходным уровнем депрессии его участников. Результаты показали, что да.Эффективность антидепрессантов была ограничена у пациентов с умеренной депрессией и мала у пациентов с тяжелой депрессией.
Исследователи задались вопросом, была ли эффективность исследования связана с исходным уровнем депрессии его участников. Результаты показали, что да.Эффективность антидепрессантов была ограничена у пациентов с умеренной депрессией и мала у пациентов с тяжелой депрессией.
Вывод из этих двух исследований заключался в том, что эффективность антидепрессантов была преувеличена и что польза могла быть ограничена гораздо меньшим числом пациентов, чем те, которые фактически принимали лекарства.
Эти и другие моменты были изложены в статье, написанной Джоном Иоаннидисом в журнале «Философия, этика и гуманитарные науки в медицине» в 2008 году.Он утверждал, что дизайн исследования и выбранные популяции, особенно короткая продолжительность многих исследований, предвзято относились к положительным результатам. Он утверждал, что хотя многие исследования достигли статистической значимости, им не удалось достичь клинической значимости. Он утверждал, что мы слишком мало знали о долгосрочном вреде и что нам представили предвзятую информацию, когда мы смотрели только на опубликованные данные.
Этот документ — «Эффективность антидепрессантов: доказательный миф, основанный на тысячах рандомизированных испытаний?» — посеяли затянувшиеся сомнения по поводу применения антидепрессантов и проведения медицинских исследований.Но недавно было опубликовано самое всестороннее исследование антидепрессантов на сегодняшний день, и оно, похоже, представляет собой тщательную попытку преодолеть препятствия прошлого.
Исследователи, в том числе д-р Иоаннидис на этот раз, провели поиск в медицинской литературе, на веб-сайтах регулирующих органов и в международных реестрах опубликованных и неопубликованных двойных слепых рандомизированных контролируемых испытаний вплоть до начала 2016 года.
Они искали плацебо — контролируемые и непосредственные испытания 21 антидепрессанта, используемого для лечения большого депрессивного расстройства у взрослых.Они использовали «метод сетевого метаанализа», который позволяет сравнивать несколько видов лечения как в рамках отдельных испытаний напрямую, так и между испытаниями косвенно с общим компаратором. Они исследовали не только то, насколько хорошо действуют лекарства, но и переносимость лечения — то, что они назвали приемлемостью.
Они исследовали не только то, насколько хорошо действуют лекарства, но и переносимость лечения — то, что они назвали приемлемостью.
Они обнаружили 522 испытания, в которых участвовало более 116 000 человек. Из них 86 были неопубликованными исследованиями, найденными в реестрах испытаний и на веб-сайтах компаний. Еще 15 были обнаружены в результате личного общения или ручного поиска обзорных статей.Авторы сделали дополнительный шаг и запросили неопубликованные данные о найденных ими исследованиях, получив их более чем для половины включенных испытаний.
Обнадеживающая новость заключается в том, что все антидепрессанты оказались более эффективными, чем плацебо. Они незначительно различались с точки зрения эффективности и приемлемости, поэтому каждый пациент и врач должны обсудить потенциальную пользу и вред отдельных препаратов.
Еще одной хорошей новостью является то, что небольшие испытания не дали существенно отличающихся результатов от более крупных испытаний.
Также не оказалось, что спонсирование испытаний промышленностью коррелирует со значительными различиями в показателях ответов или отсева. Но — и это большое «но» — подавляющее большинство испытаний финансируется промышленностью. В результате в этом метаанализе могло быть недостаточно данных о непромышленных испытаниях, чтобы точно определить, существует ли разница.
Были также признаки предвзятости «новизны»: казалось, что антидепрессанты действуют лучше, когда они только что были выпущены на рынок, но, похоже, потеряли эффективность и приемлемость в последующие годы.
Плохая новость заключается в том, что, несмотря на наличие статистически значимых различий, размеры эффекта все же были в основном скромными. Преимущества также распространялись только на людей, которые страдали от глубокой депрессии, особенно в краткосрочной перспективе. Другими словами, это исследование предоставляет доказательства того, что, когда у людей обнаруживается острая большая депрессия, лечение антидепрессантами улучшает результаты в течение первых двух месяцев терапии.
Поскольку у нас нет надежных данных, мы до сих пор не знаем, насколько хорошо антидепрессанты действуют на людей с более легкими симптомами, не соответствующими большой депрессии, особенно если пациенты принимали лекарства месяцами или даже годами.Многие люди, вероятно, попадают в эту категорию, но им по-прежнему регулярно назначают антидепрессанты в течение длительного времени. Мы не знаем, какая часть пользы, полученной от такого использования, является эффектом плацебо по сравнению с биологическим.
Я спросил доктора Иоаннидиса, так ли радикальны результаты этого нового исследования, как предполагалось во многих новостных статьях. Он подтвердил, что это был гораздо более масштабный метаанализ — с примерно в 10 раз большим количеством информации — чем те, что были проведены десять лет назад, с большим количеством неопубликованных данных и большим количеством антидепрессантов.Он также надеется, что будущие исследования будут еще лучше информировать об ответах на индивидуальном уровне, что может помочь увидеть, получают ли некоторые пациенты существенную пользу, даже когда другие, кажется, не получают никакой пользы.
Но он подумал, что некоторые из изобилия в средствах массовой информации могут быть немного преувеличены. «Я боюсь, что некоторые новостные сообщения давали очень грубые интерпретации, которые могут ввести в заблуждение, особенно когда их заголовки были слишком категоричными, например, «наркотики работают», «дебаты окончены» и так далее», — сказал он.«Клиническая (в отличие от статистической) значимость обнаруженных нами эффектов лечения будет по-прежнему оспариваться, и по-прежнему важно найти способы, с помощью которых можно определить конкретных пациентов, которые получат максимальную пользу».
Несмотря на столь обширные исследования антидепрессантов, остается много вопросов без ответа. Неясно, будут ли фармацевтические компании заинтересованы в результатах и почему. Препараты уже широко используются, и ни один регулирующий орган не требует дополнительных данных.Если пациенты хотят получить ответы, они должны сами потребовать проведения исследования.
Почему мои антидепрессанты не работают?
Отзыв:
Если вы чувствуете, что ваш антидепрессант перестал действовать, вы не одиноки. Обычно лекарство, которое когда-то творило чудеса, становится неэффективным, особенно если вы принимаете его в течение длительного времени. Симптомы возвращаются у 33% людей, принимающих антидепрессанты — это называется прорывной депрессией.
Обычно лекарство, которое когда-то творило чудеса, становится неэффективным, особенно если вы принимаете его в течение длительного времени. Симптомы возвращаются у 33% людей, принимающих антидепрессанты — это называется прорывной депрессией.
«Обычно антидепрессант, который помог пациенту, будет продолжать работать», — говорит Пол Нештадт, доктор медицинских наук, психиатр и содиректор Клиники тревожных расстройств Джека и Мэри МакГлассон в Университете Джонса Хопкинса. «Но иногда может возникнуть новый эпизод депрессии, который не так хорошо реагирует на это лекарство, или лекарство может просто перестать работать».
Почему лекарства от депрессии перестают работать?
На реакцию организма на антидепрессант могут влиять различные факторы, в том числе:
- Употребление наркотиков или алкоголя. Незаконное употребление наркотиков и алкоголя может вызвать сильные изменения настроения, которые могут сделать антидепрессанты неэффективными.

- Беременность. Вес вашего тела и объем крови увеличиваются, когда вы беременны. Поговорите со своим врачом о приеме антидепрессантов во время беременности и о возможной корректировке дозировки для дальнейшего облегчения симптомов.
- Новые стрессоры. Новая стрессовая ситуация дома или на работе может привести к изменению настроения, которое антидепрессант не сможет компенсировать.
- Другие лекарства. Взаимодействия между антидепрессантами и лекарствами от других заболеваний могут повлиять на эффективность действия антидепрессантов.
Однако чаще всего антидепрессанты перестают действовать без всякой причины. «Нет хороших исследований, показывающих, почему лекарство может перестать работать на кого-то», — говорит Нештадт. «Я думаю, что это не столько вопрос формирования толерантности, сколько постоянно меняющиеся стрессоры и факторы в мозгу.»
Когда обратиться к врачу
Если симптомы депрессии сохраняются более чем на несколько дней, пора обратиться к врачу. Но даже если вы чувствуете, что ваш антидепрессант не работает, важно продолжать принимать его, пока ваш врач не посоветует иначе. Вам может потребоваться увеличение дозы или постепенное снижение дозы. Слишком быстрое прекращение приема многих антидепрессантов может вызвать эффекты отмены, такие как:
Но даже если вы чувствуете, что ваш антидепрессант не работает, важно продолжать принимать его, пока ваш врач не посоветует иначе. Вам может потребоваться увеличение дозы или постепенное снижение дозы. Слишком быстрое прекращение приема многих антидепрессантов может вызвать эффекты отмены, такие как:
- Головные боли
- Тошнота
- Диарея или запор
- Повышенное беспокойство
- Суицидальные мысли
Ранние предупреждающие признаки прорывной депрессии — это симптомы, которые вы обычно испытываете, когда начинается приступ депрессии, — говорит Нештадт.Симптомы депрессии варьируются от человека к человеку, но признаки включают:
- Плохое настроение
- Изменения сна или аппетита
- Снижение социализации
- Потеря интереса к ранее приятным занятиям
Если ваши симптомы вернутся, не беспокойтесь — коррекция дозы или переход на другой антидепрессант часто решает проблему. (Примечание: если у вас есть мысли о самоповреждении или самоубийстве, немедленно обратитесь к врачу, позвоните по номеру 911 или обратитесь в отделение неотложной помощи.)
(Примечание: если у вас есть мысли о самоповреждении или самоубийстве, немедленно обратитесь к врачу, позвоните по номеру 911 или обратитесь в отделение неотложной помощи.)
Смена лекарств от депрессии
Если вы и ваш врач исключили факторы, которые могут помешать вашему текущему лечению, ваш врач может увеличить дозировку, перевести вас на другой антидепрессант или порекомендовать вам принять дополнительное лекарство. Медикаментозная терапия для лечения депрессии включает:
Селективные ингибиторы обратного захвата серотонина (СИОЗС)
Препараты СИОЗС являются наиболее часто назначаемыми антидепрессантами и часто считаются первой линией защиты от депрессии.Они повышают уровень нейротрансмиттера (химического вещества, передающего сообщения от клетки мозга к клетке мозга) серотонина. Этот нейротрансмиттер связан с чувством счастья и удовлетворения. Побочные эффекты СИОЗС, как правило, легкие, а симптомы депрессии значительно улучшаются примерно у 60% людей с умеренной или тяжелой депрессией.
Селективные ингибиторы обратного захвата серотонина и норадреналина (SSNRI)
Препараты как SSNRI, так и SSRI влияют на уровень серотонина, но препараты SSNRI также влияют на уровень норадреналина, другого нейромедиатора, который может влиять на настроение.Этот тип лекарств полезен для тех, кто испытывает сильную усталость, связанную с депрессией, или у кого были побочные эффекты или плохой ответ на препараты СИОЗС.
Трициклические антидепрессанты (ТЦА)
ПрепаратыTCA повышают уровень серотонина и норадреналина в головном мозге, но, в отличие от других типов антидепрессантов, они также блокируют ацетилхолин, нейротрансмиттер, связанный с повышенным стрессом, тревогой и депрессией. Вы можете испытывать больше побочных эффектов при приеме препаратов ТЦА, чем при приеме препаратов СИОЗС или СИОЗСН.
Ингибиторы моноаминоксидазы (ИМАО)
Препараты ИМАО подавляют распад дофамина, норадреналина и серотонина, что увеличивает их концентрацию в головном мозге. Низкий уровень этих нейротрансмиттеров связан с депрессией и тревогой. Препараты ИМАО имеют большее количество серьезных побочных эффектов. Люди, принимающие их, должны помнить о взаимодействии лекарства с некоторыми продуктами питания и другими лекарствами.
Низкий уровень этих нейротрансмиттеров связан с депрессией и тревогой. Препараты ИМАО имеют большее количество серьезных побочных эффектов. Люди, принимающие их, должны помнить о взаимодействии лекарства с некоторыми продуктами питания и другими лекарствами.
Бупропион
Бупропион действует на дофамин и норадреналин.Его главное преимущество заключается в том, что он не вызывает неприятных побочных эффектов, таких как снижение либидо и увеличение веса, как это делают другие типы антидепрессантов. Однако он может быть менее полезен при депрессии с признаками тревоги.
Эскетамин
Этот новый препарат обеспечивает облегчение симптомов депрессии в течение нескольких часов за счет повышения уровня глутамата, наиболее распространенного нейротрансмиттера в головном мозге. Эскетамин выпускается в виде назального спрея, который необходимо вводить в клинике, поскольку он может вызывать галлюцинации и другие сенсорные побочные эффекты в течение двух часов после лечения. Это эффективный препарат для тех, кто не ответил на другие антидепрессанты.
Это эффективный препарат для тех, кто не ответил на другие антидепрессанты.
Если у вас прорывная депрессия, важно проконсультироваться с врачом, чтобы снова почувствовать себя лучше. «Лекарства нередко перестают работать», — говорит Нештадт. «Это происходит и с другими видами лечения. Иногда ваше лекарство от кровяного давления перестает быть эффективным, и его нужно заменить. Это просто природа лечения болезни».
Эффективность антидепрессантов по сравнению с плацебо при депрессии в первичной медико-санитарной помощи — Кокрейн для клиницистов
Am Fam Physician. 1 июля 2010 г. ;82(1):42.
Клинический вопрос
Какова эффективность антидепрессантов по сравнению с плацебо при лечении депрессии в учреждениях первичной медико-санитарной помощи?
Основанный на доказательствах ответ
Трициклические антидепрессанты (ТЦА) и селективные ингибиторы обратного захвата серотонина (СИОЗС) более эффективны, чем плацебо, для лечения депрессии в учреждениях первичной медико-санитарной помощи. (Сила рекомендации = A, основанная на согласованных, ориентированных на пациента доказательствах хорошего качества)
(Сила рекомендации = A, основанная на согласованных, ориентированных на пациента доказательствах хорошего качества)
Практические рекомендации
У пациентов с симптомами депрессии от легкой до умеренной степени преимущества антидепрессантов по сравнению с плацебо незначительны или отсутствуют.Лекарства более эффективны у пациентов с тяжелой депрессией.1 В этом Кокрейновском обзоре сравнивалась эффективность антидепрессантов с плацебо у пациентов с депрессией, которые были набраны из учреждений первичной медико-санитарной помощи. В него вошли 14 рандомизированных контролируемых испытаний с участием пациентов в возрасте от 18 до 65 лет. В большинстве испытаний сообщалось о краткосрочных результатах через четыре-шесть недель; четыре испытания имели последующее наблюдение в течение 12–24 недель. Большинство исследований спонсировались фармацевтическими компаниями.
По сравнению с плацебо, ТЦА продемонстрировали большее улучшение показателей депрессии и больший клинический ответ на ремиссию (число, необходимое для лечения [ЧБНЛ] = 9; 95% доверительный интервал [ДИ], от 6 до 16), оцененные врачами первичного звена или психиатры. Число, необходимое для причинения вреда (NNH), варьировалось от 4 до 30 у участников, принимавших ТЦА, которые прекратили лечение из-за побочных эффектов.
Число, необходимое для причинения вреда (NNH), варьировалось от 4 до 30 у участников, принимавших ТЦА, которые прекратили лечение из-за побочных эффектов.
СИОЗС продемонстрировали клиническую пользу в отношении улучшения показателей депрессии (NNT = 7; 95% ДИ, от 7 до 8). Больше пациентов в группе СИОЗС выбыло из исследований из-за побочных эффектов (относительный риск [RR] = 2,05; 95% ДИ, 1,11–3,75; NNH = 20–90) по сравнению с плацебо, но меньше пациентов в группе СИОЗС выбыло из исследования из-за побочных эффектов. неэффективность лечения (ОР = 0,51; 95% ДИ, 0.34 до 0,78). Другие обзоры показали более высокие показатели отсева, связанные с переносимостью, у участников, принимающих СИОЗС.
Американский колледж врачей рекомендует, чтобы при выборе фармакологической терапии для лечения пациентов с острой большой депрессией они выбирали антидепрессанты второго поколения на основе профилей побочных эффектов, стоимости и предпочтений пациентов.2 Институт усовершенствования клинических систем заявляет что СИОЗС, а также венлафаксин (Эффексор), дулоксетин (Симбалта), миртазапин (Ремерон) и бупропион (Веллбутрин) часто выбирают в качестве вариантов лечения антидепрессантами первой линии из-за качества и количества опубликованных данных по этим препаратам; их относительная переносимость побочных эффектов по сравнению с ТЦА и ингибиторами моноаминоксидазы; и их общая относительная безопасность. 3
3
Чтобы увидеть статью полностью, авторизуйтесь или приобретите доступ.
JANELLE GUIRGIIS-BLAKE, MD
Авторское сообщение: Нечего раскрывать.
ИСТОЧНИК
Арролл Б, Элли КР, Фишман Т, и другие. Антидепрессанты по сравнению с плацебо при лечении депрессии в первичной медико-санитарной помощи. Кокрановская система базы данных, версия . 2009; (3): CD007954.
ССЫЛКИ
1. Фурнье Дж.К., Де Рубейс Р.Дж., Холлон С.Д., и другие.Эффекты антидепрессантов и тяжесть депрессии: метаанализ на уровне пациентов. ЯМА . 2010;303(1):47–53.
2. Касим А.,
Сноу В,
Денберг ТД,
Форсиа М.А.
Оуэнс Д.К.; Подкомитет по клинической эффективности Американского колледжа врачей. Использование антидепрессантов второго поколения для лечения депрессивных расстройств: руководство по клинической практике Американского колледжа врачей [опубликованное исправление опубликовано в Ann Intern Med. 2009;150(2):148]. Энн Интерн Мед .
2008;149(10):725–733.
2009;150(2):148]. Энн Интерн Мед .
2008;149(10):725–733.
3. Институт усовершенствования клинических систем. Рекомендации по охране здоровья: большая депрессия у взрослых в условиях первичной медико-санитарной помощи. 12-е изд. Май 2009 г. http://www.icsi.org/depression_5/depression__major__in_adults_in_primary_care_3.html. По состоянию на 11 мая 2010 г.
Copyright © 2010 Американской академии семейных врачей.
Этот контент принадлежит AAFP. Лицо, просматривающее его в Интернете, может сделать одну распечатку материала и может использовать эту распечатку только для личного некоммерческого ознакомления.Этот материал нельзя загружать, копировать, распечатывать, хранить, передавать или воспроизводить на любом носителе, известном сейчас или изобретенном позже, за исключением случаев, когда это разрешено в письменной форме AAFP. Контакт
[email protected] для вопросов об авторских правах и/или запросов разрешений.
Эффективность и действенность антидепрессантов: современное состояние исследований — Полный текст — Психотерапия и психосоматика 2010, Vol.
 79, № 5
79, № 5Аннотация
Справочная информация: В этой статье рассматривается текущее состояние исследований эффективности и действенности антидепрессантов. Методы: В этом документе рассматриваются четыре мета-анализа испытаний эффективности, представленных в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), и анализируется STAR*D (альтернативы последовательного лечения для облегчения депрессии), крупнейшее из когда-либо проводившихся испытаний эффективности антидепрессантов. Результаты: Мета-анализ испытаний FDA предполагает, что антидепрессанты лишь незначительно эффективны по сравнению с плацебо, и документирует глубокую предвзятость публикаций, которая преувеличивает их очевидную эффективность. Эти мета-анализы также документируют вторую форму предвзятости, когда исследователи не сообщают об отрицательных результатах по заранее заданному первичному критерию исхода, представленному в FDA, в то же время подчеркивая в опубликованных исследованиях положительные результаты вторичного или даже нового критерия, как будто это была их основная мера интереса. Анализ STAR*D показал, что эффективность терапии антидепрессантами, вероятно, была даже ниже, чем скромная, о которой сообщают авторы исследования, с очевидным прогрессивным увеличением процента отсева на каждой фазе исследования. Выводы: Проанализированные данные свидетельствуют о необходимости переоценки текущих рекомендуемых стандартов лечения депрессии.
Анализ STAR*D показал, что эффективность терапии антидепрессантами, вероятно, была даже ниже, чем скромная, о которой сообщают авторы исследования, с очевидным прогрессивным увеличением процента отсева на каждой фазе исследования. Выводы: Проанализированные данные свидетельствуют о необходимости переоценки текущих рекомендуемых стандартов лечения депрессии.
© 2010 S. Karger AG, Базель
Введение
При оценке лекарственных средств для определения их применимости в научно обоснованной клинической практике важно оценить их эффективность в рандомизированных двойных слепых плацебо-контролируемых исследованиях (РКИ) в дополнение к определению их эффективности в лечении реальных -мировые пациенты в условиях, имитирующих реальную практику.
Эффективность
Из-за давних опасений по поводу предвзятости публикаций, преувеличивающей воспринимаемую эффективность [1,2,3,4] и, как следствие, неблагоприятного воздействия на доказательную помощь, исследователи с общественным мнением уже давно выступают за всеобъемлющий репозиторий регистрационных данных предоставление полного доступа к протоколам и результатам испытаний лекарственных средств [1,5,6]. Американское управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) ни в коем случае не является полным, но в рамках процесса подачи заявок на новые лекарства у него имеется большой репозиторий исследований РКИ.Перед проведением испытаний новых препаратов фармацевтические компании должны зарегистрировать их в FDA, что включает в себя предварительное определение первичных и вторичных показателей результатов и средств анализа. Предварительная спецификация необходима для обеспечения честности исследования и позволяет обнаружить, когда исследователи выборочно публикуют показатели, которые показывают результаты, которые спонсоры предпочитают после сбора и анализа данных, форма предвзятости исследователя, известная как HARKing [7] или ‘. выдвижение гипотез после того, как результаты известны’ .
Американское управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) ни в коем случае не является полным, но в рамках процесса подачи заявок на новые лекарства у него имеется большой репозиторий исследований РКИ.Перед проведением испытаний новых препаратов фармацевтические компании должны зарегистрировать их в FDA, что включает в себя предварительное определение первичных и вторичных показателей результатов и средств анализа. Предварительная спецификация необходима для обеспечения честности исследования и позволяет обнаружить, когда исследователи выборочно публикуют показатели, которые показывают результаты, которые спонсоры предпочитают после сбора и анализа данных, форма предвзятости исследователя, известная как HARKing [7] или ‘. выдвижение гипотез после того, как результаты известны’ .
Райзинг и др. [8] недавно опубликовали метаанализ всех испытаний эффективности новых лекарств, одобренных FDA с 2001 по 2002 год, и последующий статус публикации этих испытаний 5 лет спустя. Основные выводы:
Основные выводы:
• Вероятность публикации новых исследований по применению лекарственных средств с благоприятными исходами почти в пять раз выше, чем с неблагоприятными.
• 26,5% заранее определенных первичных исходов были исключены из журнальных статей об испытаниях новых лекарств.
• Из 43 основных показателей, не подтверждающих эффективность, 20 (47%) не были включены в опубликованные результаты.
• 17 показателей были представлены только в опубликованных исследованиях, и 15 из них продемонстрировали положительные эффекты нового препарата.
Анализ Rising et al. [8] документирует значительную предвзятость публикаций, которая преувеличивает очевидную эффективность новых лекарств. В дополнение к выборочной публикации положительных испытаний, что еще более тревожно, исследователи иногда не сообщают об отрицательных результатах заранее определенных первичных показателей исхода, в то же время подчеркивая в опубликованных исследованиях положительные результаты вторичного или даже нового измерения, как если бы это была их первичная мера. интерес.Помимо того, что они ставят под сомнение точность отчетов об испытаниях отдельных лекарств в журнальных статьях, их результаты также прямо ставят под сомнение достоверность мета-анализов, охватывающих конкретные лекарства и классы лекарств, когда они ограничены опубликованными исследованиями.
интерес.Помимо того, что они ставят под сомнение точность отчетов об испытаниях отдельных лекарств в журнальных статьях, их результаты также прямо ставят под сомнение достоверность мета-анализов, охватывающих конкретные лекарства и классы лекарств, когда они ограничены опубликованными исследованиями.
Было проведено несколько мета-анализов антидепрессантов с использованием хранилища данных FDA, чтобы избежать инфляционных эффектов предвзятости публикаций. В 2008 году Тернер и соавт. [9] проанализировали 74 испытания 12 антидепрессантов, чтобы оценить последующую предвзятость публикаций и ее влияние на кажущуюся эффективность.
Согласно их метаанализу, исследования антидепрессантов с благоприятными исходами публиковались в 16 раз чаще, чем с неблагоприятными. Однако, согласно научным обзорам FDA, только 38 испытаний (51%) выявили положительные различия между препаратом и плацебо, и 37 исследований были впоследствии опубликованы. FDA расценило оставшиеся 36 исследований как отрицательные (24 исследования) или сомнительные (12 исследований), то есть отсутствие различий в первичном исходе, но значительные результаты по вторичному показателю. Только 3 (8%) были опубликованы с отрицательными результатами, в то время как остальные 33 либо не были опубликованы (22 исследования), либо опубликованы как положительные (11 исследований), что противоречит выводам FDA. Подобно Rising et al. [8], Тернер и др. [9] сообщают, что в этих 11 исследованиях авторы не сообщали о своих отрицательных результатах по заранее заданному критерию основного исхода, а вместо этого выделяли положительные результаты по другому показателю, как если бы это был их основной показатель интереса.
Только 3 (8%) были опубликованы с отрицательными результатами, в то время как остальные 33 либо не были опубликованы (22 исследования), либо опубликованы как положительные (11 исследований), что противоречит выводам FDA. Подобно Rising et al. [8], Тернер и др. [9] сообщают, что в этих 11 исследованиях авторы не сообщали о своих отрицательных результатах по заранее заданному критерию основного исхода, а вместо этого выделяли положительные результаты по другому показателю, как если бы это был их основной показатель интереса.
Тернер и др. [9] затем сравнили размер эффекта, полученный из репозитория FDA, с размером эффекта из 51 опубликованного исследования. Этот анализ показал, что средневзвешенная величина эффекта в наборе данных FDA составляла скромные 0,31 (95% доверительный интервал, 0,27–0,35) по сравнению с 0,41 (95% доверительный интервал, 0,36–0,45) в опубликованных исследованиях, указывающих на 32% увеличение кажущаяся эффективность антидепрессантов. Их выводы аналогичны выводам Kirsch et al. [10] в 2002 г. в метаанализе 47 испытаний 6 антидепрессантов, одобренных FDA.Несмотря на статистическую значимость из-за большого комбинированного числа (n = 6944), они обнаружили, что средневзвешенная разница между группами по Шкале оценки депрессии Гамильтона (HRSD) из 17 пунктов составляла всего 1,8 балла, а в 57% испытаний не было обнаружено значительных различия между препаратом и плацебо [11].
[10] в 2002 г. в метаанализе 47 испытаний 6 антидепрессантов, одобренных FDA.Несмотря на статистическую значимость из-за большого комбинированного числа (n = 6944), они обнаружили, что средневзвешенная разница между группами по Шкале оценки депрессии Гамильтона (HRSD) из 17 пунктов составляла всего 1,8 балла, а в 57% испытаний не было обнаружено значительных различия между препаратом и плацебо [11].
Кирш и др. [10] и Kirsch и Antonuccio [12] также исследовали реакцию пациентов в зависимости от силы дозы и времени. Эти анализы не выявили преимущества более высоких доз антидепрессантов. Что касается распространенного мнения о том, что эффекты лекарств более устойчивы, чем эффекты плацебо, они обнаружили, что, хотя первоначальная положительная реакция пациентов на оба препарата со временем снижается, корреляция была выше для антидепрессантов (r = -0.84), чем плацебо (r = –0,62), что позволяет предположить, что эффекты антидепрессантов уменьшаются быстрее, чем эффекты плацебо.
В 2008 г. Kirsch et al. [13] изучали взаимосвязь между тяжестью депрессии и эффективностью во всех 35 исследованиях (n = 5133) четырех антидепрессантов нового поколения. Этот анализ не выявил клинически значимых различий (определяемых как разница между препаратом и плацебо ≥3 по шкале HRSD) между антидепрессантами и плацебо в зависимости от степени тяжести, за исключением пациентов с наиболее тяжелой депрессией (т.е. те, у кого показатель HRSD ≥29). Однако даже эта разница была обусловлена снижением реакции на плацебо у пациентов с более тяжелой депрессией, а не усилением реакции на антидепрессанты.
Kirsch et al. [13] изучали взаимосвязь между тяжестью депрессии и эффективностью во всех 35 исследованиях (n = 5133) четырех антидепрессантов нового поколения. Этот анализ не выявил клинически значимых различий (определяемых как разница между препаратом и плацебо ≥3 по шкале HRSD) между антидепрессантами и плацебо в зависимости от степени тяжести, за исключением пациентов с наиболее тяжелой депрессией (т.е. те, у кого показатель HRSD ≥29). Однако даже эта разница была обусловлена снижением реакции на плацебо у пациентов с более тяжелой депрессией, а не усилением реакции на антидепрессанты.
Также в 2008 г. Barbui et al. [14] проанализировали 40 исследований пароксетина (29 опубликованных/11 неопубликованных; n = 6391), в которых в качестве основного исхода использовалось досрочное прекращение исследования по любой причине (т.е. выбывание) и оценивали его как наилучший доступный «жесткий показатель эффективности и приемлемости лечения» [[14], с.296]. Их анализ не обнаружил различий между препаратом и плацебо по этому показателю, в отличие от вторичного показателя, заключающегося в том, что пароксетин клинически превосходил плацебо в отношении вероятности достижения пациентами ≥50% снижения симптомов депрессии. Они также обнаружили, что значительно больше пациентов выбыли из лечения пароксетином из-за побочных эффектов и повышенных суицидальных тенденций. При последующем анализе этих же исследований очевидное клиническое превосходство пароксетина исчезло после статистического контроля различий в побочных эффектах препарата/плацебо [[15], цитируется в [16], с.19]. Этот вывод аналогичен выводу Greenberg et al. [17] об исключительно высокой корреляции между побочными эффектами и улучшением в исследованиях флуоксетина/плацебо и предполагает, что, когда это действительно происходит, очевидное превосходство антидепрессантов может быть связано с раскрытием информации среди исследуемых пациентов (и оценивающих), учитывая большую частоту побочных эффектов. в группах активных препаратов и информирование пациентов об указанных эффектах в рамках информированного согласия [18,19]. Кирш [[16], стр. 7–22] и Кирш и Сапирштейн [20], среди прочих [18,19,21], утверждают, что побочные эффекты усиливают плацебо-эффекты антидепрессантов, подтверждая пациентам, что они принимают активное лекарство.
Они также обнаружили, что значительно больше пациентов выбыли из лечения пароксетином из-за побочных эффектов и повышенных суицидальных тенденций. При последующем анализе этих же исследований очевидное клиническое превосходство пароксетина исчезло после статистического контроля различий в побочных эффектах препарата/плацебо [[15], цитируется в [16], с.19]. Этот вывод аналогичен выводу Greenberg et al. [17] об исключительно высокой корреляции между побочными эффектами и улучшением в исследованиях флуоксетина/плацебо и предполагает, что, когда это действительно происходит, очевидное превосходство антидепрессантов может быть связано с раскрытием информации среди исследуемых пациентов (и оценивающих), учитывая большую частоту побочных эффектов. в группах активных препаратов и информирование пациентов об указанных эффектах в рамках информированного согласия [18,19]. Кирш [[16], стр. 7–22] и Кирш и Сапирштейн [20], среди прочих [18,19,21], утверждают, что побочные эффекты усиливают плацебо-эффекты антидепрессантов, подтверждая пациентам, что они принимают активное лекарство. тем самым повышая их ожидание улучшения.Учитывая часто небольшие различия между препаратами и плацебо в этих исследованиях, не потребовалось бы большого раскрытия ослепления, чтобы объяснить положительные результаты, когда они действительно происходят. С другой стороны, тот факт, что многие РКИ терпят неудачу, несмотря на значительные различия в побочных эффектах лекарств и плацебо, предполагает, что одних только указанных эффектов недостаточно, чтобы постоянно приводить к большему улучшению, даже если они способствуют снятию ослепления.
тем самым повышая их ожидание улучшения.Учитывая часто небольшие различия между препаратами и плацебо в этих исследованиях, не потребовалось бы большого раскрытия ослепления, чтобы объяснить положительные результаты, когда они действительно происходят. С другой стороны, тот факт, что многие РКИ терпят неудачу, несмотря на значительные различия в побочных эффектах лекарств и плацебо, предполагает, что одних только указанных эффектов недостаточно, чтобы постоянно приводить к большему улучшению, даже если они способствуют снятию ослепления.
Анализ, проведенный Rising et al. [8] и Тернер и соавт. [9] отмечают, что читатели должны быть осторожны, когда исследователи заменяют заранее заданный первичный критерий исхода новым.Эта озабоченность подкрепляется недавними анализами, документирующими широко распространенную выборочную отчетность о результатах в исследованиях, спонсируемых промышленностью, и инфляционный эффект, который часто возникает, когда заранее указанный первичный показатель результата не используется для сообщения результатов [22,23]. Возможно, наиболее тревожным следствием выводов Rising-Turner-Kirsch-Barbui является то, что читатели журналов, ищущие статьи для руководства доказательной практикой, могли быть введены в заблуждение мета-анализами и обзорами, основанными на предвзятых опубликованных статьях об эффективности антидепрессантов.
Возможно, наиболее тревожным следствием выводов Rising-Turner-Kirsch-Barbui является то, что читатели журналов, ищущие статьи для руководства доказательной практикой, могли быть введены в заблуждение мета-анализами и обзорами, основанными на предвзятых опубликованных статьях об эффективности антидепрессантов.
Однако некоторые объясняют лишь незначительное превосходство антидепрессантов тем фактом, что субъекты, включенные в РКИ, не всегда имеют адекватную тяжесть заболевания. Либерман и др. [24] заметили, что в ранние РКИ часто включались госпитализированные пациенты, которые были менее чувствительны к плацебо, тогда как в более поздние исследования обычно включались тщательно отобранные амбулаторные пациенты, с которыми связывались через рекламу в СМИ и которые могли страдать менее тяжелой депрессией. В метаанализе 75 РКИ, опубликованных в период с 1981 по 2000 г., Walsh et al.[25] показали, что ответ как на антидепрессанты, так и на плацебо со временем увеличивался со значительной положительной корреляцией между годом публикации и ответом. Parker [26] утверждает, что этот прогрессивно усиливающийся ответ на оба препарата ставит под угрозу способность отличать действительно эффективные антидепрессанты от плацебо, особенно у менее тяжелых пациентов.
Parker [26] утверждает, что этот прогрессивно усиливающийся ответ на оба препарата ставит под угрозу способность отличать действительно эффективные антидепрессанты от плацебо, особенно у менее тяжелых пациентов.
Фава и др. [27] отмечает, что анализ Walsh et al. [25], вероятно, занижает показатели ответа на плацебо, так как большинство неудавшихся испытаний остаются неопубликованными; по их оценкам, истинная скорость составляет 35–45%.Затем они исследуют различные потенциальные причины неудачных результатов испытаний (например, ошибки измерения или диагностическая неоднородность) и предлагают новый дизайн исследования, который мог бы снизить долю плацебо и, следовательно, количество, необходимое для дифференциации эффективных антидепрессантов от плацебо. И Фава с соавт. [27] и Otto и Nierenberg [28] отмечают, что только два РКИ, показывающие превосходство препарата, требуются для одобрения FDA, независимо от того, сколько их было проведено, и оба приводят пример пароксетина, для которого потребовалось девять испытаний, чтобы получить два необходимых для «выигрыша». ‘ Утверждение [29].Очевидное отсутствие значительных неблагоприятных последствий неудачных испытаний для фармацевтических компаний (кроме дополнительных затрат и задержки выхода на рынок), возможно, способствовало ориентированному на производство мышлению, отдающему предпочтение количеству испытаний, а не качеству (поскольку для победы требуется всего два, а потери не учитываются) слишком часто приводит к ошибкам в науке и, как следствие, к активным дебатам по поводу методологии и интерпретации, в то же время усугубляя разрыв между результатами испытаний и их применением в клинической практике.
‘ Утверждение [29].Очевидное отсутствие значительных неблагоприятных последствий неудачных испытаний для фармацевтических компаний (кроме дополнительных затрат и задержки выхода на рынок), возможно, способствовало ориентированному на производство мышлению, отдающему предпочтение количеству испытаний, а не качеству (поскольку для победы требуется всего два, а потери не учитываются) слишком часто приводит к ошибкам в науке и, как следствие, к активным дебатам по поводу методологии и интерпретации, в то же время усугубляя разрыв между результатами испытаний и их применением в клинической практике.
При анализе амбулаторных психиатрических больных с большим депрессивным расстройством (БДР) Zimmerman et al. [30] обнаружили, что из РКИ было бы исключено 86% из-за наличия у них сопутствующей тревожности или расстройства, связанного с употреблением психоактивных веществ, недостаточных депрессивных симптомов и/или текущих суицидальных мыслей. Точно так же апостериорный анализ пациентов STAR*D (Sequenced Treatment Alternatives to Reliever Depression), крупнейшее из когда-либо проводившихся исследований эффективности антидепрессантов, показал, что 77,8% были бы исключены из РКИ из-за исходного балла HRSD ≤19, более одно сопутствующее заболевание, более одного сопутствующего психического расстройства и/или текущий депрессивный эпизод продолжительностью >2 лет [31]. Этот анализ показал, что пациенты со STAR*D, которые соответствовали критериям включения в РКИ, имели большую вероятность ремиссии, чем те, которые более репрезентативны для подавляющего большинства обращающихся за медицинской помощью (показатель ремиссии 34,4 против 24,7%). Как Вишневский и соавт. [31] отмечают, что при включении большего числа репрезентативных пациентов результаты РКИ позволят лучше оценить пользу антидепрессанта на практике, а также могут снизить частоту ответа на плацебо и связанный с этим риск неудачных испытаний. Точно так же Паркер [[26], с. 2] утверждает, что кажущаяся ограниченная эффективность антидепрессантов может быть связана не со скромными эффектами этих соединений, а скорее с дизайном РКИ и методологическими проблемами, , где «яблоки», оцененные в таких исследованиях, не соответствуют «яблокам». апельсины» клинической практики» .
Этот анализ показал, что пациенты со STAR*D, которые соответствовали критериям включения в РКИ, имели большую вероятность ремиссии, чем те, которые более репрезентативны для подавляющего большинства обращающихся за медицинской помощью (показатель ремиссии 34,4 против 24,7%). Как Вишневский и соавт. [31] отмечают, что при включении большего числа репрезентативных пациентов результаты РКИ позволят лучше оценить пользу антидепрессанта на практике, а также могут снизить частоту ответа на плацебо и связанный с этим риск неудачных испытаний. Точно так же Паркер [[26], с. 2] утверждает, что кажущаяся ограниченная эффективность антидепрессантов может быть связана не со скромными эффектами этих соединений, а скорее с дизайном РКИ и методологическими проблемами, , где «яблоки», оцененные в таких исследованиях, не соответствуют «яблокам». апельсины» клинической практики» .
Хотя относительная эффективность антидепрессантов не установлена, прогресс будет достигнут только по мере того, как в РКИ будут участвовать репрезентативные образцы БДР, для которых предназначено лекарство, в условиях, имитирующих реальную практику. Такие испытания должны следовать рекомендациям Гаудиано и Герберта [19] по различению специфических и неспецифических эффектов лечения, первое из которых предполагает наличие активной группы плацебо, чтобы уменьшить вероятность раскрытия ослепления и, таким образом, контролировать потенциальную роль побочных эффектов в повышении ожидания пациентов улучшение.
Такие испытания должны следовать рекомендациям Гаудиано и Герберта [19] по различению специфических и неспецифических эффектов лечения, первое из которых предполагает наличие активной группы плацебо, чтобы уменьшить вероятность раскрытия ослепления и, таким образом, контролировать потенциальную роль побочных эффектов в повышении ожидания пациентов улучшение.
Эффективность антидепрессантов в реальных условиях
В соответствии с целью включения большего числа репрезентативных пациентов с БДР исследование STAR*D, финансируемое NIMH [32,33,34,35,36,37,38]:
• включено 4041 реальный пациент, обращающийся за помощью, по сравнению с людьми, откликнувшимися на рекламу депрессивных субъектов;
• включал пациентов с сопутствующими медицинскими и психическими заболеваниями, а также тех, у кого текущий эпизод БДР был >2 лет;
• включены пациенты, в настоящее время проходящие курс лечения антидепрессантами, при условии, что в анамнезе не было случаев отсутствия ответа или непереносимости антидепрессантов протокола шага 1 или шага 2;
• использовали « ремиссия » по сравнению с « ответ » в качестве основного критерия успешного лечения, что является более высоким клиническим стандартом, чем используемый в предыдущих исследованиях эффективности;
• в течение 12 месяцев обеспечивалось непрерывное лечение при мониторинге устойчивости эффектов лечения по сравнению с сообщением только об улучшении неотложной помощи.
Программа STAR*D предоставляла бесплатную неотложную и непрерывную помощь очень высокого качества, чтобы максимизировать вероятность того, что пациенты с БДР достигнут ремиссии и сохранят ее. В таблице 1 подробно описаны высокое качество лечения и масштабные усилия STAR*D по удержанию пациентов. Протокол лечения включал современную неотложную помощь для достижения ремиссии с последующим 1 годом непрерывного лечения для всех пациентов, у которых был достигнут удовлетворительный клинический ответ. Целью продолжения лечения было поддержание ремиссии и предотвращение рецидива [[39], с.15].
Таблица 1
Высочайшее качество неотложной и продолжающейся помощи для достижения максимальных ремиссий при минимизации рецидивов и случаев выбывания
Фаза непрерывной помощи STAR*D также стала проверкой в реальных условиях практических рекомендаций Американской психиатрической ассоциации (APA). ) что «после ремиссии пациенты, которых лечили антидепрессантами в острой фазе, должны продолжать принимать эти препараты для предотвращения рецидива» [[40], p. 15]. Это руководство получило наивысший рейтинг доверия экспертной группы.
15]. Это руководство получило наивысший рейтинг доверия экспертной группы.
STAR*D был разработан в качестве руководства при выборе наилучшего следующего шага лечения для многих пациентов, которым не удалось получить адекватного облегчения после первоначального испытания селективных ингибиторов обратного захвата серотонина (СИОЗС) путем оценки относительной эффективности одиннадцати фармакологически различные методы лечения [41]. Когнитивная терапия (КТ) также была вариантом на этапе 2, но слишком мало пациентов включили ее в качестве приемлемого лечения, в результате чего после рандомизации был получен только 101 дополнительный данные [33].Таким образом, КТ была исключена из статей о первичном переключении и дополнении шага 2 [33,34]. Возможные причины столь малого числа пациентов, считавших КТ приемлемыми, включали: (1) предвзятый самостоятельный выбор, поскольку все пациенты начинали лечение циталопрамом на этапе 1; (2) дополнительные расходы на КТ, которые STAR*D не покрывал, в то время как он покрывал все расходы на лекарства и визиты к врачу, и (3) пациенты, прошедшие КТ, должны были пойти в другое место, чтобы увидеть нового специалиста, не являющегося врачом [42], стр. 748–749]. Несмотря на эти препятствия, в последующей статье STAR*D сообщалось, что у 101 пациента 2-й ступени, получавших CT (либо отдельно, либо в комбинации с циталопрамом), наблюдались такие же показатели ответа и ремиссии, как и у пациентов, получавших медикаментозную стратегию [42]. ], п.739].
В заключительном разделе статьи о дизайне исследования STAR*D говорится: ‘STAR * D использует рандомизированный контролируемый дизайн для оценки как теоретических принципов, так и клинических убеждений, которые в настоящее время определяют ведение терапевтически резистентной депрессии с точки зрения симптомов, функции, удовлетворенности, бремени побочных эффектов, использования медицинских услуг и оценок затрат. Учитывая недостаток контролируемых данных, результаты должны иметь существенное значение для общественного здравоохранения и науки, поскольку они получены в репрезентативных группах/условиях участников с использованием инструментов клинического управления, которые можно легко применять в повседневной практике» [[43], с.136].
Учитывая «значительную общественную и научную значимость» STAR*D для оценки эффективности антидепрессантов при их оптимальной доставке реальным пациентам, крайне важно, чтобы методология и результаты STAR*D были представлены точно.
Изменение одного из показателей исхода
В соответствии с замыслом HRSD был предварительно заданным первичным показателем STAR*D, а Инвентаризация депрессивной симптоматики (IDS-C30) — вторичным для выявления ремиссированных ‘(т.е. те, у кого показатель ≤7 HRSD) и « ответивших » (т.е. те, у кого ≥50% снижение депрессивных симптомов) пациенты [[41], p. 476, [43], с. 123]. Эти показатели были получены оценщиками результатов исследований (ROA), которые не знали о назначении лечения при входе и выходе из каждого уровня лечения, а также каждые 3 месяца в течение продолжающегося лечения. Дополнительные показатели оценки симптомов, уровня функционирования, удовлетворенности, качества жизни, бремени побочных эффектов и обращения за медицинской помощью были получены с помощью телефонной системы интерактивного голосового ответа (IVR) по тому же графику, что и HRSD и IDS-C30 [[43] , п.129] (табл. 2).
Таблица 2
Анализ выживаемости по этапам лечения пациентов, которые начали лечение в состоянии ремиссии первоначальное испытание СИОЗС. Из-за высокого процента отсева из исследования в STAR*D, что часто приводило к отсутствию оценок выхода IDS-C30 и HRSD (и, таким образом, требуемый уровень условного исчисления делал эти оценки относительно неинформативными), план статистического анализа был пересмотрен с учетом информации, полученной от отдела безопасности данных и Плата мониторинга перед блокировкой и разблокировкой данных.
В пересмотренном статистическом аналитическом плане STAR*D был исключен IDS-C30 и заменен на Быстрый перечень депрессивной симптоматики-самоотчет (QIDS-SR), инструмент, разработанный главными исследователями STAR*D, который очень коррелирует с HRSD (первичный показатель), поскольку он вводился при каждом посещении [44,45,46]. В исследованиях с этапа 1 по этап 4 QIDS-SR был вторичным показателем для выявления ремиссий и единственным показателем для выявления ответивших на лечение, в то время как HRSD был основным показателем для выявления пациентов с ремиссией [32,33,34,35,36, 37].
Изначально планировалось, что STAR*D использует QIDS-SR двумя способами. В исследовательской версии IVR вводили по тому же графику, что и другие меры на этапах 1–4, и в качестве «промежуточной» ежемесячной меры во время продолжающегося лечения [[39], с. 120, табл. 3].
Пациенты также заполняли бумажно-карандашный опросник QIDS-SR в начале каждого визита в клинику вместе с двумя самооценками побочных эффектов и опросником по приверженности лечению. Эти четыре самооценки находились под наблюдением неслепых координаторов клинических исследований, которые просматривали результаты, чтобы убедиться, что все пункты были выполнены, а затем видели, как пациент выполняет QIDS-C (версия, проводимая врачом, с идентичными 16 вопросами и ответами). варианты, такие как QIDS-SR), Шкала улучшения общего клинического впечатления, и обсудить с пациентом любые симптомы и побочные эффекты, которые он/она испытывает, а также предоставить обучающие материалы для пациентов [[39], с.75].
Затем координаторы клинических исследований записали шесть показателей в форму истории болезни для рассмотрения лечащим врачом до того, как он/она осмотрит пациента , «чтобы предоставить непротиворечивую информацию клиницистам, которые используют эту информацию в протоколе» [[43] , п. 128]. Таким образом, бумажно-карандашный QIDS-SR был одним из «инструментов клинического управления, которые можно легко применять в повседневной практике» [[43], с. 136] STAR*D и используется как таковая в «основанной на измерениях» системе помощи STAR*D, как указано в STAR*D: «Для повышения качества и согласованности лечения врачи использовали систему поддержки принятия клинических решений. которые основывались на измерении симптомов (QIDS-C и QIDS-SR), побочных эффектов (оценка частоты, интенсивности и тяжести), приверженности лечению (самостоятельный отчет) и клинической оценке, основанной на прогрессе пациента ‘ [[ 32], с.30]. Это различие между первоначально предполагаемым использованием QIDS-SR в качестве клинического инструмента по сравнению с исследовательской мерой четко указано в обеих таблицах статьи о дизайне (таблицы 2, 3) [[43], стр. 128–129] и в Руководстве по клиническим процедурам. STAR*D (табл. 2, 4) [[39], стр. 119, 121].
Таблица 3
Показатели ремиссии и прекращения лечения в STAR*D по этапам лечения
Таблица 4
Показатели ремиссии HRSD и QIDS-SR
Пересмотренный план статистического анализа не изменил ни одного из результатов сравнения следующего шага STAR *D, так как и QIDS-SR, и HRSD не выявили значительных групповых различий между видами лечения во всех пяти сравнениях.Однако это решение, по-видимому, завысило зарегистрированные показатели ремиссии и ответа STAR*D. Как указано в статье шага 1: «Более высокие показатели ремиссии были обнаружены с QIDS-SR, чем с HRSD, потому что наш первичный анализ классифицировал пациентов с отсутствующим выходом HRSD как неремиттирующих априори. Из 690 пациентов с отсутствующими показателями HRSD на выходе 152 (22,1%) достигли ремиссии QIDS-SR на последнем лечебном визите [[32], с. 34]. В шести исследованиях с этапа 1 по этап 4 было выявлено 1192 ремиссии по HRSD по сравнению с 1398 ремиссиями QIDS-SR, что на 17 больше.3% (таблица 4), а основная сводная статья STAR*D использовала QIDS-SR только для описания пошаговых результатов неотложной и продолжающейся помощи [38].
Изменение критериев приемлемости для анализа
В статье шага 1 STAR*D указано, что подходящие пациенты «имели непсихотическое большое депрессивное расстройство, определяемое по исходному показателю HRSD ≥ 14′ [[32], п. 29]. Это скромный порог тяжести симптомов (см., например, Davidson et al. [47] с порогом включения ≥20 HRSD), хотя он аналогичен многим пациентам с БДР, обращающимся за лечением [30].
Из 4790 пациентов, прошедших скрининг HRSD (время завершения: 15 минут [[39], стр. 118]), 4041 пациент начал лечение циталопрамом во время исходного визита [[39], стр. 118]. 17, [48]]. Из этих пациентов 3110 набрали ≥14 баллов по более тщательному и слепому HRSD, проводимому с помощью ROA (время завершения: 20–25 минут [39], стр. 118]), 234 из которых не явились на контрольный визит. Для полученных 2876 пациентов этапа 1, подходящих для анализа [[32], рис. 1], их исходные баллы по шкале HRSD составили в среднем 21,8 [32,] таблица 1, ряд 2].Также было 607 пациентов, которые, как сообщается, были исключены (но позже включены — см. обсуждение ниже), потому что их балл <14 означал только легкую депрессию, и 324 пациента, как сообщается, были исключены (но позже включены), потому что у них не было исходного HRSD, назначенного ROA [[32], инжир. 1].
В последующих статьях STAR*D со 2-го по 4-й этапы по-прежнему утверждалось, что все пациенты имели «непсихотическое большое депрессивное расстройство» , и не разъяснялось отклонение от приемлемости шага 1 для критериев анализа [32, 33,34,35,36,37].В частности, 607 пациентов, которые набрали <14 баллов по исходной оценке ROA, наряду с 324 пациентами, не имевшими такой оценки, получали циталопрам на этапе 1, переходили к последующим неотложным и продолжающим лечением и были включены в этапы со 2 по 4. статьях, а также в сводной статье. Таким образом, у 931 из 4041 пациента STAR*D (23%) не было HRSD ≥14, назначенного ROA, на момент включения в исследование.
Включение данных этих пациентов привело к снижению среднего значения HRSD шага 1 с 21.от 8 до 19,9 [[38], табл. 2, ряд 2]. STAR*D также включил этих 931 пациента для пересчета частоты ремиссии циталопрама на этапе 1 в своей сводной статье. При этом показатель ремиссии шага 1 был завышен до 36,8% по сравнению с исходными 32,8% статьи шага 1, основанной на мягком определении QIDS-SR.
Возможно, более серьезной проблемой является попытка определить влияние этих 931 пациентов на изменение частоты рецидивов во время продолжения лечения. Тяжесть начальных симптомов является мощным прогностическим фактором рецидива — у менее депрессивных пациентов вероятность рецидива гораздо ниже.Для пациентов, включенных в исследование с HRSD <14, возникает особая загадка, поскольку STAR*D определяет рецидив как HRSD ≥14. Это означает, что 607 пациентов, чтобы считаться рецидивирующими, должны были иметь более низкие баллы во время продолжающегося лечения, чем при первом включении в исследование.
Кроме того, отсутствие учета отсева позволило STAR*D заявить о 67% «кумулятивной» частоте ремиссии после четырех этапов лечения [[38], с. 1910]. Авторы STAR*D получили эту цифру, просто сложив завышенные значения ремиссий QIDS-SR на этапах 1–4.STAR*D признает, что это утверждение предполагает отсутствие отсева и тот же уровень ремиссии для персистирующих пациентов, что и для выбывших. Эти предположения, однако, неверны в реальном мире и, конечно, неверны в STAR*D, поскольку на каждом этапе больше пациентов выбывало из исследования, чем имело ремиссию (таблица 3). Кроме того, сравнение показателей стойкой ремиссии пациентов с выбывшими невозможно, поскольку выбывание не дает данных.
В таблице 3 представлены показатели ремиссии и выбывания STAR*D, определенные HRSD, для этапов 1–4.Эти данные очень важны для клинического понимания эффективности антидепрессантов у реальных пациентов, получающих «основанное на измерениях» современное лечение:
• на этапе 1 у 25,4% пациентов наступила ремиссия. выбыло 26,6% [49];
• на этапе 2 у 25,1% пациентов наступила ремиссия, а 30,1% выбыли;
• на этапе 3 у 17,8% пациентов наступила ремиссия, а 44,8% выбыли;
• на этапе 4 у 10,1% пациентов была ремиссия, а у 60.1% выбыл.
Результаты непрерывного лечения
Один из наиболее важных вопросов при оценке антидепрессантов — насколько длительны ремиссии. Основным вкладом STAR*D было предоставление данных наблюдения за 12 месяцами о продолжении лечения пациентов с ремиссией и улучшением состояния. Пациентам, достигшим ремиссии во время неотложной помощи, настоятельно рекомендовалось продолжить лечение. Кроме того, пациентам, ответившим на лечение, которым не удалось достичь ремиссии и которые не хотели переходить к следующему этапу неотложной помощи, было рекомендовано продолжить лечение.
В протоколе непрерывного лечения «настоятельно рекомендуется, чтобы участники продолжали принимать ранее эффективные препараты для неотложной помощи в дозах, используемых при неотложной терапии» [[38], с. 1908]. Эта рекомендация согласуется с руководством APA по фазе продолжения лечения, согласно которому «после ремиссии пациенты, получавшие лечение антидепрессантами в острой фазе, должны продолжать принимать эти препараты для предотвращения рецидива» [[40], с. 15]. Однако протокол STAR*D был более натуралистичен, чем руководство APA, в котором врачам разрешалось делать «любую психотерапию, лекарства или изменение дозы лекарств» [[38], с.1908] они сочли необходимым максимизировать вероятность сохранения ремиссии у пациентов. Это включало планирование дополнительных посещений в случае возвращения депрессивных симптомов и/или появления непереносимых побочных эффектов [[39], с. 78].
STAR*D приложила большие усилия, чтобы максимизировать удержание и собрать последующие данные. Эти усилия включали в себя дальнейшее использование всех стратегий удержания пациентов в неотложной помощи во время непрерывного лечения, информирование пациентов перед всеми телефонными звонками для оценки результатов исследования и выплату пациентам 25 долларов США.00 за прохождение указанных оценок, а также за разрешение пациентам оставаться в исследовании, если они переехали из этого района (таблица 1). Кроме того, информированное согласие было повторно получено для всех пациентов, поступающих на постоянное лечение, чтобы обеспечить их понимание его лечения и процедур оценки результатов и ожиданий [[39], с. 68].
Для оценки результатов продолжающегося лечения авторы STAR*D решили использовать QIDS-SR с IVR, который изначально предназначался только как промежуточный ежемесячный показатель во время продолжающегося лечения [[39], с.120, таблица 3], а не предварительно указанные HRSD и IDS-C30. Если пациент вызывался и набирал ≥11 баллов по шкале QIDS-SR, объявлялся рецидив; эта оценка (соответствующая HRSD ≥14) указывала на депрессию от умеренной до более тяжелой степени. Учитывая это, важно отметить, что STAR*D не сообщал о частоте устойчивых ремиссий у пациентов, находящихся в ремиссии, а только о частоте, с которой у них возникали рецидивы, оставаясь при продолжении лечения.
При расчете рецидива авторы STAR*D решили не использовать процедуры намерения лечить, в которых отсев считался бы отказом в продолжении лечения (несмотря на отдельный процесс получения информированного согласия), а вместо этого использовали данные пациентов, которые звонили в IVR. систему один раз (или более) в течение 12 месяцев.Рассчитанная частота рецидивов представляла собой долю пациентов с рецидивом среди тех, кто сделал хотя бы один такой звонок и сообщил о ≥11 QIDS-SR [[38], таблица 5, столбец 6, сноска d).
Согласно этому определению рецидива, пациенты, продолжающие лечение, которые выбыли из исследования досрочно и никогда не обращались за помощью, или многие пациенты, которые обращались один или несколько раз без баллов ≥11, а затем выбыли, никогда не могли соответствовать критерию рецидива. Поскольку вероятность рецидива увеличивается со временем наблюдения, это определение смещено в сторону недооценки частоты рецидивов.Обычно пациенты теряют надежду, когда депрессивные симптомы возвращаются, что увеличивает вероятность прекращения лечения, которое больше не эффективно для них. Это особенно верно для 75% пациентов STAR*D с диагнозом «рецидивирующая депрессия» [[38], таблица 2]. Учитывая, что у большинства пациентов со STAR*D была «повторяющаяся» депрессия, а «потеря надежды» является одним из наиболее распространенных симптомов депрессии, разумно ожидать, что у многих пациентов, прекративших лечение, возникали рецидивы.
Сводный отчет STAR*D идентифицирует 1854 пациентов с ремиссией на этапах 1–4 [[38], таблица 3, строка 8], но только 1518 согласились на продолжение лечения [[38], таблица 5, столбец 2], в то время как другие 336 выбыло. Многие из этих пациентов достигли своей ремиссии на основе бумажно-карандашного QIDS-SR во время своего последнего визита в клинику, но затем прекратили лечение, не приняв HRSD, несмотря на оплату в размере 25 долларов США за выполнение указанной меры (например, в статье шага 1 говорится, «Из 690 пациентов с отсутствующими показателями HRSD на выходе 152 (22.1%) достигли ремиссии QIDS-SR на последнем лечебном визите» [[32], с. 34]. Еще 344 пациента согласились на продолжение лечения, но затем выбыли в течение 1-го месяца, так и не позвонив в систему IVR [[38], таблица 5, столбец 5]. Это указывает на то, что 670 из 1854 пациентов в ремиссии (36,7%) STAR*D выбыли в течение 1 месяца после ремиссии QIDS-SR. Однако из-за открытого назначения окончательный результат для этих пациентов (и всех выбывших на любом этапе) неясен, поскольку пациенты могли продолжать лечение, не оставаясь в STAR * D, оплачивая свои лекарства и услуги врача, которые до этого были бесплатными. .Учитывая, что такое решение требовало принятия этой новой стоимости, которая могла быть существенной, особенно для одной трети, у которой не было страхового покрытия [[38], таблица 1], маловероятно, что многие выбывшие из программы STAR*D продолжали лечение антидепрессантами. ).
Средневзвешенная частота рецидивов STAR*D для пациентов в ремиссии, которые хотя бы один раз звонили в свою систему IVR, составила 37,4% (диапазон: от 33,5% для пациентов с этапом 1 до 50% для пациентов с этапом 4) и 64,4% для пациентов с улучшенным состоянием. пациенты, которые поступили на непрерывную терапию не в стадии ремиссии (диапазон: от 58.от 6% для стадии 1 до 83,3% для пациентов стадии 4) [[38], таблица 5, столбец 6]. В таблице 2 представлен анализ выживаемости 1518 пациентов, которые поступили на постоянное лечение в стадии ремиссии. Цифры в таблице 2 представляют пациентов в ремиссии, которые «выжили» , т.е. не имели рецидива или выбыли. Рецидивы течения представляют собой безуспешно леченных больных. Выбывшие представляют также безуспешно пролеченных пациентов, рассматриваемых с точки зрения намерения лечить. Авторы STAR*D подчеркнули свои выводы о том, что частота рецидивов у 90 383 была выше у тех, кто начал последующее наблюдение после большего количества этапов лечения (p 90 384 < 90 383 0.0001)’ [[38], с. 1911] и «ремиссия на момент начала последующего наблюдения была связана с лучшим прогнозом, чем простое улучшение без ремиссии» [[38], с. 1912]. Хотя оба утверждения статистически точны, они не учитывают тот факт, что у пациентов со STAR*D наблюдались чрезвычайно высокие показатели рецидивов и/или случаев выбывания в ходе продолжающегося лечения, независимо от этапа лечения, на котором наступила их ремиссия, или степени улучшения неотложной помощи до начала лечения. постоянный уход.
Эти результаты ставят под сомнение рекомендации APA по фазе продолжения лечения, согласно которым «после ремиссии пациенты, которые лечились антидепрессантами в острой фазе, должны продолжать принимать эти препараты для предотвращения рецидива» , несмотря на то, что эта рекомендация получила наивысшую оценку ‘ клиническая достоверность» рейтинг экспертной комиссии [[40], с.15].
Обсуждение
Учитывая стоимость в 35 миллионов долларов и продуманный дизайн, STAR*D предоставляет редкую возможность оценить эффективность антидепрессантов на реальных пациентах и, следовательно, требует анализа с нескольких точек зрения, независимых от взглядов ее авторов. Хотя аналогично анализу Fava et al. [50], документируя постепенное снижение показателей ремиссии с увеличением частоты рецидивов и непереносимости лекарств, наш анализ показал, что результаты STAR*D выглядят даже хуже, чем предполагалось ранее.Даже при экстраординарной помощи STAR*D только около четверти пациентов достигли ремиссии на этапе 1. Уровень выбывания из исследования был немного выше, чем показатель успеха. Успешность шага 2 была немного меньше, чем у шага 1, а процент отсева был больше. Показатели успеха на шаге 3 (17,8%) и шаге 4 (10,1%) были еще более скромными с еще более высокими показателями отсева (44,8 и 60,1% соответственно).
Из 4041 пациента, начавшего лечение циталопрамом, 370 (9,2%) прекратили лечение в течение 2 недель.После четырех испытаний, в каждом из которых применялись энергичные дозы лекарств от «до , гарантировалось, что вероятность достижения ремиссии была максимальной, а те, кто не достиг ремиссии, действительно были устойчивы к лекарству» [[32], с. 30], только 1854 пациента (45,9%) достигли ремиссии по мягким критериям QIDS-SR. На каждом этапе выбывало больше пациентов, чем было переведено, и этот показатель выбывания неуклонно увеличивался на протяжении всего исследования. Из 1854 пациентов в ремиссии 670 (36.7%) выбыли в течение 1 месяца после ремиссии, и только 108 (5,8%) выжили при продолжении лечения и прошли окончательную оценку без рецидива и/или выбывания. Даже для этих 108 пациентов неясно, сколько из них были одним из 607, чей исходный уровень HRSD <14 означал только легкие симптомы, когда они впервые начали принимать циталопрам на этапе 1, и, следовательно, должны были иметь более низкие баллы во время продолжения лечения, чем когда они впервые вошли в исследование, чтобы быть считается рецидивом.
В STAR*D неудачные испытания имели негативные последствия для пациентов, помимо отсутствия ремиссии.Такие неудачи снижали вероятность достижения ремиссии у пациентов в последующих испытаниях, но повышали вероятность непереносимости препарата, рецидива и/или выбывания из исследования. Эти негативные эффекты подтверждают наблюдения Fava et al. [[50], с. 262], что последовательные фармакологические манипуляции «могут перевести депрессивное заболевание в рефрактерную фазу» путем поощрения оппозиционной толерантности, при которой антидепрессант делает некоторых пациентов чувствительными к депрессии. Шуинар и Шуинар [[51], с.75] документируют аналогичные риски при применении атипичных нейролептиков и оценивают, что 50% случаев резистентной к лечению шизофрении связаны с психозом сверхчувствительности. Остается решить следующий вопрос: в какой степени ухудшение результатов STAR*D связано с развитием у подмножества такой оппозиционной толерантности, естественным снижением ожиданий пациентов в отношении улучшения после каждой неудачи (т. е. постепенно уменьшающимся эффектом плацебо), другие неизвестные факторы и/или их комбинация.
Наиболее важно для клиницистов то, что результаты STAR*D показывают, что антидепрессанты были лишь минимально эффективны у реальных пациентов, когда их применение соответствовало «теоретическим принципам и клиническим убеждениям, которые в настоящее время определяют лечение резистентной к лечению депрессии» [[43 ], п. 136]. Эта, по общему признанию, суровая оценка наиболее очевидна при использовании показателей завершения исследования в качестве наилучшего «жесткого показателя эффективности и приемлемости лечения» [[14], с. 296].
Тернер и др. [9] демонстрирует, как предвзятость публикаций завышает предполагаемую эффективность антидепрессантов, тем самым способствуя широкому распространению этого лечения. Отдельные анализы Turner et al. [9] и Кирш и соавт. [10] предполагают, что антидепрессанты лишь незначительно эффективны по сравнению с инертными плацебо, хотя результаты этих исследований могут быть связаны с недопредставленностью пациентов с менее выраженными симптомами и более выраженной сопутствующей патологией (в частности, с тревожными расстройствами, которые, как было установлено, снижают частоту ответа на антидепрессанты [10]. 52]) и давнее депрессивное заболевание, которые лучше характеризуют большинство обращающихся за помощью.Анализ Barbui et al. [[15], цит. по [16], с. 19] демонстрирует, как очевидное клиническое превосходство пароксетина над плацебо исчезло после статистического контроля различий в побочных эффектах препарата/плацебо, предполагая, что побочные эффекты способствуют раскрытию информации в РКИ и тем самым повышают ожидания пациентов в отношении улучшения, поскольку они часто правильно угадывают, что получают «настоящий» препарат и, следовательно, ожидают улучшения. Подобный анализ необходим для исследований по усилению антипсихотических/плацебо-антидепрессантов для «лечебно-резистентной депрессии» из-за значительных профилей побочных эффектов нейролептиков и той роли, которую они могут играть в раскрытии ослепления.Такой анализ имеет решающее значение для правильной оценки недавнего мета-анализа Нельсона и Папакостаса [53], в котором было обнаружено, что атипичные нейролептики превосходят плацебо в качестве усиливающих агентов, поскольку этот анализ не учитывал указанные различия в побочных эффектах препарата/плацебо и тот факт, что этот очевидный «превосходство» было исключительно скромным: 9 — это количество, необходимое для лечения, чтобы получить одну дополнительную ремиссию в испытаниях продолжительностью всего 6–8 недель.
Что еще мы можем узнать из STAR*D и обзорных статей? Во-первых, даже с примерными фармацевтическими усилиями трудно добиться устойчивого выздоровления пациентов, отражающих диапазон тяжести заболевания STAR*D.Во-вторых, результаты испытаний эффективности (будь то лекарства, психотерапия, основанная на доказательствах, или любое другое лечение) ограничены в своей способности оценивать пользу от лечения в той степени, в какой «яблока» оценивались в таких исследованиях. не соответствуют «апельсинам» клинической практики [26]. Анализ Циммермана и соавт. [30] и Wisniewski et al. [31] еще больше подчеркивают это фундаментальное несоответствие между пациентами РКИ и теми, кто чаще всего обращается в реальную клиническую практику.В-третьих, тот факт, что показатель эффективности КИ на этапе 2 был не выше, чем у антидепрессантов, подчеркивает, что БДР — с его общими сопутствующими заболеваниями и рецидивирующим характером — представляет собой серьезное, сложное и трудно поддающееся лечению расстройство, лечение которого часто приводит к меньшему количеству положительных результатов, чем можно было бы ожидать от испытаний эффективности двух наиболее широко исследованных вмешательств.
В-четвертых, стоит подумать, не мешала или не помогала система STAR*D, основанная на измерениях, с ее акцентом на измерении побочных эффектов и симптомов при каждом посещении до достижения « ремиссии » в уходе за пациентами.Авторы STAR*D явно полагали, что это помогло, и даже приравняли «высококачественная помощь» к своей системе, утверждающей: «Наконец-то была оказана высококачественная помощь (уход на основе измерений) при дополнительной поддержке со стороны координатора клинических исследований. Следовательно, результаты в этом отчете могут превзойти те, которые в настоящее время получены в повседневной практике, когда ни симптомы, ни побочные эффекты не измеряются последовательно и когда практикующие врачи сильно различаются по времени и уровню дозирования» [[38], с.1914]. STAR*D рекомендовал всем пациентам, не достигшим ремиссии на основе числа, участвовать в следующем испытании, несмотря на то, что QIDS/HRSD не смог дифференцированно взвесить основные депрессивные симптомы (например, настроение, чувство вины, суицидальные мысли или ангедония) и сопутствующие симптомы (например, аппетит, бессонница или возбуждение) [54,55] и самооценка пациентами относительной важности каждого из них. В отсутствие значимого терапевтического альянса между пациентом и врачом, полагаясь вместо этого на перечисление пациентами побочных эффектов и симптоматических изменений для руководства лечением, STAR*D, возможно, не смог извлечь выгоду из важного ингредиента, необходимого для улучшения состояния пациента.Напротив, психосоматические методы, вероятно, улучшили бы удержание пациентов и результаты, учитывая использование более клинически богатых процедур клиниметрической оценки, совместное принятие решений и их акцент на повышении самоэффективности пациентов путем обучения их навыкам самоконтроля, которые являются важными. вероятно, необходимо для поддержания восстановления после БДР [56]. Такие психосоматические методы являются по своей сути «психотерапевтическими» и, вероятно, улучшат результаты любого вмешательства, будь то антидепрессант, плацебо или какая-либо другая стратегия; особенно при лечении депрессивных — часто изначально беспомощных и безнадежных — пациентов и их часто встречающихся сопутствующих заболеваний.
В-пятых, рекомендации АПА по продолжению и поддерживающей фазе, которые по существу поощряют неограниченное использование антидепрессантов в «тех же полных дозах антидепрессантов» , что и при остром лечении, кажутся ошибочными [[40], с. 15]. Хотя рекомендации APA согласуются с метаанализом, проведенным Geddes et al. [57] и Папакостас и соавт. [58], сообщая о больших размерах эффекта антидепрессантов в предотвращении рецидива, эти анализы не учитывают предвзятость публикаций [59,60] и выборочное сообщение о результатах [22,23], оба из которых могут значительно завышать результаты метаанализов, которые не увенчались успехом. контролировать эти распространенные формы предвзятости исследователя.На данный момент проспективные натуралистические исследования, вероятно, являются лучшим руководством для оценки реальных результатов. В STAR*D даже из 1085 пациентов с ремиссией на этапе 1, которые согласились на продолжение лечения и, следовательно, имели самую высокую вероятность устойчивого выздоровления, только у 84 (7,7%) не было рецидива и/или выбывания к 12-му месяцу продолжения лечения. . Результаты STAR*D аналогичны выводам Bockting et al. [61], что только 42% использовали антидепрессанты непрерывно во время поддерживающей фазы лечения, из которых у 60,4% возникали рецидивы, тогда как у пациентов, прекративших прием антидепрессантов, рецидивы наблюдались реже, и только у 8% из тех, кто получал профилактическую КТ, рецидивы.Эти натуралистические исследования фазы продолжения подтверждают гипотезу Фава [62,63] о том, что длительное применение антидепрессантов может ухудшить течение депрессии. Помимо этих исследований, неспособность найти какую-либо очевидную пользу от продолжительного лечения антидепрессантами, недавние данные о том, что длительное применение СИОЗС в умеренных/высоких суточных дозах удваивает риск диабета [64], а также неопределенный риск оппозиционной толерантности, дают дополнительные сведения. причин для пересмотра этой слишком распространенной практики.
Наконец, в свете скудных результатов исследования STAR*D, стоит пересмотреть термин «резистентная к лечению депрессия» применительно к пациентам, которые плохо реагируют на медикаментозное лечение.Не следует ли нам обратить наше внимание на то, что не так с нашим лечением, вместо того, чтобы классифицировать некоторых пациентов как страдающих экзотической формой депрессии, потому что они не реагируют? Нашему пониманию мешает использование формулировок, ошибочно подразумевающих наличие исключительной подгруппы пациентов, невосприимчивых к эффективному в других отношениях лечению. Неизбежный вывод из результатов STAR*D заключается в том, что нам необходимо более серьезно изучить другие формы лечения (и их комбинации), которые могут быть более эффективными.Эти усилия потребуют разработки новых моделей предоставления услуг, чтобы обеспечить широкое внедрение таких методов лечения по мере их определения [65,66].
Несмотря на широко распространенное мнение об эффективности антидепрессантов и когнитивной терапии (КТ) среди врачей и общества в целом, STAR*D показывает, что антидепрессанты и КТ не приводят к устойчивым положительным эффектам для большинства людей, которые их получают. Авторы STAR*D отметили в начале исследования, что «результаты должны иметь существенное общественное здравоохранение и научное значение» .Как медицинские работники и в соответствии с тем, что рекомендуют сами авторы STAR*D, мы должны обратить внимание на то, что говорит нам это крупнейшее из когда-либо проводившихся испытаний эффективности антидепрессантов, и переоценить роль антидепрессантов и КТ в научно обоснованном лечении депрессии.
Благодарности
Авторы хотели бы поблагодарить обоих рецензентов, чьи проницательные комментарии и предложения были неоценимы для улучшения статьи.
Конфликт интересов
Н.Эдмунд Пиготт, доктор философии, и Грегори С. Альтер, доктор философии, являются основателями NeuroAdvantage, LLC, коммерческой нейротерапевтической компании. В течение последних 3 лет доктор Пиготт консультировал CNS Response, Midwest Center for Stress and Anxiety и SmartBrain Technologies.
Ссылки
- Саймс Р.Дж.: Предвзятость публикации: случай для международного реестра клинических испытаний.Дж. Клин Онкол 1986; 4: 1529–1541.
- Дикерсин К.: Существование систематической ошибки публикации и факторов риска ее возникновения. ДЖАМА 1990; 263:1385–1389.
- Дикерсин К.: Насколько важна предвзятость публикации? Синтез имеющихся данных.AIDS Educ Prev 1997; 9:15–21.
- Чан А.В., Хробьяртссон А., Хаар М.Т., Гётше П.К., Альтман Д.Г.: Эмпирические данные для выборочного сообщения результатов в рандомизированных исследованиях: сравнение протоколов с опубликованными статьями. ДЖАМА 2004; 291:2457–2465.
- Krleža-Jeric K, Chan AW, Dickersin K, Sim I, Grimshaw J, Gluud C: Принципы международной регистрации протокольной информации и результатов испытаний медицинских вмешательств на людях: Оттавское заявление (часть 1).BMJ 2005; 330: 956–958.
- Чан А.В.: Предвзятость, подтасовка и предоставление ложных сведений: время для полного доступа к протоколам и результатам испытаний. PLoS Med 2008;5:e230.
- Керр Н.Л.: HARKing: выдвижение гипотез после того, как известны результаты.Pers Soc Psychol Rev 1998; 2: 196–217.
- Rising K, Bacchetti P, Bero L: Предвзятость в сообщениях об испытаниях лекарств, представленных в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов: обзор публикации и презентации. PLoS Med 2008;5:e217.
- Тернер Э.Х., Мэтьюз А.М., Линардатос Э., Телль Р.А., Розенталь Р.: Выборочная публикация испытаний антидепрессантов и ее влияние на очевидную эффективность.N Engl J Med 2008; 358: 252–260.
- Кирш И., Мур Т., Скобория А., Николс С.: Новые лекарства императора: анализ данных о лечении антидепрессантами, представленных в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Prev Treat 2002;5:статья 23.
- Кирш И., Скобория А., Мур Т.Дж.: Антидепрессанты и плацебо: секреты, открытия и вопросы без ответов.Prev Treat 2002; 5: статья 33.
- Кирш И., Антонуччо Д.: Антидепрессанты против плацебо: существенных преимуществ не хватает. Psych Times, 19 сентября 2002 г.
- Кирш И., Дикон Б., Уэдо-Медина Т.Б., Мур Т.Дж., Джонсон Б.Т.: Начальная тяжесть и преимущества антидепрессантов: метаанализ данных, представленных в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов.PLoS Med 2008;5:e45.
- Barbui C, Furukawa TA, Cipriani A: Эффективность пароксетина при лечении острой большой депрессии у взрослых: систематический пересмотр опубликованных и неопубликованных данных рандомизированных исследований. CMAJ2008;178:296–305.
- Barbui C, Cipriani A, Kirsch I: Опосредовано ли разделение эффективности пароксетина и плацебо побочными эффектами? Представлен систематический пересмотр рандомизированных двойных слепых исследований.
- Кирш I: Новые лекарства императора: Развенчание мифа об антидепрессантах. Лондон, Бодли-Хед, 2009 г.
- Гринберг Р.П., Борнстейн Р.Ф., Зборовски М.Дж., Фишер С., Гринберг М.Д.: метаанализ результатов применения флуоксетина при лечении депрессии.J Nerv Ment Dis 1994; 182: 547–551.
- Антонуччо Д.О., Дантон В.Г., ДеНельски Г.Ю., Гринберг Р.П., Гордон Дж.С.: Поднятие вопросов об антидепрессантах. Psychother Psychosom 1999; 68: 3–14.
- Гаудиано Б.А., Герберт Д.Д.: Методологические вопросы клинических испытаний антидепрессантов: перспективы исследования результатов психотерапии.Psychother Psychosom 2005; 74: 17–25.
- Кирш И., Сапирштейн Г.: Слушая прозак, но слушая плацебо: метаанализ антидепрессантов. Prev Treat 1998;1:статья 0002a.
- Монкрифф А., Коэн Д.: Переосмысление моделей действия психотропных препаратов.Psychother Psychosom 2005; 74: 145–153.
- Матье С., Бутрон И., Мохер Д., Альтман Д.Г., Раво П.: Сравнение зарегистрированных и опубликованных первичных исходов в рандомизированных контролируемых исследованиях. ДЖАМА 2009; 302:977–984.
- Ведула С.С., Беро Л., Шерер Р.В., Дикерсин К.: Отчетность о результатах спонсируемых промышленностью испытаний габапентина для использования не по прямому назначению.N Engl J Med 2009; 361: 1963–1971.
- Либерман Дж. А., Гринхаус Дж., Хамер Р. М., Кришнан К. Р., Немерофф С. Б., Шихан Д. В., Тасе М. Э., Келлер М. Б.: Сравнение эффектов антидепрессантов: согласованные рекомендации по оценке количественных обзоров эффективности антидепрессантов. Нейропсихофармакология 2005; 30:445–460.
- Уолш Б.Т., Сейдман С.Н., Сиско Р., Гулд М.: Реакция плацебо в исследованиях большой депрессии: переменная, существенная и растущая. ДЖАМА 2002; 287: 1840–1847.
- Паркер Дж.: Испытание антидепрессантов: насколько достоверны доказательства? Бр. Дж. Психиатрия, 2009; 194:1–3.
- Фава М., Эвинс Э., Дорер Д.Дж., Шенфельд Д.А.: Проблема реакции на плацебо в клинических испытаниях психических расстройств: виновники, возможные средства и новый подход к дизайну исследования. Psychother Psychosom 2003; 72: 115–127.
- Отто М.В., Ниренберг А.А.: Чувствительность анализа, неудачные клинические испытания и ведение науки.Psychother Psychosom 2002; 71: 241–243.
- Хупер М., Амстердам Д.Д.: Отражают ли клинические испытания потенциал лекарства? Обзор оценки FDA новых антидепрессантов. 39-я встреча NCDEU Annu, Бока-Ратон, июнь 1998 г.
- Циммерман М., Маттиа Д.И., Постернак М.А. Являются ли участники испытаний фармакологического лечения депрессии репрезентативными для пациентов в обычной клинической практике? Am J Psychiatry 2002; 159: 469–473.
- Wisniewski SR, Rush AJ, Nierenberg AA, Gaynes BN, Warden D, Luther JF, McGrath PJ, Lavori PW, Thase ME, Fava M, Trivedi MH: Можно ли обобщить результаты испытаний антидепрессантов III фазы на клиническую практику? Отчет STAR*D. Am J Psychiatry 2009; 166: 599–607.
- Trivedi MH, Rush AJ, Wisniewski SR, Nierenberg AA, Warden D, Ritz L, Norquist G, Howland RH, Lebowitz B, McGarth PJ, Shores-Wilson K, Biggs MM, Balasubramani GK, Fava M: Оценка результатов с циталопрамом для депрессия с использованием лечения, основанного на измерениях, в STAR*D: последствия для клинической практики.Am J Psychiatry 2006; 163: 28–40.
- Rush AJ, Trivedi MH, Wisniewski SR, Stewart JW, Nierenberg AA, Thase ME, Ritz L, Biggs MM, Warden D, Luther JF, Shores-Wilson K, Niederehe G, Fava M: бупропион-SR, сертралин или венлафаксин- XR после неэффективности СИОЗС при депрессии. N Engl J Med 2006; 354: 1231–1242.
- Trivedi MH, Fava M, Wisniewski SR, Thase ME, Quitkin F, Warden D, Ritz L, Nierenberg AA, Lebowitz BD, Biggs MM, Luther JF, Shores-Wilson K, Rush AJ: Медикаментозная аугментация после неэффективности СИОЗС при депрессии . N Engl J Med 2006; 354: 1243–1252.
- Fava M, Rush AJ, Wisniewski SR, Nierenberg AA, Alpert JE, McGrath PJ, Thase ME, Warden D, Biggs MM, Luther JF, Niederehe G, Ritz L, Trivedi MH: сравнение миртазапина и нортриптилина после двух последовательных неудачных лекарств амбулаторное лечение депрессивных больных: отчет STAR*D.Am J Psychiatry 2006; 163: 1161–1172.
- Ниренберг А.А., Фава М., Триведи М.Х., Вишневски С.Р., Тейз М.Е., МакГрат П.Дж., Альперт Дж.Е., Уорден Д., Лютер Дж.Ф., Нидерехе Г., Лебовиц Б.Д., Шорс-Уилсон К., Раш А.Дж.: Сравнение аугментации литием и Т3 после двух неудачное медикаментозное лечение депрессии: отчет STAR*D.Am J Psychiatry 2006; 163: 1519–1530.
- McGrath PJ, Stewart JW, Fava M, Trivedi MH, Wisniewski SR, Nierenberg AA, Thase ME, Davis L, Biggs MM, Shores-Wilson K, Luther JF, Niederehe G, Warden D, Rush AJ: Транилципромин в сравнении с венлафаксином плюс миртазапин, следующие три неудачных испытания антидепрессантов для лечения депрессии: отчет STAR*D.Am J Psychiatry 2006; 163: 1531–1541.
- Rush AJ, Trivedi MH, Wisniewski SR, Nierenberg AA, Stewart JW, Warden D, Niederehe G, Thase ME, Lavori PW, Lebowitz BD, McGrath PJ, Rosenbaum JF, Sackheim HA, Kupfer DJ, Luther J, Fava M: Acute and долгосрочные результаты у амбулаторных пациентов с депрессией, требующих одного или нескольких этапов лечения: отчет STAR*D.Am J Psychiatry 2006; 163: 1905–1917.
- Триведи М.Х., Стегман Д., Раш А.Дж., Вишневски С.Р., Ниренберг А.А.: Руководство по клиническим процедурам STAR*D. 31 июля 2002 г. www.edc.pitt.edu/stard/public/study_manuals.html (по состоянию на 1 июня 2009 г.).
- Практические рекомендации по лечению пациентов с большим депрессивным расстройством, изд. 2.Вашингтон, Американская психиатрическая ассоциация, 2000 г.
- Fava M, Rush AJ, Trivedi MH, Nierenberg AA, Thase ME, Sackeim HA, Quitkin FM, Wisniewski SR, Lavori PW, Rosenbaum JF, Kupfer DJ: Предыстория и обоснование исследования альтернатив последовательного лечения для облегчения депрессии (STAR*D) .Психиатр Clin North Am 2003; 26: 457–494.
- Thase ME, Friedman ES, Biggs MM, Wisniewski SR, Trivedi MH, Luther JF, Fava M, Nierenberg AA, McGrath PJ, Warden D, Niederehe G, Hollon SD, Rush AJ: Когнитивная терапия по сравнению с медикаментозной аугментацией и переключением стратегий в качестве секунданта -этапное лечение: отчет STAR*D.Am J Psychiatry 2007; 164: 739–752.
- Раш А.Дж., Фава М., Вишневски С.Р., Лавори П.В., Триведи М.Х., Сакем Х.А., Тасе М.Е., Ниренберг А.А., Куиткин Ф.М., Кашнер Т.М., Купфер Д.Дж., Розенбаум Д.Ф., Альперт Дж., Стюарт Д.В., МакГрат П.Дж., Биггс М.М., Шорс- Уилсон К., Лебовиц Б.Д., Ритц Л., Нидерехе Г.: Альтернативы последовательного лечения для облегчения депрессии (STAR*D): обоснование и дизайн.Испытания Control Clin 2004; 25: 119–142.
- Раш А.Дж., Триведи М.Х., Ибрагим Х.М., Кармоди Т.Дж., Амов Б., Кляйн Д.Н., Марковиц Дж.К., Нинан П.Т., Корнштейн С., Манбер Р., Тасе М.Е., Кочиш Дж.Х., Келлер М.Б.: Быстрый перечень симптомов депрессии из 16 пунктов (QIDS) ), клинический рейтинг (QIDS-C) и самоотчет (QIDS-SR): психометрическая оценка пациентов с хронической большой депрессией.Биол Психиатрия 2003; 54: 573–583.
- Раш А.Дж., Триведи М.Х., Кармоди Т.Дж., Ибрагим Х.М., Марковиц Дж.К., Кейтнер Г.И., Корнштейн С.Г., Арноу Б., Кляйн Д.Н., Манбер Р., Даннер Д.Л., Геленберг А.Дж., Кочиш Д.Х., Немерофф К.Б., Фосетт Д., Тазе М.Э., Рассел Д.М. , Джоди Д.Н., Борлан Ф.Е., Келлер М.Б.: Самоотчетные показатели депрессивных симптомов: чувствительность к обнаружению изменений в рандомизированном контролируемом исследовании амбулаторных пациентов с хронической депрессией, не страдающих психозом.Нейропсихофармакология 2005; 30:405–416.
- Раш А.Дж., Бернстайн И.Х., Триведи М.Х., Кармоди Т.Дж., Вишневски С., Мундт Дж.К., Шорс-Уилсон К., Биггс М.М., Ниренберг А.А., Фава М.: оценка экспресс-инвентаризации депрессивной симптоматики и рейтинговой шкалы Гамильтона для депрессии: Отчет об испытаниях альтернатив последовательного лечения для облегчения депрессии.Биол Психиатрия 2006; 59: 493–501.
- Дэвидсон Дж. Р., Гадде К. М., Фэрбанк Дж. А. и др.: Эффект зверобоя продырявленного (зверобоя) при большом депрессивном расстройстве: рандомизированное контролируемое исследование. ДЖАМА 2002; 287: 1807–1814.
- Wisniewski SR: специалист по биостатистике STAR*D, личное сообщение, 1 июля 2008 г.
- Warden D, Trivedi MH, Wisniewski SR, Davis L, Nierenberg AA, Gaynes BN, Zisook S, Hollon SD, Balasubramani GK, Howland R, Fava M, Stewart JW, Rush AJ: Predictors истощения во время начального (циталопрам) лечения депрессии : отчет STAR*D. Am J Psychiatry 2007; 164: 1189–1197.
- Фава Г.А., Томба Э., Гранди С.: Путь к выздоровлению от депрессии – не езди сегодня по вчерашней карте. Psychother Psychosom 2007; 76: 260–265.
- Chouinard G, Chouinard VA: Атипичные нейролептики: исследование CATIE, двигательное расстройство, вызванное лекарствами, и возникающие в результате ятрогенные психические симптомы, психоз сверхчувствительности и синдром отмены отмены.Psychother Psychosom 2008; 77: 69–77.
- Фава М., Юбелакер Л.А., Альперт Дж.Е., Ниренберг А.А., Пава Дж.А., Розенбаум Дж.Ф. Основные депрессивные подтипы и ответ на лечение. Биол Психиатрия 1997;42:568-576.
- Нельсон Дж. К., Папакостас Г. И.: Атипичная антипсихотическая аугментация при большом депрессивном расстройстве: метаанализ плацебо-контролируемых рандомизированных исследований.Am J Psychiatry 2009; 166: 980–991.
- Faravelli C: Оценка психопатологии. Psychother Psychosom 2004; 73: 139–141.
- Фава Г.А., Руини С., Рафанелли С.: Психометрическая теория является препятствием для прогресса клинических исследований.Psychother Psychosom 2004; 73: 145–148.
- Фава Г.А., Сонино Н.: Психосоматическая оценка. Psychother Psychosom 2009; 78: 333–341.
- Geddes JR, Carney SM, Davies C, Furukawa TA, Kupfer DJ, Frank E, Goodwin GM: Профилактика рецидивов с помощью лечения антидепрессантами при депрессивных расстройствах: систематический обзор.Ланцет 2003; 361: 653–661.
- Папакостас Г.И., Перлис Р.Х., Скалиа М.Дж., Петерсен Т.Дж., Фава М.: Метаанализ показателей раннего устойчивого ответа между антидепрессантами и плацебо для лечения большого депрессивного расстройства. J Clin Psychopharmacol 2006; 26: 56–60.
- Фава Г.А., Руини С., Сонино Н.: Лечение рецидивирующей депрессии: последовательный психотерапевтический и психофармакологический подход.CNS Drugs 2003;17:1109–1117.
- Торнтон А., Ли П.: Предвзятость публикации в метаанализе: ее причины и последствия. J Clin Epidemiol 2000; 53: 207–216.
- Bockting CLH, Doesschate MC, Spijker J, Spinhoven P, Koeter MWJ, Schene AH, Исследовательская группа DELTA: Продолжение и поддерживающее использование антидепрессантов при рецидивирующей депрессии.Psychother Psychosom 2008; 77: 17–26.
- Фава Г.А.: Повышают ли антидепрессанты и успокаивающие препараты хронизацию аффективных расстройств? Psychother Psychosom 1994; 61: 125–131.
- Фава Г.А.: Может ли длительное лечение антидепрессантами ухудшить течение депрессии? Дж. Клин Психиатрия 2003; 64: 123–133.
- Андерсон Ф., Шаде Р., Суисса С., Гарбе Э.: Длительное применение антидепрессантов при депрессивных расстройствах и риск развития сахарного диабета. Am J Psychiatry 2009; 166: 591–598.
- Marks I: Клиники психического здоровья в 21 веке.Psychother Psychosom 2009; 78: 133–138.
- Фава Г.А., Парк С.К., Дубовский С.Л.: Психиатрическая клиника: новая модель. Всемирная психиатрия 2008; 7: 177–181.
Автор Контакты
Ed Pigott, PhD
7111 Moorland Drive
Clarksville, MD 21029 (США)
Тел.+1 443 812 9497, факс +1 301 854 0577
Электронная почта [email protected]
Информация о статье / публикации
Предварительный просмотр первой страницы
Получено: 09 июля 2009 г.
Принято: 22 февраля 2010 г.
Опубликовано онлайн: 09 июля 2010 г.
Дата выпуска выпуска: август 2010 г.
Количество печатных страниц: 13
Количество фигурок: 0
Количество столов: 4
ISSN: 0033-3190 (печать)
eISSN: 1423-0348 (онлайн)
Для получения дополнительной информации: https://www.karger.com/PPS
Авторское право / Дозировка препарата / Отказ от ответственности
Авторское право: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или любую систему хранения и поиска информации, без письменного разрешения издателя. .
Дозировка препарата: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор препарата и дозировка, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством.
Отказ от ответственности: заявления, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и участникам, а не издателям и редакторам.Появление рекламы и/или ссылок на продукты в публикации не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор(ы) отказываются от ответственности за любой ущерб, нанесенный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании или рекламе.




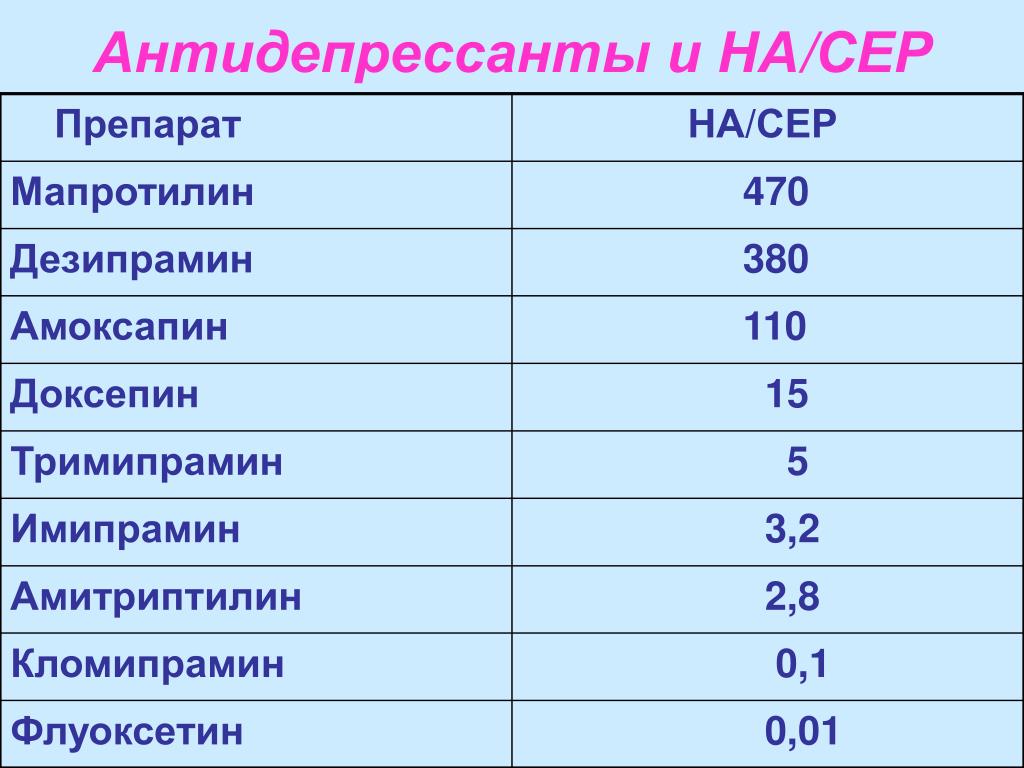 Птицы — это, можно сказать, цветы небесные. И во многих ситуациях, особенно в городских условиях, если мы оставим их без помощи, то они с нами сосуществовать не будут. Останутся, может быть, только вороны и голуби, но ведь этого мало», — рассуждает он.
Птицы — это, можно сказать, цветы небесные. И во многих ситуациях, особенно в городских условиях, если мы оставим их без помощи, то они с нами сосуществовать не будут. Останутся, может быть, только вороны и голуби, но ведь этого мало», — рассуждает он.